100 câu trắc nghiệm Kim loại kiềm, Kim loại kiềm thổ, Nhôm có lời giải (nâng cao – phần 2)
Với 100 câu trắc nghiệm Kim loại kiềm, Kim loại kiềm thổ, Nhôm có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm câu trắc nghiệm Kim loại kiềm, Kim loại kiềm thổ, Nhôm.
100 câu trắc nghiệm Kim loại kiềm, Kim loại kiềm thổ, Nhôm có lời giải (nâng cao – phần 2)
Thi online Hóa 12 KNTTThi online Hóa 12 CDThi online Hóa 12 CTST
Bài giảng: Bài tập trọng tâm về kim loại kiềm, kim loại kiềm thổ và nhôm - Cô Nguyễn Thị Thu (Giáo viên VietJack)
Câu 41. Cho 19 gam hỗn hợp gồm kim loại M ( hóa trị không đổi ) và Zn (có tỉ lệ mol tương ứng là 1,25:1) và bình đựng 4,48 lít khí Cl2 (đktc), sau các phản ứng hoàn toàn thu được hỗn hợp chất rắn X. Cho X tan hết trong dung dịch HCl (dư) thấy có 5,6 lít khí H2 thoát ra (đktc). Kim loại M là
A. Mg B. Al
C. Ca D. Na
Lời giải:
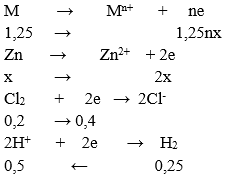
BT e ⇒ 1,25nx + 2x = 0,4 + 0,5 = 0,9 (1)
Mặt khác: 1,25M + 65M = 19 (2)
Từ (1) và (2) ⇒ (1,25M +65)/(1,25n + 2) = 19/0,9 ⇒ n = 2; M = 24(Mg)
→ Đáp án A
Câu 42. Cho m gam bột Al vào cốc chứa V lít dung dịch NaOH 2M, sau phản ứng hoàn toàn cho tiếp vào dung dịch HCl vào cốc đó đến khi kết tủa tan hết thấy cần dùng 800ml dung dịch HCl 1M và có 3,36 lít khí thoát ra (ở đktc). Giá trị của m và V lần lượt là
A. 6,075 và 0,2500
B. 7,425 và 0,0625
C. 3,375 và 0,2500
D. 6,075 và 0,0625
Lời giải:
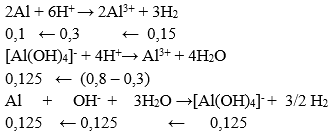
⇒ m = (0,125 + 0,1).27 = 6,075 g
⇒ Vdd NaOH = 0,125/2 = 0,0625 lít
→ Đáp án D
Câu 43. Cho dung dịch chứa 6,595 gam muối clorua của kim loại kiềm thuộc hai chu kì liên tiếp và dung dịch AgNO3 (dư), thu được 15,785 gam kết tủa. Phần trăm khối lượng của muối có khối lượng phân tử nhỏ là:
A. 92,719% B. 11,296%
C. 7,281% D. 88,704%
Lời giải:
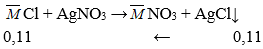
⇒ M + 35,5 = 6,595/0,11
⇒ M = 24,45 ⇒ M1 = 23 (Na) < M < M2 = 39 (K)
Ta có: a + b = 0,11 (1)
58,5a + 74,5b = 6,595 (2)
⇒ a = 0,1, b = 0,01
⇒ % mNaCl = (0,1.58,5.100%)/6,595 = 88,7%
→ Đáp án D
Câu 44. Cho 13,44 lít khí clo (ở đktc) đi qua 2,5 lít dung dịch KOH ở 100oC. Sau khi phản ứng xảy ra hoàn toàn, thu được 37,25 gam KCl. Dung dịch KOH trên có nồng độ là
A. 0,24M. B. 0,48M.
C. 0,2M. D. 0,4M.
Lời giải:
nKCl = 35,25/74,5 = 0,5 mol; nCl2 = 13,44/22,4 = 0,6 mol
2KOH (1mol) + Cl2 (0,6) → KCl (0,5) + KClO + H2O
CM KOH = 1/2,5 = 0,4 M
→ Đáp án D
Câu 45. Dung dịch X chứa hỗn hợp gồm Na2CO3 1,5M , KHCO3 1M. Nhỏ từ từ từng giọt cho đến hết 200ml dung dịch HCl 1M vào 100 ml dung dịch X, sinh ra V lít khí (ở đktc). Giá trị của V là :
A. 4,48 B. 3,36
C. 2,24 D. 1,12
Lời giải:
nCO32- = 0,15 mol; nHCO3- = 0,1 mol; nH+ = 0,2 mol
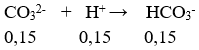
nH+ còn lại = 0,2 – 0,15 = 0,05 mol
nHCO3- = 0,1 + 0,15 = 0,25 mol
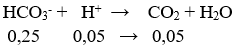
⇒ V = 0,05.22,4 = 1,12 lít
→ Đáp án D
Câu 46. Cho 3,024 gam một kim loại M tan hết trong dung dịch HNO3 loãng, thu được 940,8 ml khí NxOy (sản phẩm khử duy nhất, ở đktc) có tỉ khối đối với H2 bằng 22. Khí NxOy và kim loại M là
A. NO và Mg. B. N2O và Al
C. N2O và Fe. D. NO2 và Al.
Lời giải:
MKhí = 22 chứng tỏ NxOy là N2O duy nhất
nN2O = 0,042 mol
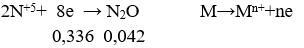
BT e ⇒ ne = 0,036 mol ⇒ nM = 0,036/n
Khi đó M = 3,024/(0,336:n)
M = 9n ⇒ n = 3, M = 27 ⇒ Chọn Al
→ Đáp án B
Câu 47. Dung dịch X chứa hỗn hợp gồm Na2CO3 1,5M và KHCO3 1M. Nhỏ từ từ từng giọt cho đến hết 200 ml dung dịch HCl 1M vào 100 ml dung dịch X, sinh ra V lít khí (ở đktc). Giá trị của V là
A. 4,48. B. 1,12.
C. 2,24. D. 3,36.
Lời giải:
Số mol CO32- = 0,15 (mol); số mol HCO3- = 0,1(mol); số mol H+ = 0,2(mol)
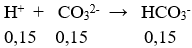
Tổng số mol HCO3- = 0,25 mol;
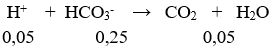
VCO2 = 0,05.22,4 = 1,12 (lít)
→ Đáp án B
Câu 48. Cho m gam bột Mg vào 500ml dung dịch FeCl3 1M. Sau khi phản ứng xảy ra hoàn toàn, khối lượng dung dịch thay đổi 2,4 gam so với dung dịch ban đầu ( nước bay hơi, không đáng kể). Giá trị nào của m trong các giá trị sau là không thỏa mãn ?
A. 2,4 B. 12,3
C. 8,7 D. 9,6
Lời giải:
Mg + 2Fe3+ → Mg2+ + 2Fe2+ (1)
+) Nếu Mg hết Fe3+ còn ⇒ m = 2,4
+) Nếu Mg còn, Fe3+ hết
(1) ⇒ nMg = 1/2 nFe3+ = 0,25 mol
Mg + Fe2+ → Mg2+ + Fe (2)
• Nếu Δm↓ = 24(x + 0,25) – 56x = 2,4 ⇒ x = 0,1125 mol
⇒ m = (0,25 + 0,1125).24 = 8,7 g
• Nếu Δm↑ = -24(x + 0,25 ) + 56x = 2,4 ⇒ x = 0,2625 mol
⇒ m = (0,25 + 0,2625).24 = 12,3 g
→ Đáp án D
Câu 49. Cho 100ml dung dịch AlCl3 1M tác dụng với 200ml dung dịch NaOH. Kết tủa tạo thành được làm khô và nung đến khối lượng không đổi cân nặng 2,55g. Tính nồng độ dung dịch NaOH ban đầu.
A. 0,75 M B. 1,75M
C. 1M D. 1,25M
Lời giải:
Số mol AlCl3 là: nAlCl3 = 0,1.1 = 0,1 (mol)
Số mol Al2O3 là: nAl2O3 = 2,55/102 = 0,025 (mol)
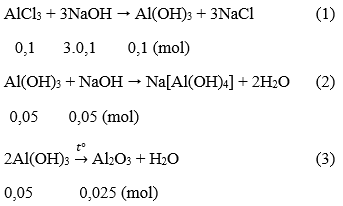
Theo pt(3) ta thấy số mol Al(OH)3 còn lại là 0,05 mol
Như vậy đã có: 0,1 - 0,05 = 0,05 mol Al(OH)3 đã bị hòa tan.
Từ (1) và (2) số mol NaOH = 3.0,1 + 0,05 = 0,35 (mol)
Nồng độ mol/l CM (NaOH) = 0,35/0,2 = 1,75M
→ Đáp án B
Câu 50. Hấp thụ hoàn toàn 2,688 lít CO2 (đktc) vào 2,5 lít dung dịch Ba(OH)2 có nồng độ a mol/l, thu được 15,76 gam kết tủa. Giá trị của a là:
A. 0,032 B. 0,048
C. 0,06 D. 0,04
Lời giải:
Ta có: nCO2 = 2,688/22,4 = 0,12 mol;
nBaCO3 = 11,82/197 = 0,06 mol
Do nCO2 ≠ nBaCO3 nên ngoài BaCO3 còn có Ba(HCO3)2 được tạo thành.

Theo phản ứng: ∑nBa(OH)2 = 0,08 + 0,02 = 0,1 mol
a = 0,1/2,5 = 0,04M
→ Đáp án D
Câu 51. Trộn 5,4g bột Al với 17,4g bột Fe3O4 rồi tiến hành phản ứng nhiệt nhôm (giả sử chỉ xảy ra phản ứng khử Fe2O3 thành Fe). Hòa tan hoàn toàn hỗn hợp rắn sau phản ứng bằng dung dịch H2SO4 loãng, dư thì thu được 5,376 lít H2 (dktc). Hiệu suất của phản ứng nhiệt nhôm là:
A. 62,5% B. 60%
C. 20% D. 80%
Lời giải:
Ta có: nAl = 5,4/27 = 0,2 mol
nFe3O4 = 17,4/232 = 0,075 mol
nH2 = 5,376/22,4 = 0,24 mol
8Al (8/3 x) + 3Fe3O4 (x) → 9Fe (3x) + 4Al2O3
Gọi số mol Fe3O4 phản ứng là x mol
Vì hiệu suất không đạt 100% nên cả Al và Fe3O4 đều chưa phản ứng hết.
Hỗn hợp rắn sau phản ứng gồm Al dư, Fe3O4 dư, Al2O3 và Fe.
Theo phản ứng: nAl phản ứng = 8/3 x mol ⇒ Al dư = (0,2 - 8/3 x) mol
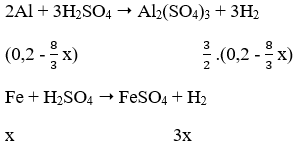
⇒ 3/2. (0,2 - 8x/3) + 3x = 0,24 ⇒ x = 0,06 mol
Vậy H = (0,06/0,075). 100% = 80%
→ Đáp án D
Câu 52. Cho 0,448 lít khí CO2 (ở đktc) hấp thụ hết vào 100 ml dung dịch chứa hỗn hợp NaOH 0,06M và Ba(OH)2 0,12M, thu được m gam kết tủa. Giá trị của m là
A. 3,940. B. 1,182.
C. 2,364. D. 1,970.
Lời giải:
nOH- = 0,006 + 2.0,012 = 0,03(mol)
nCO2 = 0,02(mol). Có: 1 < (nOH-)/nCO2 < 2 nên tạo ra 2 ion số mol bằng nhau = 0,01mol
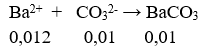
Khối lượng kết tủa = 0,01. 197 = 1,97(g)
→ Đáp án D
Câu 53. Nhỏ từ từ từng giọt đến hết 30 ml dung dịch HCl 1M vào 100 ml dung dịch chứa Na2CO3 0,2M và NaOH 0,2M , sau phản ứng thu được số mol CO2 là:
A. 0,03 B. 0,01
C. 0,02 D. 0,015
Lời giải:
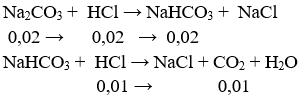
⇒ nCO2 = 0,01 mol
→ Đáp án B
Câu 54. Hòa tan hết 17,94 gam một kim loại kiềm vào một lượng nước du thu được dung dịch X. Cho dung dịch X tác dụng với 36,92 gam P2O5 thì thu được dung dịch Y chỉ chứa hai muối có nồng độ mol bằng nhau. Kim loại kiềm là
A. Na B. Rb
C. K D. Li
Lời giải:
nH3PO4 = 2nP2O5 = 2.36,92/142 = 0,52 mol
M + H2O → MOH + 1/2 H2 ↑
Phản ứng xảy ra theo thứ tự:
H3PO4 + MOH → MH2PO4 + H2O
MH2PO4 + MOH → M2HPO4 + H2O
MH2PO4 + MOH → M3PO4 + H2O
Xét hai trường hợp:
TH1: Hai muối là M2HPO4 và MH2PO4 ⇒ nMH2PO4 = nM2HPO4 = 0,26
nM = nMH2PO4 + 2nM2HPO4 = 0,78 mol ⇒ M = 17,94/0,78 = 23(Na)
TH2: Hai muối là: M2HPO4 và M3PO4 ⇒ nM2HPO4 = nM3PO4 = 0,26
nM = 2nM2HPO4 + 3nM3PO4 = 1,3 mol ⇒ M = 17,94/1,3 = 13,8(loại)
→ Đáp án A
Câu 55. Trộn 5,4 gam bột Al với 17,4 gam bột Fe3O4 rồi tiến hành phản ứng nhiệt nhôm (trong điều kiện không có không khí). Giả sử chỉ xảy ra phản ứng khử Fe3O4 thành Fe. Hòa tan hoàn toàn chất rắn sau phản ứng bằng dung dịch H2SO4 loãng (dư) thu được 5,376 lít khí H2 (ở đktc). Hiệu suất phản ứng nhiệt nhôm và số mol H2SO4 đã phản ứng là:
A. 75 % và 0,54 mol B. 80 % và 0,52 mol
C. 75 % và 0,52 mol D. 80 % và 0,54 mol
Lời giải:
nAl = 0,2 mol; nFe3O4 = 0,075 mol; nH2 = 0,24 mol
Phản ứng xảy ra không hoàn toàn: 8Al (x) + 3Fe3O4 → 4Al2O3 (0,5x) + 9Fe
Hòa tan chất rắn (Fe, Al dư) vào H2SO4 ⇒ H2
BT e ta có: 2.nFe + 3.nAl = 2.nH2
⇒ 9/8.x.2 + (0,2 – x).3 = 0,24.2 → x = 0,16 mol → Hphản ứng = 0,16/0,2 = 80%
BT e ⇒ nH+phản ứng = 2.nFe + 3.nAl + 6.nAl2O3 + 8.nFe3O4 = 0,36 + 0,12 + 0,48 + 0,12 = 1,08 mol
→ nH2SO4 phản ứng = 1,08/2 = 0,54mol
→ Đáp án D
Câu 56. Hấp thụ hoàn toàn 3,36 lít khí CO2 (ở đktc) vào m gam dung dịch hỗn hợp chứa 0,05 mol NaOH; 0,05mol KOH; 0,05 mol Ba(OH)2. Dung dịch sau phản ứng có khối lượng?
A. (m – 11,65) gam
B. (m + 6,6) gam
C. (m – 5,05) gam
D. (m – 3,25) gam
Lời giải:
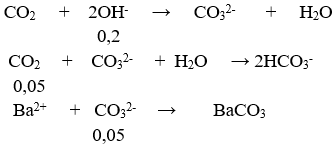
⇒ mdd = m + 0,15.44 – 197.0,05 = (m – 3,25) gam
→ Đáp án D
Câu 57. Trộn 100 ml dung dịch hỗn hợp gồm H2SO4 0,05M và HCl 0,1M với 100 ml dung dịch hỗn hợp gồm NaOH 0,2M và Ba(OH)2 0,1M thu được dung dịch X. Dung dịch X có pH là
A. 1,2 B. 1,0
C. 12,8 D. 13,0
Lời giải:
nH+ = 0,1(2. CM H2SO4 + CM HCl ) = 0,02;
nNaOH = 0,1[CM NaOH + 2CM Ba(OH)2] = 0,04.
H+ + OH- → H2O dư 0,02 mol OH-.
[OH-] = 0,02/(0,1 + 0,1) = 0,1 = 10-1.
[H+] = 10-13 ⇒ pH = 13
→ Đáp án D
Câu 58. Hoà tan hoàn toàn 8,94 gam hỗn hợp gồm Na, K và Ba vào nước, thu được dung dịch X và 2,688 lít khí H2 (đktc). Dung dịch Y gồm HCl và H2SO4, tỉ lệ mol tương ứng là 4 : 1. Trung hoà dung dịch X bởi dung dịch Y, tổng khối lượng các muối được tạo ra là
A. 13,70 gam. B. 18,46 gam.
C. 12,78 gam. D. 14,62 gam.
Lời giải:
nH2 = 0,12 mol; nOH- = 0,24 mol
Để trung hòa dd X thì dung dịch Y cần dùng với số mol H+ là 0,24 mol
Gọi số mol của H2SO4 là x thì số mol của HCl là 4x
2x + 4x = 0,24 nên x = 0,04;
Khối lượng muối = khối lượng kim loại + khối lượng gốc axi = 8,94 + 0,04.96 + 0,16.35,5 = 18,46 g
→ Đáp án B
Câu 59. Nhận biết Al, Mg, Al2O3 dùng:
A. Dung dịch HCl.
B. Dung dịch HNO3.
C. Dung dịch CuCl2.
D. Dung dịch NaOH.
Lời giải:
Lần lượt cho NaOH vào các mẫu thử. Chất rắn tan có khí thoát ra là Al, tan không có khí là Al2O3, không tan là MgO.
Phương trình hóa học:
Al + NaOH + H2O → NaAlO2 + 3/2 H2
Al2O3 + 2NaOH → NaAlO2 + H2O
→ Đáp án D
Câu 60. Hòa tan hoàn toàn a gam bột Al vào dung dịch HNO3 dư thu được 8,96 lít (đktc) gồm hỗn hợp hai khí NO và N2O có tỉ lệ số mol là 1 : 3. Giá trị của a là:
A. 32,4 B. 24,3
C. 15,3 D. 29,7
Lời giải:
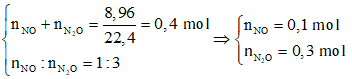
-BT e→ 3nAl = 3nNO + 8nN2O = 2,7 mol ⇒ nAl = 0,9 mol → a = 24,3g
→ Đáp án B
Câu 61. Hòa tan hết 0,81 gam bột nhôm vào 550ml dung dịch HCl 0,2M thu được dung dịch A. Tính thể tích dung dịch NaOH 0,5M cần thêm vào dung dịch A để thu được lượng kết tủa lớn nhất.
A. 0,22l B. 0.2l
C. 0,15l D. 0,12l
Lời giải:
Số mol Al = 0,81/27 = 0,03 (mol); số mol HCl = 0,55.0,2 = 0,11 (mol)
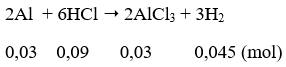
Dung dịch A thu được gồm AlCl3 = 0,03 mol; HCl = 0,11 - 0,09 = 0,02 mol.
Để có lượng kết tủa lớn nhất:
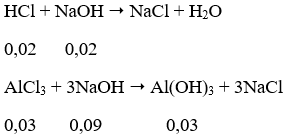
Thể tích dung dịch NaOH cần dùng = (0,02+0,09)/0,5 = 0,22 (lít)
→ Đáp án A
Câu 62. Hấp thụ hoàn toàn 0,672lit khí CO2 (đktc) vào 1 lít dd gồm NaOH 0,025M và Ca(OH)2 0,0125M, thu được x gam kết tủa. Giá trị của x là :
A. 2,00 B. 0,75
C. 1,25 D. 1,00
Lời giải:
nOH- = nNaOH + 2nCa(OH)2 = 0,05 mol
nCO2 = 0,672/22,4 = 0,03 mol
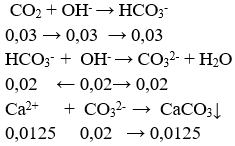
⇒ x = 0,0125.100 = 1,25 g
→ Đáp án C
Câu 63. Hòa tan hoàn toàn 14,58 gam Al trong dung dịch HNO3 loãng, đun nóng thì có 2,0 mol HNO3, đã phản ứng, đồng thời có V lít khí N2 thoát ra (đktc). Giá trị của V là
A. 2,24 B. 2,80
C. 1,12 D. 1,68
Lời giải:
+ Đặt nNH4NO3 = a, nN2 = b
⇒ 10nNH4NO3 + 8nN2 = 3nAl = 1,62 (1)
⇒ 12nNH4NO3 + 10nN2 = nHNO3 = 2 (2)
+ Giải hệ (1) và (2) ⇒ b = nN2 = 0,05 mol
⇒ VN2 = 1,12 lít
→ Đáp án C
Câu 64. Cho dung dịch chứa a mol Ca(HCO3)2 tác dụng với dung dịch chứa a mol chất tan X. Để thu được lượng kết tủa lớn nhất thì X là
A. Ba(OH)2. B. Ca(OH)2.
C. NaOH. D. Na2CO3.
Lời giải:
Lượng kết tủa thu được lớn nhất khi:
- X chứa cation cũng tạo được kết tủa với .
- Cation có nguyên tử khối lớn nhất.
Kết hợp hai điều kiện trên chọn được chất X phù hợp là Ba(OH)2.
Ca(HCO3)2 + Ba(OH)2 → CaCO3↓ + 2H2O + BaCO3↓
→ Đáp án A
Câu 65. Cho các dung dịch: HNO3, NaCl, Na2SO4, Ca(OH)2, KHSO4, Mg(NO3)2. Số dung dịch tác dụng được với dung dịch NaHCO3 là:
A. 3. B. 1.
C. 2. D. 4.
Lời giải:
Có 3 dung dịch tác dụng được với dung dịch NaHCO3: HNO3, Ca(OH)2, KHSO4.
HNO3 + NaHCO3 → NaNO3 + H2CO3
Ca(OH)2 + 2NaHCO3 → CaCO3 + 2H2O + Na2CO3
2NaHCO3 + 2KHSO4 → 2H2O + Na2SO4 + K2SO4 + 2CO2
→ Đáp án A
Câu 66. Hỗn hợp X gồm Ba, BaO và Ba(OH)2 có tỉ lệ số mol tương ứng 1: 2 : 3. Cho m gam X vào nước thì thu được a lít dung dịch Y và V lít khí H2 (đktc). Hấp thụ 8V lít CO2 (đktc) vào a lít dung dịch Y đến phản ứng xảy ra hoàn toàn thì thu được 98,5 gam kết tủa. Giá trị của m là
A. 105,16. B. 119,50.
C. 95,60. D. 114,72.
Lời giải:
Đặt nBa = a, nBaO = 2a và nBa(OH)2 = 3a
⇒ nH2 = nBa = a ⇒ ∑nBa(OH)2 = a + 2a 3a = 6a = 6V/22,4
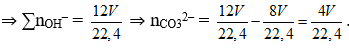
⇒ nBaCO3 = (4V/22,4) x 197 = 98,5 → V = 2,8.
⇒ nBa = 2,8/22,4 = 0,125 mol ⇒ nBaO = 0,25, nBa(OH)2 = 0,375.
⇒ m = 0,125 x 137 + 0,25 x 153 + 0,375 x 171 = 119,5 gam
→ Đáp án B
Câu 67. Đốt nóng hỗn hợp X gồm Fe2O3 và bột Al trong môi trường không có không khí. Nếu cho những chất còn lại sau phản ứng tác dụng với dung dịch NaOH dư sẽ thu được 0,3 mol H2; còn nếu cho tác dụng với dung dịch HCl dư thu được 0,4 mol H2. Vậy số mol Al trong hỗn hợp X là:
A. 0,3 B. 0,4
C. 0,25 D. 0,6
Lời giải:
Khi cho Al phản ứng với NaOH hoặc HCl thì số mol H2 thu được là như nhau:
nH2 = 0,3 mol ⇒ nAl = 0,2 mol
Từ đó suy ra nH2 do Fe tạo ra = 0,4 - 0,3 = 0,1 mol
→ nFe = 0,1 mol ⇒ nAl đã phản ứng tạo Fe là 0,1 mol vì:
Fe2O3 + 2Al (0,1) → Al2O3 + 2Fe (0,1)
→ ∑nAl trong X = 0,1 + 0,2 = 0,3mol
→ Đáp án A
Câu 68. Cho 200ml dung dịch AlCl3 1,5M tác dụng với V lít dung dịch NaOH 0,5M; lượng kết tủa thu được là 15,6 gam. Giá trị lớn nhất của V là:
A. 1,2 B. 1,8
C. 2,4 D. 2
Lời giải:
Ta có: nAlCl3 = 1,5.0,2 = 0,3 mol; nAl(OH)3 = 15,6/78 = 0,2 mol
Thể tích NaOH lớn nhất khi kết tủa sinh ra cực đại, bị NaOH hòa tan 1 phần còn 15,6 (g).
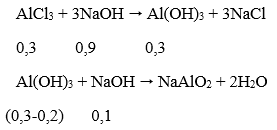
Theo phương trình phản ứng, ta có: nNaOH = 0,9 + 0,1 = 1 mol
⇒ VNaOH = 1/0,5 = 2 lít
→ Đáp án D
Câu 69. Cho 19,02 gam hỗn hợp Mg, Ca, MgO, CaO, MgCO3, CaCO3 tác dụng vừa đủ với m gam dung dịch HCl 10% thu được 4,704 lít hỗn hợp khí X (đktc). Biết khối lượng hỗn hợp khí X là 5,25 gam và dung dịch sau phản ứng chứa 19,98 gam CaCl2. Giá trị của m gần giá trị nào nhất sau đây?
A. 229,95. B. 153,30.
C. 237,25. D. 232,25.
Lời giải:
X gồm H2 và CO2. Đặt nCO2 = x; nH2 = y ⇒ nX = x + y = 0,21 mol;
mX = 5,25g = 44x + 2y.
Giải hệ có: x = 0,115 mol; y = 0,095 mol.
Quy đổi hỗn hợp ban đầu về Mg, Ca, O và CO2
⇒ nCa = nCaCl2 = 0,18 mol.
Đặt nMg = x; nO = y ⇒ 24x + 0,18 x 40 + 16y + 0,115 x 44 = 19,02g
Bảo toàn electron: 2x + 0,18 × 2 = 0,095 × 2 + 2y.
Giải hệ có: x = 0,135 mol; y = 0,22 mol.
⇒ nHCl = 2nMg + 2nCa = 2 x 0,135 + 2 x 0,18 = 0,63 mol
⇒ m = 0,63 x 36,5 : 0,1 = 229,95(g).
→ Đáp án A
Câu 70. Hấp thụ hoàn toàn 4,48 lít CO2 ở (đktc) vào 500 ml dung dịch hỗn hợp gồm NaOH 0,1M và Ba(OH)2 0,2M, sinh ra m gam kết tủa. Giá trị của m là:
A. 19,70 B. 17,73
C. 9,85 D. 11,82
Lời giải:
Ta có: nCO2 = 4,48/22,4 = 0,2 mol
nNaOH = 0,5.0,1 = 0,05 mol
nBa(OH)2 = 0,2.0,5 = 0,1 mol
nOH- = 0,1.2 + 0,05 = 0,25 mol
nBa2+ = 0,1 mol
Ta thấy:
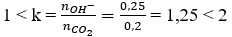
→ tạo ra 2 ion CO32- và HCO3-
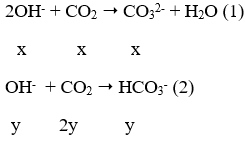
Ta có hệ phương trình:
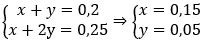
Ba2+ + CO32- → BaCO3↓
⇒ mBaCO3 = 0,05.197 = 9,85 g
→ Đáp án C
Thi online Hóa 12 KNTTThi online Hóa 12 CDThi online Hóa 12 CTST
Xem thêm các dạng bài tập Hóa học lớp 12 ôn thi Tốt nghiệp có lời giải hay khác:
- 100 câu trắc nghiệm Kim loại kiềm, Kim loại kiềm thổ, Nhôm có lời giải (cơ bản – phần 1)
- 100 câu trắc nghiệm Kim loại kiềm, Kim loại kiềm thổ, Nhôm có lời giải (cơ bản – phần 2)
- 100 câu trắc nghiệm Kim loại kiềm, Kim loại kiềm thổ, Nhôm có lời giải (cơ bản – phần 3)
- 100 câu trắc nghiệm Kim loại kiềm, Kim loại kiềm thổ, Nhôm có lời giải (nâng cao – phần 1)
- 100 câu trắc nghiệm Kim loại kiềm, Kim loại kiềm thổ, Nhôm có lời giải (nâng cao – phần 3)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Lớp 12 Kết nối tri thức
- Soạn văn 12 (hay nhất) - KNTT
- Soạn văn 12 (ngắn nhất) - KNTT
- Giải sgk Toán 12 - KNTT
- Giải sgk Vật Lí 12 - KNTT
- Giải sgk Hóa học 12 - KNTT
- Giải sgk Sinh học 12 - KNTT
- Giải sgk Lịch Sử 12 - KNTT
- Giải sgk Địa Lí 12 - KNTT
- Giải sgk Giáo dục KTPL 12 - KNTT
- Giải sgk Tin học 12 - KNTT
- Giải sgk Công nghệ 12 - KNTT
- Giải sgk Hoạt động trải nghiệm 12 - KNTT
- Giải sgk Giáo dục quốc phòng 12 - KNTT
- Giải sgk Âm nhạc 12 - KNTT
- Giải sgk Mĩ thuật 12 - KNTT
- Lớp 12 Chân trời sáng tạo
- Soạn văn 12 (hay nhất) - CTST
- Soạn văn 12 (ngắn nhất) - CTST
- Giải sgk Toán 12 - CTST
- Giải sgk Vật Lí 12 - CTST
- Giải sgk Hóa học 12 - CTST
- Giải sgk Sinh học 12 - CTST
- Giải sgk Lịch Sử 12 - CTST
- Giải sgk Địa Lí 12 - CTST
- Giải sgk Giáo dục KTPL 12 - CTST
- Giải sgk Tin học 12 - CTST
- Giải sgk Hoạt động trải nghiệm 12 - CTST
- Giải sgk Âm nhạc 12 - CTST
- Lớp 12 Cánh diều
- Soạn văn 12 Cánh diều (hay nhất)
- Soạn văn 12 Cánh diều (ngắn nhất)
- Giải sgk Toán 12 Cánh diều
- Giải sgk Vật Lí 12 - Cánh diều
- Giải sgk Hóa học 12 - Cánh diều
- Giải sgk Sinh học 12 - Cánh diều
- Giải sgk Lịch Sử 12 - Cánh diều
- Giải sgk Địa Lí 12 - Cánh diều
- Giải sgk Giáo dục KTPL 12 - Cánh diều
- Giải sgk Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 - Cánh diều
- Giải sgk Giáo dục quốc phòng 12 - Cánh diều
- Giải sgk Âm nhạc 12 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

