Bài tập Tách, tinh chế kim loại và hợp chất của kim loại (chọn lọc, có đáp án)
Bài viết Tách, tinh chế kim loại và hợp chất của kim loại với phương pháp giải chi tiết giúp học sinh ôn tập, biết cách làm bài tập Tách, tinh chế kim loại và hợp chất của kim loại.
Bài tập Tách, tinh chế kim loại và hợp chất của kim loại (chọn lọc, có đáp án)
Thi online KHTN 9 KNTTThi online KHTN 9 CDThi online KHTN 9 CTST
Bài 1: Quặng nhôm có Al2O3 lẫn với các tạp chất là Fe2O3 và SiO2. Hãy nêu phản ứng nhằm tách riêng từng oxit ra khỏi quặng nhôm.
Bài 2: Một hỗn hợp gồm Al, Fe, Cu và Ag. Bằng phương pháp hóa học hãy tách rời hoàn toàn các kim loại ra khỏi hỗn hợp trên.
Bài 3: Hỗn hợp gồm FeCl2, NaCl, AlCl3, CuCl2. Tách riêng lấy từng chất?
Bài 4: Tách riêng mỗi chất ra khỏi hỗn hợp sau:
a) Hỗn hợp Al2O3, CuO, FeS, K2SO4
b) Hỗn hợp AlCl3, FeCl3, BaCl2
c) Hỗn hợp Cu, Ag, S, Fe
Đáp án và hướng dẫn giải
Bài 1:
- Hòa tan hỗn hợp oxit bằng dung dịch kiềm, Al2O3 và SiO2 tan:
Al2O3 + 2NaOH → 2NaAlO2 + H2O
SiO2 + 2NaOH → Na2SiO3 + H2O
+ Lọc thu được Fe2O3 không tan.
- Sục CO2 dư vào nước lọc để tách được kết tủa Al(OH)3
NaAlO2 + CO2 + 2H2O → Al(OH)3 + NaHCO3
- Lọc kết tủa đem nung nóng thu được Al2O3.
Al(OH)3 → Al2O3 + 3H2O
- Dùng HCl tác dụng với nước lọc để tạo kết tủa H2SiO3.
2HCl + Na2SiO3 → 2NaCl + H2SiO3
- Lọc kết tủa nung nóng H2SiO3 thu được SiO2
H2SiO3 → SiO2 + H2O
Bài 2:
Cho hỗn hợp 4 kim loại tác dụng với HCl thu được dung dịch FeCl2, AlCl3 và kết tủa không tan Cu, Ag.
- Cho 2 dung dịch FeCl2, AlCl3 tác dụng với NaOH dư, thu được kết tủa Fe(OH)2 và dung dịch NaCl, NaAlO2, NaOH dư.
+ Lọc kết tủa Fe(OH)2 tái tạo thành FeCl2, điện phân dung dịch được Fe.
+ Sục khí CO2 dư vào dung dịch NaCl, NaAlO2, NaOH dư thu được kết tủa Al(OH)3, tái tạo thành AlCl3, điện phân nóng chảy thu được Al.
- Cho 2 kết tủa không tan Cu, Ag tác dụng với HCl có sục khí O2, Cu tan thành CuCl2 trong dung dịch, Ag không tan.
+ Lọc kết tủa Ag.
+ Điện phân dung dịch CuCl2 thu được Cu.
Bài 3:
Cho hh vào dd NaOH dư
+ Có kết tủa lọc tách : Cu(OH)2 và Fe(OH)2 (nhóm 1)
+ dd : NaCl, NaAlO2, NaOH dư (nhóm 2)
Nhóm 1: cho td dd HCl dư, bay hơi HCl thu đc 2 muối khan cho vào nước, đpdd được : Cu, Fe; cho Cu, Fe tác dụng với dd HCl dư thu đc FeCl2 và Cu. Lọc kết tủa, cho Cu tác dụng với Cl2 thu được CuCl2.
Nhóm 2: cho tác dụng với CO2 dư, lọc tách kết tủa thu được:
+ Al(OH)3: Cho Al(OH)3 tác dụng với HCl → AlCl3
+ NaCl, NaHCO3: nung được NaCl khan và Na2CO3, cho hỗn hợp rắn vào nước sau đó cho tác dụng CaCl2 dư thu được NaCl và kết tủa CaCO3, lọc kết tủa thu đc NaCl.
Bài 4:
a)
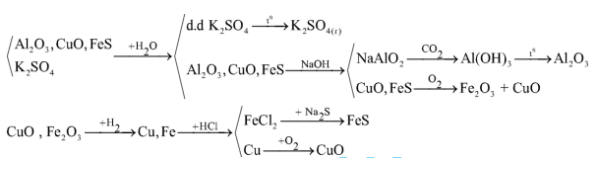
b) Cho hỗn hợp tác dụng với dung dịch NH3 dư → dung dịch và 2 kết tủa.
Từ dung dịch (BaCl2 và NH4Cl) điều chế được BaCl2 bằng cách cô cạn và đun nóng (NH4Cl thăng hoa).
(Hoặc dùng Na2CO3 và HCl để thu được BaCl2)
Hòa tan 2 kết tủa Fe(OH)3 và Al(OH)3 vào NaOH dư → thu được 1 dung dịch và 1 kết tủa.
Từ dung dịch tái tạo AlCl3
NaAlO2 → Al(OH)3 →Al2O3 → AlCl3.
Từ kết tủa tái tạo FeCl3
Fe(OH)3 → FeCl3
c)
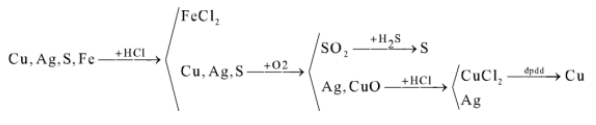
Thi online KHTN 9 KNTTThi online KHTN 9 CDThi online KHTN 9 CTST
Xem thêm các dạng bài tập Hóa học lớp 9 có đáp án, hay khác:
Xem thêm các loạt bài Để học tốt Hóa học 9 hay khác:
- Giải bài tập Hóa học 9
- Giải sách bài tập Hóa 9
- Đề thi Hóa học 9
- Wiki 200 Tính chất hóa học
- Wiki 3000 Phản ứng hóa học quan trọng
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Chuyên đề: Lý thuyết - Bài tập Hóa học lớp 9 có đáp án được biên soạn bám sát nội dung chương trình sgk Hóa học 9.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 9 Global Success
- Giải sgk Tiếng Anh 9 Smart World
- Giải sgk Tiếng Anh 9 Friends plus
- Lớp 9 Kết nối tri thức
- Soạn văn 9 (hay nhất) - KNTT
- Soạn văn 9 (ngắn nhất) - KNTT
- Giải sgk Toán 9 - KNTT
- Giải sgk Khoa học tự nhiên 9 - KNTT
- Giải sgk Lịch Sử 9 - KNTT
- Giải sgk Địa Lí 9 - KNTT
- Giải sgk Giáo dục công dân 9 - KNTT
- Giải sgk Tin học 9 - KNTT
- Giải sgk Công nghệ 9 - KNTT
- Giải sgk Hoạt động trải nghiệm 9 - KNTT
- Giải sgk Âm nhạc 9 - KNTT
- Giải sgk Mĩ thuật 9 - KNTT
- Lớp 9 Chân trời sáng tạo
- Soạn văn 9 (hay nhất) - CTST
- Soạn văn 9 (ngắn nhất) - CTST
- Giải sgk Toán 9 - CTST
- Giải sgk Khoa học tự nhiên 9 - CTST
- Giải sgk Lịch Sử 9 - CTST
- Giải sgk Địa Lí 9 - CTST
- Giải sgk Giáo dục công dân 9 - CTST
- Giải sgk Tin học 9 - CTST
- Giải sgk Công nghệ 9 - CTST
- Giải sgk Hoạt động trải nghiệm 9 - CTST
- Giải sgk Âm nhạc 9 - CTST
- Giải sgk Mĩ thuật 9 - CTST
- Lớp 9 Cánh diều
- Soạn văn 9 Cánh diều (hay nhất)
- Soạn văn 9 Cánh diều (ngắn nhất)
- Giải sgk Toán 9 - Cánh diều
- Giải sgk Khoa học tự nhiên 9 - Cánh diều
- Giải sgk Lịch Sử 9 - Cánh diều
- Giải sgk Địa Lí 9 - Cánh diều
- Giải sgk Giáo dục công dân 9 - Cánh diều
- Giải sgk Tin học 9 - Cánh diều
- Giải sgk Công nghệ 9 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 9 - Cánh diều
- Giải sgk Âm nhạc 9 - Cánh diều
- Giải sgk Mĩ thuật 9 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

