Cách nhận biết carbonic acid (H2CO3) nhanh nhất
Carbonic acid là một hợp chất chứa cacbon có công thức hóa học là H2CO3. Dung dịch CO2 trong nước chứa một lượng nhỏ hợp chất này. Cách nhận biết dung dịch axit này như thế nào? Bài viết bên dưới sẽ giúp các em có câu trả lời.
Cách nhận biết carbonic acid (H2CO3)
I. Cách nhận biết carbonic acid
Carbonic acid là một axit yếu, không phân li hoàn toàn trong nước:
H2CO3 ⇄ H+ +HCO3-
carbonic acid cũng không bền, dễ bị phân hủy:
H2CO3 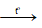 CO2↑ + H2O
CO2↑ + H2O
- Cách nhận biết: Dùng quỳ tím
- Hiện tượng: Quỳ tím hóa đỏ nhạt
Ngoài ra, chúng ta có thể dùng dung dịch Ca(OH)2 hoặc Ba(OH)2 dư để nhận biết.
+ Hiện tượng: Xuất hiện kết tủa màu trắng
+ Phương trình hóa học:
H2CO3 + Ba(OH)2 → BaCO3↓ + 2H2O
H2CO3 + Ca(OH)2 → CaCO3↓ + 2H2O
II. Bài tập nhận biết carbonic acid
Bài 1: Chỉ dùng dung dịch Ba(OH)2 thì phân biệt được bao nhiêu dung dịch trong dãy sau: H2CO3, Na2SO4, HCl, Na2CO3?
Hướng dẫn giải:
- Khi nhỏ Ba(OH)2 vào các mẫu thử, hiện tượng:
+ Xuất hiện kết tủa trắng: H2CO3, Na2SO4, Na2CO3 (nhóm I)
H2CO3 + Ba(OH)2 → BaCO3↓ + 2H2O
Na2SO4 + Ba(OH)2 → BaSO4↓ + 2NaOH
Na2CO3 + Ba(OH)2 → BaCO3↓ + 2NaOH
+ Không hiện tượng: HCl
- Dùng HCl đã nhận biết nhỏ vào các kết tủa tương ứng của các chất nhóm I:
+ Kết tủa tan và có khí thoát ra: BaCO3 hay chất ban đầu là H2CO3 hoặc Na2CO3
BaCO3 + 2HCl → BaCl2 + CO2↑ + H2O
+ Kết tủa không tan: BaSO4 hay chất ban đầu là Na2SO4.
- Dùng HCl đã nhận biết nhỏ vào các mẫu thử còn lại (H2CO3 hoặc Na2CO3)
+ Có khí không màu thoát ra: Na2CO3
Na2CO3 + 2HCl → 2NaCl + CO2↑ + H2O
+ Không hiện tượng: H2CO3.
→ Phân biệt được cả 4 dung dịch.
Bài 2: Nêu hiện tượng khí nhúng từng mẩu quỳ tím vào từng dung dịch sau: Na2SO4, HCl, H2SO4, BaCl2, Ba(OH)2, Na2CO3, NaOH, H2CO3.
Hướng dẫn giải:
- Quỳ tím chuyển sang màu đỏ: HCl, H2SO4, H2CO3 (đỏ nhạt).
- Quỳ tím chuyển sang màu xanh: Ba(OH)2, Na2CO3, NaOH.
- Quỳ tím không đổi màu: Na2SO4 và BaCl2.
Xem thêm cách nhận biết các chất hóa học nhanh, chi tiết khác:
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)








 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



