Cách nhận biết FeO nhanh nhất
iron (II) oxide có công thức hóa học là FeO. FeO là một basic oxide. Bài viết sau đây, cung cấp cho các em cách nhận biết oxit này trong dạng bài tập nhận biết. Các em hãy đọc ngay để nắm được cách nhận biết nhé.
Cách nhận biết FeO
I. Cách nhận biết FeO
- Đặc điểm: FeO là chất rắn, màu đen và không tan trong nước.

- Cách nhận biết: Hòa tan FeO trong HCl.
- Hiện tượng: Chất rắn màu đen tan ra, dung dịch có màu lục nhạt.
- Phương trình hóa học:
FeO + 2HCl → FeCl2 + H2O
Ngoài ra, khi cho FeO tác dụng với H2SO4 đặc, HNO3 thì sinh ra khí:
2FeO + 4H2SO4đặc → Fe2(SO4)3 + SO2 ↑ + 4H2O
3FeO + 10HNO3 → 3Fe(NO3)3 + NO ↑ + 5H2O
II. Mở rộng
FeO là hợp chất không có trong tự nhiên và có thể điều chế bằng cách dùng H2 hay CO khử Fe2O3 ở 500 °C :
Fe2O3 + CO 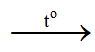 2FeO + CO2↑
2FeO + CO2↑
III. Bài tập nhận biết FeO
Bài 1: Phân biệt hai chất rắn màu đen sau: FeO và CuS? Viết phương trình hóa học minh họa.
Hướng dẫn giải:
- Phân biệt hai chất rắn FeO và CuS bằng dung dịch axit HCl, hiện tượng thu được:
+ Chất rắn màu đen tan ra: FeO
FeO + 2HCl → FeCl2 + H2O
+ Chất rắn không tan: CuS.
Bài 2: Chỉ dùng một thuốc thử, hãy phân biệt 4 gói chất rắn có màu tương tự nhau sau: FeO, CuO, MnO2 và hỗn hợp (Fe + FeO)? Viết phương trình hóa học minh họa.
Hướng dẫn giải:
- Lấy mẫu thử và đánh số thứ tự tương ứng.
- Nhỏ thêm dung dịch HCl vào các mẫu thử, đun nóng hiện tượng:
+ Chất rắn tan ra, có khí màu vàng lục thoát ra: MnO2
MnO2 + 4HCl 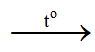 MnCl2 + Cl2↑ + 2H2O
MnCl2 + Cl2↑ + 2H2O
+ Chất rắn tan ra, có khí không màu thoát ra, dung dịch có màu xanh lục: hỗn hợp Fe + FeO
Fe + 2HCl → FeCl2 + H2↑
FeO + 2HCl → FeCl2 + H2O
+ Chất rắn tan ra, dung dịch có màu lục nhạt, không có khí thoát ra: FeO
FeO + 2HCl → FeCl2 + H2O
+ Chất rắn tan ra, dung dịch có màu xanh đậm hơn: CuO
CuO + 2HCl → CuCl2 + H2O
Xem thêm cách nhận biết các chất hóa học nhanh, chi tiết khác:
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)








 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



