HCHO + AgNO3 + NH3 + H2O → Ag + NH4NO3 + (NH4)2CO3 | HCHO ra Ag
Phản ứng HCHO + AgNO3 + NH3 + H2O ra Ag (formic aldehyde + AgNO3) thuộc loại phản ứng oxi hóa khử đã được cân bằng chính xác và chi tiết nhất. Bên cạnh đó là một số bài tập có liên quan về HCHO có lời giải, mời các bạn đón xem:
HCHO + 4AgNO3 + 6NH3 + 2H2O 4Ag ↓+ 4NH4NO3 + (NH4)2CO3
1. Phương trình phản ứng tráng gương của HCHO
HCHO + 4AgNO3 + 6NH3 + 2H2O → 4Ag + 4NH4NO3 + (NH4)2CO3
2. Cách tiến hành phản ứng tráng gương của HCHO
Cho vào ống nghiệm 1 mL dung dịch AgNO3 1%, sau đó thêm dần từng giọt dung dịch NH3, đồng thời lắc đều đến khi thu được dung dịch trong suốt thì dừng lại. Thêm tiếp vài giọt dung dịch formic aldehyde, đun nhẹ trong vài phút ở 60oC đến 70oC.
3. Hiện tượng phản ứng tráng gương của HCHO
Trên thành ống nghiệm thấy có một lớp bạc kim loại màu sáng.
4. Cân bằng phản ứng theo phương pháp thăng bằng electron
Ta có các quá trình:
Phương trình hoá học:
HCHO + 4AgNO3 + 6NH3 + 2H2O → 4Ag + 4NH4NO3 + (NH4)2CO3
5. Mở rộng kiến thức về andehit
5.1. Định nghĩa, phân loại, danh pháp
a. Định nghĩa
- Anđehit là những hợp chất hữu cơ mà phân tử có nhóm – CH = O (hay – CHO) liên kết trực tiếp với nguyên tử cacbon hoặc nguyên tử hiđro.
- Nhóm chức – CHO là nhóm chức anđehit.
- Ví dụ:
HCHO; CH3CHO; OHC – CHO…
b. Phân loại
- Dựa theo đặc điểm cấu tạo của gốc hydrocarbon, anđehit được chia thành:
+ Anđehit no;
+ Anđehit không no;
+ Anđehit thơm.
- Dựa theo số nhóm -CHO trong phân tử, anđehit được chia thành:
+ Anđehit đơn chức
+ Anđehit đa chức
Chú ý:
Anđehit no, mạch hở, đơn chức có công thức cấu tạo thu gọn CxH2x+1CHO (x ≥ 0) hay công thức phân tử chung CnH2nO (n ≥ 1).
c. Danh pháp
Tên thông thường
- Một số anđehit có tên thông thường.
- Tên thông thường = anđehit + tên axit tương ứng
- Ví dụ:
HCHO: formic aldehyde
CH3CHO: aldehyde acetic
Tên thay thế của các anđehit no, đơn chức, mạch hở:
- Chọn mạch chính của phân tử anđehit là mạch cacbon dài nhất có chứa nhóm -CHO.
- Đánh số thứ tự C trên mạch chính, bắt đầu từ nhóm – CHO.
- Tên thay thế = tên hydrocarbon tương ứng với mạch chính + al
- Ví dụ:
6.2. Đặc điểm cấu tạo và tính chất vật lý
a. Đặc điểm cấu tạo
Trong nhóm – CHO, liên kết đôi C = O gồm một liên kết σ bền và một liên kết π kém bền hơn, tương tự liên kết C = C trong phân tử alkene, do đó anđehit có một số tính chất giống alkene.
b. Tính chất vật lý
- Ở điều kiện thường, các anđehit đầu dãy đồng đẳng là chất khí và tan tốt trong nước. Các anđehit tiếp theo là chất lỏng hoặc rắn.
- Độ tan trong nước của các anđehit giảm dần theo chiều tăng của phân tử khối.
6.3. Tính chất hóa học
a. Phản ứng cộng hiđro
Ví dụ:
CH3 – CH = O + H2 CH3 – CH2 – OH
Phản ứng tổng quát:
RCHO + H2 RCH2OH
⇒ Trong phản ứng này anđehit đóng vai trò là chất oxi hóa.
b. Phản ứng oxi hóa không hoàn toàn
- Phản ứng tráng gương
Ví dụ:
CH3CHO + 2AgNO3 + H2O + 3NH3 CH3COONH4 + 2NH4NO3 + 2Ag↓
Phản ứng tổng quát:
RCHO + 2AgNO3 + H2O + 3NH3 RCOONH4 + 2NH4NO3 + 2Ag↓
- Phản ứng tạo thành axit
2RCHO + O2 2RCOOH
⇒ Trong các phản ứng trên anđehit đóng vai trò là chất khử.
c. Phản ứng oxi hóa hoàn toàn
Phản ứng tổng quát khi đốt cháy hoàn toàn anđehit no, đơn chức, mạch hở:
CnH2nO + O2 nCO2 + nH2O
6.4: Điều chế
a. Từ ancol
Oxi hóa ancol bậc I, được anđehit tương ứng:
RCH2OH + CuO RCHO + Cu + H2O
b. Từ hydrocarbon?/span>
- Oxi hóa methane có xúc tác thu được formic aldehyde
CH4 + O2 HCHO + H2O
- Oxi hóa không hoàn toàn etilen là phương pháp hiện đại để sản xuất aldehyde acetic
2CH2= CH2 + O2 2CH3CHO
6.5: Ứng dụng
- Fomanđehit được dùng làm nguyên liệu sản xuất nhựa phenol – fomanđehit và nhựa ure – fomanđehit.
- Dung dịch nước của fomanđehit được dùng làm chất tẩy uế, ngâm mẫu động vật làm tiêu bản …
- aldehyde acetic được dùng làm nguyên liệu sản xuất acetic acid.
- Nhiều anđehit có nguồn gốc thiên nhiên được dùng làm hương liệu cho công nghiệp thực phẩm, mĩ phẩm …
7. Bài tập vận dụng liên quan
Câu 1: Đốt cháy hoàn toàn một lượng anđehit A cần vừa đủ 2,52 lít O2 (đktc), được 4,4 gam CO2 và 1,35 gam H2O. A có công thức phân tử là
A. C3H4O.
B. C4H6O.
C. C4H6O2.
D. C8H12O
Hướng dẫn giải:
Đáp án C
nO2 = 0,1125 mol; nCO2 = 0,1 mol; nH2O = 0,075 mol;
BTNT "C": nC(A) = nCO2 = 0,1 mol
BTNT "H": nH(A) = 2nH2O = 0,15 mol
BTNT "O": nO(A) + 2nO2 = 2nCO2 + nH2O
=> nO(A) + 2.0,1125 = 2.0,1 + 0,075 => nO(A) = 0,05 mol
=> nC : nH : nO = 0,1 : 0,15 : 0,05 = 2 : 3 : 1
=> A có công thức đơn giản nhất là C2H3O.
Vậy đáp án C thỏa mãn.
Câu 2: X, Y, Z, T là 4 anđehit no hở đơn chức đồng đẳng liên tiếp, trong đó MT = 2,4MX. Đốt cháy hoàn toàn 0,1 mol Z rồi hấp thụ hết sản phẩm cháy vào bình đựng dung dịch Ca(OH)2 dư thấy khối lượng dung dịch tăng hay giảm bao nhiêu gam?
A. Tăng 18,6 gam.
B. Tăng 13,2 gam.
C. Giảm 11,4 gam.
D. Giảm 30 gam.
Hướng dẫn giải:
Đáp án C
Ta có: MT = MX + 3.M-CH2- = MX + 3.14
Mà MT = 2,4MX MX = 30 (HCHO)
Vậy Z là CH3CH2CHO
Đốt 0,1 mol Z => nCO2 = nH2O = 0,3 mol = nCaCO3 (vì Ca(OH)2 dư)
=> Δm dd = mCO2 + mH2O - mCaCO3 = 0,3.(44 + 18) - 30 = -11,4 gam < 0
Vậy khối lượng của dung dịch giảm 11,4 gam
Câu 3: Đốt cháy hoàn toàn 0,1 mol hỗn hợp X gồm 2 anđehit đơn chức là đồng đẳng kế tiếp thu được 8,064 lít khí CO2 (đktc) và 4,68 gam H2O. Công thức cấu tạo của 2 anđehit là:
A. HCHO và CH3CHO
B. CH3CHO và CH3CH2CHO
C. CH2=CHCHO và CH2=CHCH2CHO
D. OHC-CH2-CH2-CHO và OHC-(CH2)3-CHO
Hướng dẫn giải:
Đáp án C
nCO2 = 0,36 mol; nH2O = 0,26 mol
Ta thấy: nCO2 - nH2O = nX nên 2 andehit đơn chức, không no có 1 nối đôi C=C.
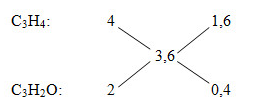
Số nguyên tử C trung bình = nCO2 : nX = 0,36 : 0,1 = 3,6
Do 2 anđehit là đồng đẳng kế tiếp do đó 2 anđehit là: CH2=CHCHO và CH2=CHCH2CHO
Câu 4: Cho hỗn hợp khí X gồm HCHO và H2 đi qua ống sứ đựng bột Ni nung nóng. Sau khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Y gồm hai chất hữu cơ. Đốt cháy hết Y thì thu được 11,7 gam H2O và 7,84 lít khí CO2 (ở đktc). Phần trăm theo thể tích của H2 trong X là
A. 35,00%.
B. 65,00%.
C. 53,85%.
D. 46,15%.
Hướng dẫn giải:
Đáp án D
Ta thấy, số mol của các nguyên tố trong X, Y là giống nhau => Khi đốt Y tương tự như đốt cháy X.
BTNT C: nCO2 = nHCHO = 0,35 mol
BTNT H: nH2O = nHCHO + nH2 = 0,65 mol
=> nH2 = 0,65 - 0,35 = 0,3 mol
=> %VH2 = (0,3/0,65).100% = 46,15%
Câu 5:Hiđro hoá hoàn toàn m gam hỗn hợp X gồm hai anđehit no, đơn chức, mạch hở, kế tiếp nhau trong dãy đồng đẳng thu được (m + 1) gam hỗn hợp hai ancol. Mặt khác, khi đốt cháy hoàn toàn cũng m gam X thì cần vừa đủ 17,92 lít khí O2 (ở đktc). Giá trị của m là
A. 10,5.
B. 8,8.
C. 24,8.
D. 17,8.
Hướng dẫn giải:
Đáp án D
*Phản ứng của anđehit và H2:
BTKL: mH2 = mancol - manđehit = 1 gam
=> nH2 = 0,5 mol = nanđehit = nancol
=> nO(X) = n anđehit = 0,5 mol
*Phản ứng đốt cháy anđehit:
Do là anđehit no, đơn chức, mạch hở nên khi đốt thì nCO2 = nH2O = x mol
BTNT "O": nO(X) + 2nO2 = 2nCO2 + nH2O hay 0,5 + 2.0,8 = 2x + x
=> x = 0,7 mol
BTKL: mX + mO2 = mCO2 +mH2O
=> mX = 0,7.44 + 0,7.18 – 0,8.32 = 17,8 gam
Câu 6: Cho hỗn hợp M gồm anđehit X (no, đơn chức, mạch hở) và hydrocarbon Y, có tổng số mol là 0,2 (số mol của X nhỏ hơn của Y). Đốt cháy hoàn toàn M, thu được 8,96 lít khí CO2 (đktc) và 7,2 gam H2O. hydrocarbon Y là
A. C3H6.
B. C2H4.
C. CH4.
D. C2H2.
Hướng dẫn giải:
Đáp án B
nCO2 = nH2O = 0,4 mol
Anđehit no, đơn chức, mạch hở nên khi đốt cho số mol CO2 bằng H2O
=> Đốt hydrocarbon cũng thu được số mol CO2 bằng H2O
=> hydrocarbon có dạng CnH2n
Mặt khác, Ctb = nCO2 : nM = 0,4 : 0,2 = 2
A. Sai vì nếu Y là C3H6 thì X là HCHO => nX = nY => Loại.
B. Đúng.
C. Sai vì không phải dạng CnH2n.
D. Sai vì không phải dạng CnH2n.
Câu 7: Cho hỗn hợp X gồm 2 anđehit đồng đẳng liên tiếp cộng H2 thu được hỗn hợp 2 rượu đơn chức. Đốt cháy hoàn toàn hỗn hợp 2 rượu này thu được 6,6 gam CO2 và 4,5 gam nước. Tìm công thức phân tử các anđehit trong X.
A. C3H4O và C4H6O.
B. C3H6O và C4H8O.
C. CH2O và C2H4O.
D. C4H6O và C5H8O.
Hướng dẫn giải:
Đáp án C
Khi đốt cháy rượu nCO2 (0,15 mol) < nH2O (0,25 mol) => Ancol no, đơn chức, hở.
=> nancol = nH2O - nCO2 = 0,1 mol
=> Ctb ancol = nCO2 : n ancol = 0,15 : 0,1 = 1,5 => Ancol là CH3OH và C2H5OH
=> X chứa HCHO và CH3CHO
Câu 8: Hỗn hợp M gồm một anđehit và một alkyne (có cùng số nguyên tử cacbon). Đốt cháy hoàn toàn x mol hỗn hợp M, thu được 3x mol CO2 và 1,8x mol H2O. Phần trăm số mol của anđehit trong hỗn hợp M là
A. 50%
B. 40%.
C. 30%.
D. 20%.
Hướng dẫn giải:
Đáp án D
- Số nguyên tử C trung bình: C tb = nCO2 : nM = 3 => alkyne là C3H4
- Số nguyên tử H trung bình: H tb = nH : nM = 2nH2O : nM = 3,6
Mà alkyne có H > 3,6 => Andehit có số H < 3,6 => có 2H => Andehit là C3H2O (CH≡C-CHO)
Áp dụng phương pháp đường chéo về số nguyên tử H trung bình ta có:
=> nC3H4 : nC3H2O = 1,6 : 0,4 = 4 : 1
Giả sử nC3H4 = 4 mol; nanđehit = 1 mol
=> %nanđehit = = 20%
Câu 9:Đốt cháy hoàn toàn 7,2 gam hợp chất hữu cơ A thu được 0,4 mol CO2 và 0,4 mol H2O. Biết A chỉ chứa một loại nhóm chức và 0,05 mol A tham gia phản ứng tráng gương thì tạo ra 0,1 mol Ag. Công thức cấu tạo thu gọn của A là
A. C3H7CHO.
B. CH3CHO.
C. C2H5CHO.
D. C2H3CHO.
Hướng dẫn giải:
Đáp án A
BTNT C, H: nC = nCO2 = 0,4 mol; nH = 2nH2O = 0,8 mol
BTKL: mO(A) = mA - mC - mH = 7,2 - 0,4.12 – 0,8 = 1,6 gam
=> nO = 0,1 mol
=> nC : nH : nO = 4 : 8 : 1. Mà nAg : nA = 2 : 1 => Phân tử A có chứa 1 nhóm -CHO
=> A có CTPT C4H8O, CTCT thu gọn là C3H7CHO
Câu 10: Hỗn hợp M gồm một anđehit và một alkyne (có cùng số nguyên tử cacbon). Đốt cháy hoàn toàn 0,2 mol hỗn hợp M, thu được 13,44 lít khí CO2 (ở đktc) và 6,48 gam H2O. Nếu cho 0,1 mol hỗn hợp M tác dụng hết với lượng dư dung dịch AgNO3 trong NH3. Số mol AgNO3 phản ứng là:
A. 0,20
B. 0,14
C. 0,12
D. 0,10
Hướng dẫn giải:
Đáp án B
nCO2 = 0,6 mol; nH2O = 0,36 mol
Số C trung bình: Ctb = nCO2 : nM = 0,6 : 0,2 = 3 => alkyne là C3H4
Số H trung bình: Htb = 2nH2O : nM = 2.0,36 : 0,2 = 3,6
=> Anđehit có số H < 3,6 (vì alkyne có H > 3,6) => Anđehit có 2H => CH≡C-CHO
Giả sử 0,1 mol hỗn hợp M chứa a mol CH≡C-CHO và b mol CH≡C-CH3
+ nH2O (đốt 0,1 mol M) = a + 2b = 0,36/2 = 0,18 (1)
+ a + b = 0,1 (2)
Giải hệ được a = 0,02 và b = 0,08
CH≡C-CHO + 3AgNO3 → Sp (Vì anđehit có 1 liên kết ba đầu mạch + 1 nhóm -CHO)
CH≡C-CH3 + AgNO3 → Sp (Vì alkyne có 1 liên kết ba đầu mạch)
=> nAgNO3 pư = 3n anđehit + n alkyne = 3.0,02 + 0,08 = 0,14 mol
Câu 11: Hai chất hữu cơ X và Y, thành phần nguyên tố đều gồm C, H, O, có cùng số nguyên tử cacbon (MX < MY). Khi đốt cháy hoàn toàn mỗi chất trong oxi dư đều thu được số mol H2O bằng số mol CO2. Cho 0,1 mol hỗn hợp gồm X và Y phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3, thu được 28,08 gam Ag. Phần trăm khối lượng của X trong hỗn hợp ban đầu là:
A. 39,66%.
B. 60,34%.
C. 21,84%.
D. 78,16%.
Hướng dẫn giải:
Đáp án C
Ta có: n hh = 0,1 mol; nAg = 0,26 mol
- Hỗn hợp có phản ứng tráng gương nên suy ra có chứa nhóm -CHO
- Mà đốt X hay đốt Y đều thu được số mol CO2 bằng số mol H2O và tỉ lệ:
nAg : nhh = 2,6
=> Hỗn hợp có chứa HCHO => Chất còn lại là HCOOH (Vì cùng số nguyên tử C)
Giả sử hỗn hợp ban đầu chứa HCHO (a mol) và HCOOH (b mol)
Giải hệ: nhh = a + b = 0,1 và nAg = 4a + 2b = 0,26 được a = 0,03 và b = 0,07
=> %mHCHO =
Câu 12: Cho hỗn hợp M gồm anđehit X (no, đơn chức, mạch hở) và hydrocarbon Y, có tổng số mol là 0,2 (số mol của X nhỏ hơn của Y). Đốt cháy hoàn toàn M, thu được 8,96 lít khí CO2 (đktc) và 7,2 gam H2O. Y có tính chất nào trong các tính chất sau đây?
A. Đốt cháy Y tạo ra số mol CO2 bé hơn số mol nước.
B. Từ Y có thể điều chế được aldehyde acetic.
C. Y có thể tác dụng với dung dịch AgNO3/NH3 tạo kết tủa vàng nhạt.
D. Y có một đồng phân cấu tạo, mạch vòng.
Hướng dẫn giải:
Đáp án B
Ta thấy: nCO2 = nH2O = 0,4 mol
Anđehit đốt cho số mol CO2 bằng số mol H2O => hydrocarbon khi đốt cũng thu được số mol CO2 bằng số mol H2O => hydrocarbon có dạng CnH2n.
Số nguyên tử C trung bình: Ctb = nCO2 : nM = 0,4 : 0,2 = 2
=> Anđehit có thể là HCHO hoặc CH3CHO
Nếu hỗn hợp chứa HCHO (a mol) và CnH2n (b mol)
+ Ta có: a + b = 0,2 và nCO2 = a + nb = 0,4 => b = 0,2/(n - 1)
Mà số mol của X nhỏ hơn Y => b > 0,1 => 0,2/(n - 1) > 0,1 => n < 3 (*)
+ Mà Ctb = 2 => n > 2 (**)
(*) (**) => 2 < n < 3 không có nghiệm => Loại
Vậy hỗn hợp chứa CH3CHO và CH2=CH2.
Xét các phương án:
A sai
B đúng: CH2=CH2 + H2O CH3CHO
C sai vì alkene không phản ứng với AgNO3.
D sai vì CH2=CH2 không có đồng phân.
Câu 13: Hỗn hợp X gồm hai anđehit no, mạch hở. Đốt cháy hoàn toàn hỗn hợp X tạo ra số mol nước đúng bằng số mol X đã phản ứng. Mặt khác khi cho 0,25 mol hỗn hợp X phản ứng hoàn toàn với lượng dư dung dịch AgNO3/NH3, thu được m gam Ag. Giá trị của m là:
A. 27 gam
B. 81 gam
C. 108 gam
D. 54 gam
Hướng dẫn giải:
Đáp án C
Giả sử công thức chung của 2 anđehit là CxHyOz.
Ta có sơ đồ: CxHyOz 0,5y H2O
Số mol của X bằng số mol H2O nên suy ra: 1 = 0,5y => y = 2
Mà anđehit có tối thiểu 2H nên suy ra 2 anđehit là HCHO và OHC-CHO.
Ta thấy: 1 mol mỗi chất phản ứng tráng gương đều thu được 4 mol Ag
=> nAg = 4nX = 4. 0,25 = 1 (mol) => mAg = 108 (g)
Câu 14: Hỗn hợp X gồm hai anđehit. Đốt cháy hoàn toàn 0,25 mol X thu được 0,3 mol CO2. Mặt khác, nếu cho 0,25 mol X tác dụng hết với dung dịch AgNO3/NH3 dư, thu được 0,9 mol Ag. Công thức cấu tạo thu gọn của hai anđehit trong X là:
A. CH3CHO và OHC-CHO.
B. HCHO và OHC-CHO.
C. HCHO và CH3-CHO.
D. HCHO và CH3-CH2-CHO.
Hướng dẫn giải:
Đáp án C
Số C trung bình: Ctb = nCO2 : nX = 0,3 : 0,25 = 1,2
=> Hỗn hợp có chứa HCHO
Ta có nAg : nX = 0,9 : 0,25 = 3,6 => Cứ 1 phân tử anđehit còn lại tráng gương được 2Ag => Anđehit đơn chức
Đặt số mol của HCHO và anđehit còn lại là a và b (mol)
Giải hệ a + b = 0,25 và nAg = 4a + 2b = 0,9 được a = 0,2 và b = 0,05
BTNT "C": nCO2 = 0,2.1 + 0,05n = 0,3 => n = 2
=> Anđehit còn lại là CH3CHO
Câu 15:Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai anđehit cần dùng vừa đủ 0,375 mol O2, thu được 0,3 mol CO2 và 0,3 mol H2O. Nếu cho m gam X tác dụng hết với lượng dư dung dịch AgNO3 trong NH3 thì khối lượng Ag thu được là:
A. 32,4 gam
B. 48,6 gam.
C. 75,6 gam.
D. 64,8 gam.
Hướng dẫn giải:
Đáp án B
BTNT "O": nO(X) = 2nCO2 + nH2O - 2nO2 = 2.0,3 + 0,3 - 2.0,375 = 0,15 mol
Ta thấy nCO2 = nH2O nên các anđehit đều no, đơn chức, mạch hở
=> nX = nO(X) = 0,15 mol
Số nguyên tử C trung bình: nCO2 : nX = 0,3 : 0,15 = 2
=> Trong hỗn hợp có chứa HCHO.
=> 2.0,15 mol < nAg < 0,15.4 mol
=> 32,4 gam < mAg < 64,8 gam
Xét các phương án thấy giá trị mAg = 48,6 gam thỏa mãn.
Xem thêm các phương trình hóa học hay khác:
- 2CH3CHO + O2 2CH3COOH
- CH3CHO + H2 C2H5OH
- CH3CHO + 2AgNO3 + 3NH3 + H2O CH3COONH4 + 2NH4NO3 + 2Ag↓
- HCHO + Br2 + H2O → HCOOH + 2HBr
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)

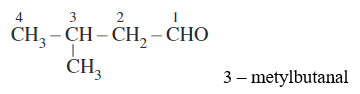







 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



