Tính chất của Photpho, phosphoric acid, Muối photphonat (chi tiết nhất)
Bài viết Tính chất của Photpho, phosphoric acid, Muối photphonat chi tiết nhất giúp học sinh nắm vững kiến thức trọng tâm Hóa học 11.
Tính chất của Photpho, phosphoric acid, Muối photphonat (chi tiết nhất)
(199k) Xem Khóa học Hóa 11 KNTTXem Khóa học Hóa 11 CDXem Khóa học Hóa 11 CTST
I. Photpho
1. Tính chất hóa học
a) Tính oxi hoá: tác dụng với một số kim loại hoạt động, tạo ra photphua kim loại.
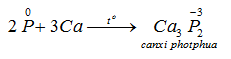
b) Tính khử: tác dụng với các phi kim hoạt động như oxi, halozen, lưu huỳnh ... cũng như với các chất oxi hóa mạnh khác
→ Tác dụng với oxi: Khi đốt nóng, photpho cháy trong không khí tạo ra các oxit của photpho :
Thiếu oxi :
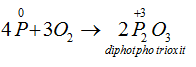
Dư Oxi :
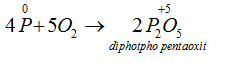
→ Tác dụng với clo: Khi cho clo đi qua P nóng chảy, sẽ thu được các hợp chất photpho clorua:
Thiếu clo :
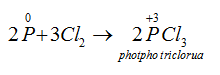
Dư clo :
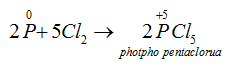
→ Tác dụng với hợp chất:
6P + 5KClO3 → 3P2O5 + 5KCl
2. Điều chế : Trong công nghiệp, photpho được sản xuất bằng cách nung hỗn hợp quặng photphorit, cát và than cốc khoảng 1200oC trong lò điện:
Ca3(PO4)2 + 3SiO2 + 5C to→ 3CaSiO3 + 2P + 5CO (3CaO. P2O5)
Hơi photpho thoát ra được ngưng tụ khi làm lạnh, thu được photpho trắng ở dạng rắn
II. Phosphoric acid
Công thức cấu tạo :
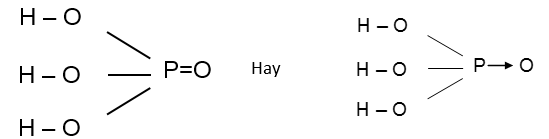
1. Tính chất vật lí: Là chất rắn dạng tinh thể trong suốt, không màu, nóng chảy ở 42,5oC. dễ chảy rữa và tan vô hạn trong nước.
2. Tính chất hóa học:
a) Tính oxi hóa – khử:
Axít photphoric khó bị khử (do P ở mức oxi hóa +5 bền hơn so với N trong nitric acid) , không có tính oxi hóa.
b) Tính axit: Axít photphoric là axit có 3 lần axit, có độ mạnh trung bình. Trong dung dịch nó phân li ra 3 nấc:
H3PO4 ⇌ H+ + H2PO4- k1 = 7, 6.10-3
H2PO4- ⇌ H+ + HPO42- k2 = 6,2.10-8 nấc 1 > nấc 2 > nấc 3
HPO42- ⇌ H+ + PO43- k3 = 4,4.10-13
→ Dung dịch axít photphoric có những tính chất chung của axit như làm quì tím hóa đỏ, tác dụng với basic oxide, bazơ, muối, kim loại.
→ Khi tác dụng với basic oxide, bazơ tùy theo lượng chất tác dụng mà axít photphoric tạo ra muối trung hòa, muối axit hoặc hỗn hợp muối:
H3PO4 + NaOH → NaH2PO4 + H2O
H3PO4 + 2NaOH → Na2HPO4 + 2H2O
H3PO4 + 3NaOH → Na3PO4 + 3H2O
3. Điều chế :
a) Trong phòng thí nghiệm: P + 5HNO3 →H3PO4 + H2O + 5NO2
b) Trong công nghiệp:
+ Cho H2SO4 đặc tác dụng với quặng photphorit hoặc quặng apatit: Ca3(PO4)2 + 3H2SO4 → 3CaSO4 + 2H3PO4
Điều chế bằng phương pháp này không tinh khiết và lượng chất thấp
+ Để điều chế H3PO4 có độ tinh khiết và nồng độ cao hơn người ta đốt cháy P để được P2O5 rồi cho P2O5 tác dụng với nước :
4P + 5O2 → 2P2O5
P2O5 + 3H2O → 2H3PO4
III. Muối photphat
Axít photphoric tạo ra 3 loại muối:
- Muối photphat trung hòa:Na3PO4, Ca3(PO4)2, ...
- Muối đihidrophotphat: NaH2PO4, Ca(H2PO4)2, ...
- Muối hidrophotphat: Na2HPO4, CaHPO4 ...
1.Tính tan: Tất cả các muối đihidrophotphat đều tan trong nước.Các muối hidrophotphat và photphat trung hòa đều không tan hoặc ít tan trong nước ( trừ muối natri, kali, amoni ).
2. Nhận biết ion photphat: Thuốc thử là silver nitrate.
3Ag+ + PO43- → Ag3PO4 ↓ (màu vàng)
(199k) Xem Khóa học Hóa 11 KNTTXem Khóa học Hóa 11 CDXem Khóa học Hóa 11 CTST
Xem thêm Chuyên đề lý thuyết và các dạng bài tập Hóa học lớp 11 hay khác:
- Nitơ là gì (cấu tạo phân tử, tính chất, điều chế)
- Tính chất của amonia và muối amoni
- Tính chất của axit nitoric và muối nitrate
- Phân bón hóa học (phân loại, điều chế)
- Hiệu suất trong tổng hợp NH3 và cách giải
- Bài tập Hiệu suất tổng hợp NH3
- Phản ứng tạo phức của NH3 và cách giải
- Bài tập Phản ứng tạo phức của NH3
- Phản ứng muối amoni
- Bài tập Phản ứng muối amoni
- Kim loại tác dụng với HNO3
- Bài tập Kim loại tác dụng với HNO3
- Oxit kim loại tác dụng với HNO3
- Bài tập Oxit kim loại tác dụng với HNO3
- Phản ứng NO3- trong môi trường bazơ
- Bài tập Phản ứng NO3- trong môi trường bazơ
- Nhiệt phân muối NO3-
- Bài tập Nhiệt phân muối NO3-
- Photpho và hợp chất của photpho
- Bài tập Photpho và hợp chất của photpho
- Nhận biết một số chất tiêu biểu của nhóm nitơ
- Bài tập Nhận biết một số chất tiêu biểu của nhóm nitơ
Xem thêm các tài liệu học tốt lớp 11 hay khác:
- Giải Chuyên đề học tập Hóa 11 Kết nối tri thức
- Giải Chuyên đề học tập Hóa 11 Chân trời sáng tạo
- Giải Chuyên đề học tập Hóa 11 Cánh diều
- Giải lớp 11 Kết nối tri thức (các môn học)
- Giải lớp 11 Chân trời sáng tạo (các môn học)
- Giải lớp 11 Cánh diều (các môn học)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 11 Global Success
- Giải sgk Tiếng Anh 11 Smart World
- Giải sgk Tiếng Anh 11 Friends Global
- Lớp 11 - Kết nối tri thức
- Soạn văn 11 (hay nhất) - KNTT
- Soạn văn 11 (ngắn nhất) - KNTT
- Giải sgk Toán 11 - KNTT
- Giải sgk Vật Lí 11 - KNTT
- Giải sgk Hóa học 11 - KNTT
- Giải sgk Sinh học 11 - KNTT
- Giải sgk Lịch Sử 11 - KNTT
- Giải sgk Địa Lí 11 - KNTT
- Giải sgk Giáo dục KTPL 11 - KNTT
- Giải sgk Tin học 11 - KNTT
- Giải sgk Công nghệ 11 - KNTT
- Giải sgk Hoạt động trải nghiệm 11 - KNTT
- Giải sgk Giáo dục quốc phòng 11 - KNTT
- Giải sgk Âm nhạc 11 - KNTT
- Lớp 11 - Chân trời sáng tạo
- Soạn văn 11 (hay nhất) - CTST
- Soạn văn 11 (ngắn nhất) - CTST
- Giải sgk Toán 11 - CTST
- Giải sgk Vật Lí 11 - CTST
- Giải sgk Hóa học 11 - CTST
- Giải sgk Sinh học 11 - CTST
- Giải sgk Lịch Sử 11 - CTST
- Giải sgk Địa Lí 11 - CTST
- Giải sgk Giáo dục KTPL 11 - CTST
- Giải sgk Hoạt động trải nghiệm 11 - CTST
- Giải sgk Âm nhạc 11 - CTST
- Lớp 11 - Cánh diều
- Soạn văn 11 Cánh diều (hay nhất)
- Soạn văn 11 Cánh diều (ngắn nhất)
- Giải sgk Toán 11 - Cánh diều
- Giải sgk Vật Lí 11 - Cánh diều
- Giải sgk Hóa học 11 - Cánh diều
- Giải sgk Sinh học 11 - Cánh diều
- Giải sgk Lịch Sử 11 - Cánh diều
- Giải sgk Địa Lí 11 - Cánh diều
- Giải sgk Giáo dục KTPL 11 - Cánh diều
- Giải sgk Tin học 11 - Cánh diều
- Giải sgk Công nghệ 11 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 11 - Cánh diều
- Giải sgk Giáo dục quốc phòng 11 - Cánh diều
- Giải sgk Âm nhạc 11 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

