Tính chất của Iot (I): Tính chất hóa học, vật lí, Điều chế, Ứng dụng chi tiết nhất
Bài viết Tính chất của Iot (I): Tính chất hóa học, vật lí, Điều chế, Ứng dụng với phương pháp giải chi tiết giúp học sinh ôn tập, biết cách làm bài tập Tính chất của Iot (I): Tính chất hóa học, vật lí, Điều chế, Ứng dụng.
Tính chất của Iot (I): Tính chất hóa học, vật lí, Điều chế, Ứng dụng chi tiết nhất
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
I. Trạng thái tự nhiên
- So với các halogen khác, iot có trong vỏ trái đất ít nhất.
- Hợp chất iot có trong nước biển nhưng rất ít.
- Iot còn có trong tuyến giáp của người tuy nhỏ nhưng rất quan trọng vì nếu thiếu sẽ bị bệnh bướu cổ.
II. Tính chất
1. Tính chất vật lý
- Iot là tinh thể màu đen tím, có vẻ sáng kim loại.
- Hiện tượng thăng hoa:
+ Đun nóng, iot không nóng chảy mà biến thành thể hơi.
+ Làm lạnh, hơi iot chuyển thành tinh thể, không thông qua thể lỏng.
- Ít tan trong nước, tan nhiều trong dung môi hữu cơ.
2. Tính chất hóa học
a. Tác dụng với kim loại
- Iot oxi hóa được nhiều kim loại nhưng chỉ xảy ra khi đun nóng hoặc có xúc tác.
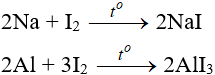
b. Tác dụng với hidro
H2 + I2 → 2HI phản ứng xảy ra thuận nghịch.
- Hidro Iotua dễ tan trong nước tạo thành dd axit Iothidric, đó là 1 axit rất mạnh, mạnh hơn cả hydrochloric acid, bromhidric.
- Iot hầu như không tác dụng với H2O.
c. Iot có tính oxi hóa kém clo và brom:
Cl2 + 2NaI → 2NaCl + I2
Br2 + 2NaI → 2NaBr + I2
d. Tính khử của axit HI
- HI có tính khử mạnh có thể khử được axit H2SO4 đặc.
8HI + H2SO4 → 4I2 + H2S + 4H2O
2HI + 2FeCl3 → FeCl2 + I2 + 2HCl
e. Tính chất đặc trưng của Iot
- Iot có tính chất đặc trưng là tác dụng với hồ tinh bột tạo thành hợp chất có màu xanh.
III. Ứng dụng, điều chế
1. Ứng dụng
- Dùng nhiều dưới dạng cồn iot (dd iot 5% trong ethyl alcohol) làm chất sát trùng.
- Có trong thành phần của nhiều dược phẩm.
- Trộn với lượng nhỏ KI và KIO3 thành muối iot giúp tránh các rối loạn do thiếu iot.
2. Điều chế
Cl2 + 2NaI → 2NaCl + I2
IV. Một số hợp chất của iot
1. Hidro iotua và axit iothidric
- HI kém bền với nhiệt, bị phân hủy thành I2 ở 300oC.
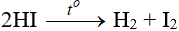
- Là axit mạnh, có tính khử mạnh:
8HI + H2SO4 → 4I2 + H2SO4 + 4H2O
2HI + 2FeCl3 → 2FeCl2 + I2 + 2HCl
2. Một số hợp chất khác
- Muối của axit iothidric đa số dễ tan trong nước.
- Một số muối iot không tan và có màu. Ví dụ: AgI màu vàng, PbI2 màu vàng.
- Ion iotua bị oxi hóa khi tác dụng với clo và brom:
2NaI + Cl2 → 2NaCl + I2
2NaI + Br2 → 2NaBr + I2
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
Xem thêm các phần Lý thuyết Hóa học lớp 10 ôn thi Tốt nghiệp THPT khác:
Lý thuyết Hidro clorua - hydrochloric acid (HCl) và muối clorua
- Lý thuyết về clo và hợp chất của clo
- Tóm tắt lý thuyết Hóa 10 chương 5
Để học tốt lớp 10 các môn học sách mới:
- Giải bài tập Lớp 10 Kết nối tri thức
- Giải bài tập Lớp 10 Chân trời sáng tạo
- Giải bài tập Lớp 10 Cánh diều
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Lớp 10 - Kết nối tri thức
- Soạn văn 10 (hay nhất) - KNTT
- Soạn văn 10 (ngắn nhất) - KNTT
- Soạn văn 10 (siêu ngắn) - KNTT
- Giải sgk Toán 10 - KNTT
- Giải sgk Vật lí 10 - KNTT
- Giải sgk Hóa học 10 - KNTT
- Giải sgk Sinh học 10 - KNTT
- Giải sgk Địa lí 10 - KNTT
- Giải sgk Lịch sử 10 - KNTT
- Giải sgk Kinh tế và Pháp luật 10 - KNTT
- Giải sgk Tin học 10 - KNTT
- Giải sgk Công nghệ 10 - KNTT
- Giải sgk Hoạt động trải nghiệm 10 - KNTT
- Giải sgk Giáo dục quốc phòng 10 - KNTT
- Lớp 10 - Chân trời sáng tạo
- Soạn văn 10 (hay nhất) - CTST
- Soạn văn 10 (ngắn nhất) - CTST
- Soạn văn 10 (siêu ngắn) - CTST
- Giải Toán 10 - CTST
- Giải sgk Vật lí 10 - CTST
- Giải sgk Hóa học 10 - CTST
- Giải sgk Sinh học 10 - CTST
- Giải sgk Địa lí 10 - CTST
- Giải sgk Lịch sử 10 - CTST
- Giải sgk Kinh tế và Pháp luật 10 - CTST
- Giải sgk Hoạt động trải nghiệm 10 - CTST
- Lớp 10 - Cánh diều
- Soạn văn 10 (hay nhất) - Cánh diều
- Soạn văn 10 (ngắn nhất) - Cánh diều
- Soạn văn 10 (siêu ngắn) - Cánh diều
- Giải sgk Toán 10 - Cánh diều
- Giải sgk Vật lí 10 - Cánh diều
- Giải sgk Hóa học 10 - Cánh diều
- Giải sgk Sinh học 10 - Cánh diều
- Giải sgk Địa lí 10 - Cánh diều
- Giải sgk Lịch sử 10 - Cánh diều
- Giải sgk Kinh tế và Pháp luật 10 - Cánh diều
- Giải sgk Tin học 10 - Cánh diều
- Giải sgk Công nghệ 10 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 10 - Cánh diều
- Giải sgk Giáo dục quốc phòng 10 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

