Lý thuyết Khái quát về nhóm Halogen (hay, chi tiết)
Bài viết Lý thuyết Khái quát về nhóm Halogen hay, chi tiết giúp bạn nắm vững kiến thức trọng tâm Khái quát về nhóm Halogen.
Lý thuyết Khái quát về nhóm Halogen (hay, chi tiết)
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
Bài giảng: Bài 21: Khái quát về nhóm halogen - Cô Phạm Thu Huyền (Giáo viên VietJack)
I. Nhóm halogen trong bảng tuần hoàn các nguyên tố
- Gồm có các nguyên tố 9F 17Cl 35Br 53I 85At. Phân tử dạng X2 như F2 khí màu lục nhạt, Cl2 khí màu vàng lục, Br2 lỏng màu nâu đỏ, I2 tinh thể tím.
II. Cấu hình electron nguyên tử và cấu tạo phân tử của các nguyên tố trong nhóm halogen
- Cấu hình electron lớp ngoài cùng của nguyên tử các halogen là ns2np5
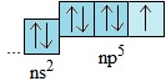
- Dễ nhận thêm một electron để đạt cấu hình bền vững của khí hiếm
X + 1e → X- (X: F, Cl, Br, I)
- Ở trạng thái cơ bản, nguyên tử các halogen đều có một electron độc thân.
- Lớp electron ngoài cùng của nguyên tử flo là lớp thứ hai nên không có phân lớp d. Nguyên tử clo, brom và iot có phân lớp d còn trống, khi được kích thích 1, 2 hoặc 3 electron có thể chuyển đến những obitan d còn trống:
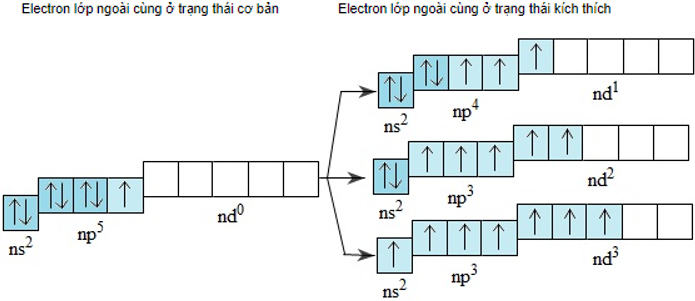
Do đó ở các trạng thái kích thích, nguyên tử clo, brom hoặc iot có thể có 3, 5 hoặc 7 electron độc thân.
III. Khái quát về tính chất của các halogen
1. Tính chất vật lý
- Nhiệt độ nóng chảy và nhiệt độ sôi: Tăng dần từ F đến I.
- Nguyên tử halogen có 7e lớp ngoài cùng ns2np5, bán kính nguyên tử nhỏ, có độ âm điện lớn ⇒ dễ nhận e, halogen có tính oxi hóa mạnh và là phi kim điển hình.
Ion halogenua X- có mức oxi hóa thấp nhất nên thể hiện tính khử.
| I2 Br2 Cl2 F2 | Tính oxi hóa tăng dần |
| 2I- 2Br- 2Cl- 2F- | Tính khử giảm dần |
- Lí tính:
| Halogen | F2 | Cl2 | Br2 | I2 |
| Trạng thái | Khí | Khí | Lỏng | Rắn |
| Màu sắc | Xanh nhạt | Vàng lục | Đỏ nâu | Tím than |
- Giữa các phân tử X2 chỉ có lực hút Van der Waals yếu nên các halogen hoặc ở trạng thái khí (F2, Cl2) hoặc ở trạng thái lỏng (Br2) dễ bay hơi, cũng có thể ở trạng thái rắn(I2) dễ thăng hoa.
- Tính tan: Flo phân hủy nước rất mạnh nên không tan trong nước.
Các halogen khác tan tương đối ít trong nước và tan nhiều trong dung môi hữu cơ.
2. Tính chất hóa học
- Cấu hình e lớp ngoài cùng tương tự nhau nên các halogen có nhiều điểm giống nhau về tính chất hóa học:
+ Có 7 e lớp ngoài cùng nên có xu hướng nhận thêm 1 e tạo thành ion âm X-.
+ Là phi kim điển hình, có tính oxi hóa mạnh.
- Tính oxi hóa của halogen:
Nhóm halogen với 7 điên tử ở lớp ngoài cùng và độ âm điện lớn, nguyên tử halogen X dễ dàng lấy 1 điện tử tạo ra X-có cấu hình khí trơ bền vững.
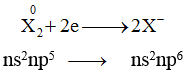
Do đó tính chất quan trọng nhất của nhóm halogen là tính oxi hóa, tính này giảm dần từ F2 (chất oxi hóa mạnh nhất) đến I2 (chất oxi hóa trung bình).
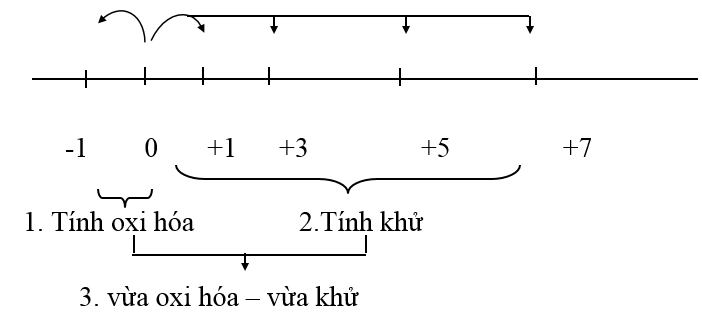
Các bậc oxi hóa đặc trưng của các halogen là: -1, 0, +1, +3, +5, +7 (trừ F luôn có số oxi hóa -1).
Ở dạng đơn chất, các halogen tồn tại dưới dạng phân tử X2. Có bậc oxi hóa trung gian là 0 là bậc oxi hóa trung gian. Nên nó vừa thể hiện tính oxi hóa vừa thể hiện tính khử.
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
Xem thêm các phần Lý thuyết Hóa học lớp 10 ôn thi Tốt nghiệp THPT khác:
Lý thuyết Hidro clorua - hydrochloric acid (HCl) và muối clorua
- Lý thuyết về clo và hợp chất của clo
- Tóm tắt lý thuyết Hóa 10 chương 5
Để học tốt lớp 10 các môn học sách mới:
- Giải bài tập Lớp 10 Kết nối tri thức
- Giải bài tập Lớp 10 Chân trời sáng tạo
- Giải bài tập Lớp 10 Cánh diều
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Lớp 10 - Kết nối tri thức
- Soạn văn 10 (hay nhất) - KNTT
- Soạn văn 10 (ngắn nhất) - KNTT
- Soạn văn 10 (siêu ngắn) - KNTT
- Giải sgk Toán 10 - KNTT
- Giải sgk Vật lí 10 - KNTT
- Giải sgk Hóa học 10 - KNTT
- Giải sgk Sinh học 10 - KNTT
- Giải sgk Địa lí 10 - KNTT
- Giải sgk Lịch sử 10 - KNTT
- Giải sgk Kinh tế và Pháp luật 10 - KNTT
- Giải sgk Tin học 10 - KNTT
- Giải sgk Công nghệ 10 - KNTT
- Giải sgk Hoạt động trải nghiệm 10 - KNTT
- Giải sgk Giáo dục quốc phòng 10 - KNTT
- Lớp 10 - Chân trời sáng tạo
- Soạn văn 10 (hay nhất) - CTST
- Soạn văn 10 (ngắn nhất) - CTST
- Soạn văn 10 (siêu ngắn) - CTST
- Giải Toán 10 - CTST
- Giải sgk Vật lí 10 - CTST
- Giải sgk Hóa học 10 - CTST
- Giải sgk Sinh học 10 - CTST
- Giải sgk Địa lí 10 - CTST
- Giải sgk Lịch sử 10 - CTST
- Giải sgk Kinh tế và Pháp luật 10 - CTST
- Giải sgk Hoạt động trải nghiệm 10 - CTST
- Lớp 10 - Cánh diều
- Soạn văn 10 (hay nhất) - Cánh diều
- Soạn văn 10 (ngắn nhất) - Cánh diều
- Soạn văn 10 (siêu ngắn) - Cánh diều
- Giải sgk Toán 10 - Cánh diều
- Giải sgk Vật lí 10 - Cánh diều
- Giải sgk Hóa học 10 - Cánh diều
- Giải sgk Sinh học 10 - Cánh diều
- Giải sgk Địa lí 10 - Cánh diều
- Giải sgk Lịch sử 10 - Cánh diều
- Giải sgk Kinh tế và Pháp luật 10 - Cánh diều
- Giải sgk Tin học 10 - Cánh diều
- Giải sgk Công nghệ 10 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 10 - Cánh diều
- Giải sgk Giáo dục quốc phòng 10 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

