150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải (cơ bản – phần 4)
Với 150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm câu trắc nghiệm Crom, Sắt, Đồng.
150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải (cơ bản – phần 4)
Thi online Hóa 12 KNTTThi online Hóa 12 CDThi online Hóa 12 CTST
Bài giảng: Bài tập tổng hợp về sắt và hợp chất của sắt - Cô Nguyễn Thị Thu (Giáo viên VietJack)
Câu 121: Cho các hoá chất:
(a) Dung dịch HNO3
(b) Dung dịch H2S có hòa tan O2
(c) O2
(d) Dung dịch FeCl3
(e) Dung dịch H2SO4 loãng
(f) Dung dịch NaCl
Kim loại Ag không tác dụng với chất nào ?
A. b, c, e
B. b, c
C. d, e, f
D. c, d, e, f
Lời giải:
Ag tác dụng được với dung dịch HNO3, H2S có hòa tan O2
Ag không tác dụng với O2, FeCl3 , H2SO4, NaCl
→ Đáp án D
Câu 122. Có các cặp chất sau: Cu và dung dịch FeCl3; H2S và dung dịch CuSO4; H2S và dung dịch FeCl3; dung dịch AgNO3 và dung dịch FeCl3. Số cặp chất xảy ra phản ứng ở điều kiện thường là:
A. 2 B. 3
C. 4 D. 1
Lời giải:
Các cặp chất xảy ra phản ứng:
Cu + 2FeCl3 → CuCl2 + 2FeCl2
H2S + CuSO4 → CuS + H2SO4
H2S + 2FeCl3 → 2FeCl2 + S + 2HCl
3AgNO3 + FeCl3 → 3AgCl + Fe(NO3)3
→ Đáp án C
Câu 123. Cho Fe vào dung dịch AgNO3 dư. Sau phản ứng hoàn toàn ta thu được dung dịch X và kết tủa Y. Trong dung dịch X có chứa:
A. Fe(NO3)3, AgNO3, Fe(NO3)2.
B. Fe(NO3)3, Fe(NO3)2.
C. Fe(NO3)3, AgNO3.
D. AgNO3, Fe(NO3)2.
Lời giải:
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Fe(NO3)2 + AgNO3 dư → Fe(NO3)3 + Ag
→ Đáp án C
Câu 124. Có các phát biểu sau:
(1) Thiếc, chì là những kim loại mà nguyên tử có 4 electron ở lớp ngoài cùng.
(2) Pb không tác dụng với dung dịch H2SO4 loãng lẫn dung dịch H2SO4 đặc nóng vì sản phẩm là PbSO4 không tan bọc ngoài kim loại, ngăn không cho phản ứng xảy ra tiếp.
(3) Sn, Pb bị hòa tan trong dung dịch kiềm, đặc nóng.
(4) Sn tác dụng với dung dịch H2SO4 loãng và dung dịch H2SO4 đặc tạo ra cùng một loại muối.
Các phát biểu đúng là:
A. 1, 2 B. 2, 3
C. 1, 3 D. 3, 4
Lời giải:
(1) đúng, thiếc: [Kr]4d105s25p2; Chì: [Kr]4f145d106s26p2; cả 2 chất thuộc nhóm IVA
(2) sai, Pb tan nhanh trong H2SO4 đặc nóng vào tạo thành muối Pb(HSO4)2
(3) đúng
(4) sai, Sn tác dụng với H2SO4 loãng được Sn(II), còn với H2SO4 đặc được Sn(IV)
→ Đáp án C
Câu 125. Cho từ từ đến dư một lượng bột sắt vào trong bình đựng một lượng nhỏ khí clo đã được đun nóng. Sau khi các phản ứng xảy ra hoàn toàn, chất rắn thu được trong bình là
A. FeCl2
B. FeCl2 và FeCl3
C. Fe và FeCl2
D. Fe và FeCl3
Lời giải:
2Fe + 3Cl2 2FeCl3
Vậy sau phản ứng chất rắn gồm Fe, FeCl3.
Chú ý phản ứng FeCl2 với Cl2 xảy ra khi FeCl2 ở trạng thái dung dịch
→ Đáp án D
Câu 126. Cho hỗn hợp X gồm Fe2O3, ZnO và Cu tác dụng với dung dịch HCl (dư) thu được dung dịch Y và phần không tan Z. Cho Y tác dụng với dung dịch NaOH (loãng, dư) thu được kết tủa
A. Fe(OH)2 và Cu(OH)2.
B. Fe(OH)2, Cu(OH)2 và Zn(OH)2.
C. Fe(OH)3.
D. Fe(OH)3 và Zn(OH)2.
Lời giải:
Do thu được cả kết tủa nên Cu còn dư sau phản ứng với Fe3+
Như vậy, trong dung dịch Y có FeCl2, ZnCl2 và CuCl2
Cho phản ứng với NaOH thì kết tủa thu được là Fe(OH)2 và Cu(OH)2
→ Đáp án A
Câu 127. Nhiệt phân hoàn toàn hỗn hợp gồm x mol AgNO3 và y mol Cu(NO3)2 được hỗn hợp khí có M = 42,5 amu. Tỉ số x/y là:
A. 1 B. 3
C. 2 D. 4
Lời giải:
Tổng số NO2 và O2 thu được
nNO2 = x + 2y
nO2 = 0,5x + 0,5 y
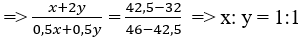
→ Đáp án A
Câu 128. Gang, thép là hợp kim của sắt. Tìm phát biểu đúng ?
A. Gang là hợp kim sắt – cacbon (5-10%).
B. Thép là hợp kim sắt – cacbon (2-5%).
C. Nguyên tắc sản xuất gang là khử sắt trong oxit bằng CO, H2 hay Al ở nhiệt độ cao.
D. Nguyên tắc sản xuất thép là oxi hóa các tạp chất trong gang (C, Si, Mn,S, P..) thành oxit, nhằm giảm hàm lượng của chúng.
Lời giải:
Gang là hợp kim sắt – cacbon (2-5%).
Thép là hợp kim sắt – cacbon (hàm lượng C < 2%)
Nguyên tắc sản xuất gang khử sắt trong oxit bằng CO ở nhiệt độ cao
→ Đáp án D
Câu 129. Để bảo quản dung dịch muối sắt (II) trong phòng thí nghiệm, người ta thường ngâm vào dung dịch đó
A. Một thanh Cu
B. Một thanh Zn
C. Một thanh Fe
D. Một thanh AI
Lời giải:
- Trong điều kiện thường Fe2+ dễ chuyển thành Fe3+
- Khi có Fe thì: Fe + 2Fe3+ → 3Fe2+
⇒ Do đó, trong dung dịch luôn có Fe2+
→ Đáp án C
Câu 130. Trong các cặp kim loại sau: (1) Mg, Fe; (2) Fe, Cu; (3) Fe, Ag . Cặp kim loại khi tác dụng với dung dịch HNO3 có thể tạo ra dung dịch chứa tối đa 3 muối (không kể trường hợp tạo NH4NO3) là:
A. (1)
B. (1) và (2)
C. (2) và (3)
D. (1) và (2) và (3)
Lời giải:
(1) Phản ứng với HNO3 thì Mg phản ứng trước, sau đến sắt, nếu dư sắt thì 3 muối
(2) Phản ứng với HNO3 thì Fe phản ứng trước nếu Fe và Cu dư thì có thể tạo 3 muối.
(3) Không có trường hợp nào do Ag+ có tính oxi hóa mạnh hơn Fe3+... hơn nữa chỉ tạo ra Fe3+
→ Đáp án B
Câu 131. Người chụp ảnh thường dùng dung dịch X để lau sạch những vết đen bám trên Ag. X là
A. Na2S2O3. B. Na2S2O7.
C. Na2CrO4. D. NaSCN.
Lời giải:
Trong nhiếp ảnh người ta dùng AgBr (không dùng AgCl kém nhạy, AgI quá nhạy với ánh sáng).
Để lau sạch những viết bám đen người ta dùng Na2S2O3 có khả năng hòa tan lớp AgBr
AgBr + 2Na2S2O3 → Na3[Ag(S2O3)2] + NaBr.
→ Đáp án A
Câu 132. Gang, thép là hợp kim của sắt. Tìm phát biểu đúng ?
A. Gang là hợp kim sắt – cacbon (5-10%).
B. Thép là hợp kim sắt – cacbon (2-5%).
C. Nguyên tắc sản xuất gang là khử sắt trong oxit bằng CO, H2 hay Al ở nhiệt độ cao.
D. Nguyên tắc sản xuất thép là oxi hóa các tạp chất trong gang (C, Si, Mn,S, P..) thành oxit, nhằm giảm hàm lượng của chúng.
Lời giải:
Gang là hợp kim sắt – cacbon (2-5%).
Thép là hợp kim sắt – cacbon (hàm lượng C < 2%)
Nguyên tắc sản xuất gang khử sắt trong oxit bằng CO ở nhiệt độ cao
→ Đáp án D
Câu 133. Nhỏ từ từ đến dư dung dịch FeSO4 đã được axit hóa bằng H2SO4 vào dung dịch KMnO4. Hiện tượng quan sát được là
A. dung dịch màu tím hồng bị nhạt dần rồi chuyển sang màu vàng
B. dung dịch màu tím hồng bị nhạt dần đến không màu
C. dung dịch màu tím hồng bị chuyển dần sang nâu đỏ
D. màu tím bị mất ngay. Sau đó dần dần xuất hiện trở lại thành dung dịch có màu hồng
Lời giải:
10FeSO4 + 8H2SO4 + 2KMnO4 → 5Fe2(SO4)3 + 2MnSO4 + 8H2O + K2SO4.
Chú ý muối Fe2(SO4)3 và FeCl3 có màu vàng
→ Đáp án A
Câu 134. Dãy gồm các chất mà khi cho từng chất tác dụng với dung dịch HI đều sinh ra sản phẩm có iot là
A. Fe2O3, Fe3O4, Fe2(SO4)3, Cl2
B. Fe(OH)3, FeO, FeCl3, Fe3O4
C. AgNO3, Na2CO3, Fe2O3, Br2
D. Fe3O4, FeO, AgNO3, FeS
Lời giải:
Ta có AgNO3 + HI → AgI↓ + HNO3 → Loại C, D
FeO + 2HI → FeI2 + H2O → Loại B
Chú ý các hợp chất Fe2O3, Fe(OH)3, Fe3O4, Fe2(SO4)3 khi tác dụng với HI sinh ra hợp chất Fe3+ có tính oxi hóa mạnh tương tác với I- trong dung dịch sinh ra I2 và Fe2+.
→ Đáp án A
Câu 135. Cho các dung dịch: Cu(NO3)2, AlCl3, AgNO3, ZnSO4, NaCl, FeCl3. Số dung dịch tạo kết tủa với dung dịch NH3 dư là:
A. 5 B. 2
C. 3 D. 4
Lời giải:
Các chất tạo kết tủa với NH3 là AlCl3 và FeCl3
→ Đáp án B
Câu 136. Phát biểu nào sau đây không đúng?
A. Crom (VI) oxit là basic oxide.
B. ethyl alcohol bốc cháy khi tiếp xúc với CrO3.
C. Khi phản ứng với dung dịch HCl, kim loại Cr bị oxi hóa thành ion Cr2+.
D. Crom (III) oxit và crom (II) hiđroxit đều là chất có tính lưỡng tính.
Lời giải:
- Crom (VI) oxit là basic oxide không đúng vì: CrO3 là acidic oxide.
- ethyl alcohol bốc cháy khi tiếp xúc với CrO3: đúng vì CrO3 có tính oxi hóa mạnh.
- Khi phản ứng với dung dịch HCl, kim loại Cr bị oxi hóa thành ion Cr2+ đúng vì dung dịch HCl không có tính oxi hóa trong khi đó Cr có 3 số oxi hóa phổ biến +2, +3, +6.
Vậy: Crom (VI) oxit là basic oxide là sai.
→ Đáp án A
Câu 137. Cho các dung dịch loãng: (1) FeCl3, (2) FeCl2, (3) H2SO4, (4) HNO3, (5) hỗn hợp gồm HCl và NaNO3. Những dung dịch phản ứng được với kim loại Cu là:
A. (1), (2), (3) B. (1), (3), (5)
C. (1), (4), (5) D. (1), (3), (4)
Lời giải:
Các dung dịch phản ứng với kim loại đồng là FeCl3, HNO3, hỗn hợp gồm HCl, NaNO3. Các phản ứng:
2FeCl3 + Cu → 2FeCl2 + CuCl2
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
3Cu + 2 NO3- + 8H+ → 3Cu2+ + 2NO↑ + 4H2O
→ Đáp án C
Câu 138. Cho các phát biểu về đồng, bạc, vàng như sau:
(1) Tính khử yếu dần theo thứ tự: Cu > Ag > Au
(2) Cả 3 kim loại đều tan trong dung dịch HNO3
(3) Cả 3 kim loại đều có thể tồn tại trong tự nhiên dưới dạng đơn chất
(4) Dung dịch HNO3 chỉ hòa tan được Cu, Ag; còn không hòa tan được Au.
(5) Chỉ có Cu mới hòa tan trong dung dịch HCl, còn Ag, Au không hòa tan trong dung dịch HCl.
Số phát biểu đúng là:
A. 2. B. 3.
C. 4. D. 5.
Lời giải:
• Tính khử yếu dần theo thứ tự: Cu > Ag > Au.
- Dung dịch HNO3 chỉ hòa tan được Cu, Ag; còn Au chỉ hòa tan trong nước cường toan ( hỗn hợp 1 thể tích HNO3 và 3 thể tích HCl đặc).
- Cả ba kim loại Cu, Ag, Au đứng sau H nên đều không hòa tan trong HCl.
- Cả ba kim loại đều có thể tồn tại trong tự nhiên dưới dạng đơn chất.
→ Có 3 phát biểu đúng là (1), (3), (4)
→ Đáp án B
Câu 139. Dãy gồm các chất mà khi cho từng chất tác dụng với dung dịch HI đều sinh ra sản phẩm có iot là
A. Fe2O3, Fe3O4, Fe2(SO4)3, Cl2
B. Fe(OH)3, FeO, FeCl3, Fe3O4
C. AgNO3, Na2.CO3, Fe2O3, Br2
D. Fe3O4, FeO, AgNO3, FeS
Lời giải:
Ta có AgNO3 + HI → AgI↓ + HNO3 → Loại C, D
FeO + 2HI → FeI2 + H2O → Loại B
Chú ý các hợp chất Fe2O3, Fe(OH)3, Fe3O4, Fe2(SO4)3 khi tác dụng với HI sinh ra hợp chất Fe3+ có tính oxi hóa mạnh tương tác với I- trong dung dịch sinh ra I2 và Fe2+.
→ Đáp án A
Câu 140. Cho vài giọt dung dịch H2S vào dung dịch FeCl3 hiện tượng xảy ra là
A. dung dịch xuất hiện kết tủa đen
B. có kết tủa vàng
C. kết tủa trắng hóa nâu
D. không hiện tượng gì
Lời giải:
H2S + 2FeCl3 → S↓(vàng) + 2FeCl2 + 2HCl
→ Đáp án B
Câu 141. Vàng bị hoà tan trong nước cường toan tạo thành
A. AuCl và khí NO.
B. AuCl3 và khí NO2.
C. AuCl và khí NO2.
D. AuCl3 và khí NO.
Lời giải:
Au + HNO3 + 3HCl → AuCl3 + NO + 2H2O
→ Đáp án A
Câu 142. Ni tác dụng được với tất cả các chất trong dãy nào sau đây ?
A. O2, F2, Cl2, H2
B. O2, Cl2, dung dịch H2SO4 đặc nóng, dung dịch AgNO3
C. F2, Cl2, dung dịch HNO3, dung dịch Fe(NO3)2
D. S, F2, dung dịch NaCl, dung dịch Pb(NO3)2
Lời giải:
A sai, Ni không tác dụng với H2
C sai, Ni không tác dụng với Fe(NO3)2
D sai, Ni không tác dụng với NaCl
Ni tác dụng được với tất cả các chất trong B
→ Đáp án B
Câu 143. Có các phát biểu về kẽm sau:
(a) Zn có thể tác dụng với các dung dịch HCl, HNO3 đặc nguội, NaOH;
(b) những đồ vật bằng Zn không bị han rỉ, không bị oxi hóa trong không khí và trong nước;
(c) có thể dùng Zn để đẩy Au ra khỏi phức xianua [Au(CN)2]- (phương pháp khai thác vàng);
(d) Zn không thể đẩy được Cu ra khỏi dung dịch CuSO4
(e) không tồn tại hợp chất ZnCO3
Số phát biểu đúng là
A. 2. B. 3.
C. 4. D. 5.
Lời giải:
Có các phát biểu về kẽm:
- Zn có thể tác dụng với các dung dịch HCl, HNO3 đặc, nguội, NaOH.
- Zn không bị han rỉ, không bị oxi hóa trong không khí và trong nước vì trên bề mặt kẽm có màng oxit hoặc carbonate bazơ bảo vệ.
- Zn có thể đẩy Au ra khỏi phức xianua [Au(CN)2]- (phương pháp khai thác vàng).
- Zn có thể đẩy được Cu ra khỏi dung dịch CuSO4.
- ZnCO3 tồn tại ở dạng rắn, không tồn tại ở dạng dung dịch.
→ Có 3 phát biểu đúng là (a), (b), (c)
→ Đáp án B
Câu 144. Nhỏ từ từ dung dịch NH3 vào dung dịch CuSO4 cho tới dư. Hiện tượng quan sát được là
A. xuất hiện kết tủa màu xanh nhạt, lượng kết tủa tăng dần.
B. xuất hiện kết tủa màu xanh nhạt, lượng kết tủa tăng dần đến không đổi. Sau đó lượng kết tủa giảm dần cho tới khi tan hết thành dung dịch màu xanh đậm.
C. xuất hiện kết tủa màu xanh nhạt, lượng kết tủa tăng đến không đổi.
D. xuất hiện kết tủa màu xanh nhạt.
Lời giải:
Nhỏ từ từ dung dịch NH3 vào dung dịch CuSO4 cho tới dư:
CuSO4 + 2NH3 + 2H2O → Cu(OH)2↓ + (NH4)2SO4
Cu(OH)2↓ + 4NH3 → [Cu(NH3)4](OH)2
→ Hiện tượng quan sát được là xuất hiện ↓ màu xanh nhạt, lượng ↓ tăng dần đến không đổi. Sau đó ↓ giảm dần cho tới khi tan hết thành dung dịch màu xanh đậm
→ Đáp án B
Câu 145. Cho thanh Zn tác dụng với dung dịch CuSO4, nhận định đúng là:
A. Zn bị khử còn Cu2+ bị oxi hóa
B. Zn bị oxi hóa còn Cu2+ bị khử
C. Zn và Cu đều bị oxi hóa
D. Zn và Cu đều bị khử
Lời giải:
Phương trình phản ứng: Zn + CuSO4 → ZnSO4 + Cu↓ (đỏ)
Cu sinh ra bám vào lá Zn, đồng thời lượng Cu2+ trong dung dịch giảm đi nên màu xanh giảm dần.
→ Đáp án B
Câu 146. Cho bột sắt dư vào dung dịch H2SO4 loãng thu được V lít H2 (đktc) và dung dịch có chứa m1 gam muối. Mặt khác, cho bột sắt dư vào dung dịch H2SO4 đặc, nóng thu được V lít SO2 (đktc) và dd có chứa m2 gam muối. So sánh m1 và m2.
A. m1 = m2
B. m1 = 0,5m2
C. m1 > m2
D. m1 < m2
Lời giải:
Cho Fe dư + H2SO4 → m1 gam muối + V lít H2
Fe + 2H+ → Fe2+ + H2↑
nFe2+ = nH2 = V/22,4 → m1 = mFeSO4 = V/22,4 x 152 gam.
Cho Fe + H2SO4 đặc, nóng → m2 gam muối + V lít SO2
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ + 6H2O
nFe2(SO4)3 = 1/3 x nSO2 = 1/3 x V/22,4 mol
→ m2 = mFe2(SO4)3 = 1/3 x V/22,4 x 400 gam
→ m1 > m2
→ Đáp án C
Câu 147. Cho vào ống nghiệm một ít tinh thể K2Cr2O7, sau đó cho nước vào và khuấy đều để K2Cr2O7 tan hết, thu được dung dịch X. Thêm vài giọt dung dịch KOH vào dung dịch X, thu được dung dịch Y. Màu của dung dịch X và Y lần lượt là:
A. Màu vàng và màu da cam
B. Màu nâu đỏ và màu vàng
C. Màu da cam và màu vàng
D. Màu vàng và màu nâu đỏ
Lời giải:
Trong dung dịch K2Cr2O7 (màu da cam) có cân bằng:
Cr2O72-(da cam) + H2O ⇆ 2Cr2O42-(vàng) + 2H+
Khi thêm dung dịch KOH vào, OH- trung hòa H+ làm cân bằng chuyển dịch sang phải tạo ra CrO42- có màu vàng
→ Đáp án C
Câu 148. Cho các chất sau: Cu(OH)2, AgCl, Ni, Zn(OH)2, Pb, Sn. Số chất tan trong dung dịch NH3 là:
A. 2. B. 3.
C. 4. D. 5.
Lời giải:
Cu(OH)2↓ + 4NH3 → [Cu(NH3)4](OH)2
AgCl↓ + 2NH3 → [Ag(NH3)2]Cl
Ni + NH3 → không phản ứng.
Zn(OH)2↓ + 4NH3 → [Zn(NH3)4](OH)2
Pb + NH3 → không phản ứng.
Sn + NH3 → không phản ứng.
→ Có 3 chất tan trong dung dịch NH3
→ Đáp án B
Câu 149. Để oxi hóa hoàn toàn 0,01 mol CrCl3 thành K2CrO4 bằng Cl2 khi có mặt KOH, lượng tối thiểu Cl2 và KOH tương ứng là:
A. 0,015 mol và 0,04 mol
B. 0,015 mol và 0,08 mol
C. 0,03 mol và 0,08 mol
D. 0,03 mol và 0,04 mol
Lời giải:
2CrCl3 (0,01) + 3Cl2 (0,015) + 16KOH (0,08) → 2K2CrO4 + 12KCl + 8H2O
→ Đáp án B
Câu 150. Những bức tranh cổ (vẽ bằng bột chì, thành phần chính là muối bazơ 2PbCO3.Pb(OH)2) thường có màu đen. Hãy cho biết có thể dùng chất nào dưới đây để phục hồi bức tranh cổ này ?
A. H2O2 B. HNO3
C. H2SO4 D. AgNO3
Lời giải:
- Những bức tranh cổ vẽ bằng bột chì (thành phần chính là muối bazơ 2PbCO3.Pb(OH)2). Khi để lâu bột chì tác dụng với H2S trong không khí tạo PbS màu đen.
2PbCO3.Pb(OH)2 + 3H2S → 3PbS + 2CO2 + 4H2O
- Có thể dùng H2O2 để phục hồi bức tranh này, vì PbS màu đen biến thành PbSO4 thành màu trắng theo phản ứng:
PbS + 4H2O2 → PbSO4 + 4H2O2.
→ Đáp án A
Bài giảng: Bài tập sắt, hợp chất của sắt tác dụng với chất oxi hóa mạnh - Cô Nguyễn Thị Thu (Giáo viên VietJack)
Thi online Hóa 12 KNTTThi online Hóa 12 CDThi online Hóa 12 CTST
Xem thêm các dạng bài tập Hóa học lớp 12 ôn thi Tốt nghiệp có lời giải hay khác:
- 150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải (cơ bản – phần 1)
- 150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải (cơ bản – phần 2)
- 150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải (cơ bản – phần 3)
- 150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải (nâng cao – phần 1)
- 150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải (nâng cao – phần 2)
- 150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải (nâng cao – phần 3)
- 150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải (nâng cao – phần 4)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Lớp 12 Kết nối tri thức
- Soạn văn 12 (hay nhất) - KNTT
- Soạn văn 12 (ngắn nhất) - KNTT
- Giải sgk Toán 12 - KNTT
- Giải sgk Vật Lí 12 - KNTT
- Giải sgk Hóa học 12 - KNTT
- Giải sgk Sinh học 12 - KNTT
- Giải sgk Lịch Sử 12 - KNTT
- Giải sgk Địa Lí 12 - KNTT
- Giải sgk Giáo dục KTPL 12 - KNTT
- Giải sgk Tin học 12 - KNTT
- Giải sgk Công nghệ 12 - KNTT
- Giải sgk Hoạt động trải nghiệm 12 - KNTT
- Giải sgk Giáo dục quốc phòng 12 - KNTT
- Giải sgk Âm nhạc 12 - KNTT
- Giải sgk Mĩ thuật 12 - KNTT
- Lớp 12 Chân trời sáng tạo
- Soạn văn 12 (hay nhất) - CTST
- Soạn văn 12 (ngắn nhất) - CTST
- Giải sgk Toán 12 - CTST
- Giải sgk Vật Lí 12 - CTST
- Giải sgk Hóa học 12 - CTST
- Giải sgk Sinh học 12 - CTST
- Giải sgk Lịch Sử 12 - CTST
- Giải sgk Địa Lí 12 - CTST
- Giải sgk Giáo dục KTPL 12 - CTST
- Giải sgk Tin học 12 - CTST
- Giải sgk Hoạt động trải nghiệm 12 - CTST
- Giải sgk Âm nhạc 12 - CTST
- Lớp 12 Cánh diều
- Soạn văn 12 Cánh diều (hay nhất)
- Soạn văn 12 Cánh diều (ngắn nhất)
- Giải sgk Toán 12 Cánh diều
- Giải sgk Vật Lí 12 - Cánh diều
- Giải sgk Hóa học 12 - Cánh diều
- Giải sgk Sinh học 12 - Cánh diều
- Giải sgk Lịch Sử 12 - Cánh diều
- Giải sgk Địa Lí 12 - Cánh diều
- Giải sgk Giáo dục KTPL 12 - Cánh diều
- Giải sgk Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 - Cánh diều
- Giải sgk Giáo dục quốc phòng 12 - Cánh diều
- Giải sgk Âm nhạc 12 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

