150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải (nâng cao – phần 4)
Với 150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm câu trắc nghiệm Crom, Sắt, Đồng.
150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải (nâng cao – phần 4)
Thi online Hóa 12 KNTTThi online Hóa 12 CDThi online Hóa 12 CTST
Bài giảng: Bài tập tổng hợp về sắt và hợp chất của sắt - Cô Nguyễn Thị Thu (Giáo viên VietJack)
Câu 121. Cho 28 gam Fe hòa tan trong 256 ml dung dịch H2SO4 14% (có khối lượng riêng 1,095 g/ml), có khí hiđro thoát ra. Sau khi kết thúc phản ứng, đem cô cạn dung dịch thì thu được m gam một tinh thể muối ngậm 7 phân tử nước (nmuối : nnước = 1 : 7). Trị số của m là
A. 116,8 gam B. 70,13 gam
C. 111,2 gam D. 139 gam
Lời giải:
mH2SO4 = 256. 1,095. 0,14 = 39,2448 g ⇒ nH2SO4 (0,4) < nFe (0,5)
nFeSO4 = nH2SO4 = 0,4 mol
mFeSO4. 7H2O = 0,4 . 278 = 111,2 g
→ Đáp án C
Câu 122. Cho 10 g Fe vào dung dịch HNO3 loãng dư thu được sản phẩm khử NO duy nhất. Sau khi phản ứng xảy ra hoàn toàn, còn dư 1,6g Fe. Thể tích NO thoát ra ở điều kiện tiêu chuẩn là:
A. 2,24 B. 3,36
C. 4,48 D. 11,2
Lời giải:
mFe phản ứng = 10 - 1,6 = 8,4g → nFe phản ứng = 8,4/56 = 0,15 mol
Do Fe dư nên sau khi Fe bị HNO3 oxi hóa thành Fe3+ thì toàn bộ Fe3+ lại bị khử thành Fe2+ nên có phản ứng:
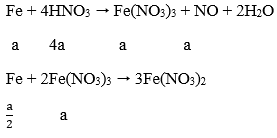
Ta có: a + a/2 = 0,15 → a = 0,1 mol
VNO = 0,1.22,4 = 2,24 lít
→ Đáp án A
Câu 123. Hòa tan a gam FeSO4.7H2O trong nước, được 300 ml dung dịch A. Thêm H2SO4 vào 200 ml dung dịch A, dung dịch hỗn hợp này làm mất màu 30ml dung dịch KMnO4 0,1M. Vậy a có giá trị là:
A. 62,55g B. 65,44g
C. 63,35g D. 55,67g
Lời giải:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Theo phương trình: nFeSO4 = 0,015 mol
Trong 300ml có: nFeSO4 = (0,015.300)/20 = 0,225 mol
mFeSO4.7H2O = a = 62,55 (g)
→ Đáp án A
Câu 124. Cho m gam bột Zn vào 500ml dung dịch Fe2(SO4)3 0,24M. Sau khi các phản ứng xảy ra hoàn toàn, khối lượng dung dịch tăng thêm 9,6 gam so với khối lượng dung dịch ban đầu. Giá trị của m là:
A. 32,50 B. 20,80
C. 29,25 D. 48,75
Lời giải:
Ta có: nFe2(SO4)3 = 0,12 mol → nFe3+ = 0,24 mol
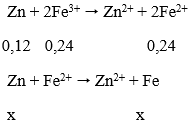
Ta có: mdd tăng = mZn phản ứng - mFe sinh ra
9,6 = 0,12 + x.65 - 56.x → x = 0,2
Vậy: mZn = (0,12 + 0,2).56 = 20,8 (g)
→ Đáp án B
Câu 125. Hòa tan hoàn toàn 12 gam hỗn hợp Fe và Cu (tỉ lệ mol 1:1) bằng axit HNO_3, thu được V lít hỗn hợp X gồm(NO và NO2) và dung dịch Y chỉ chứa 2 muối và axit dư. Tỉ khối hơi của X đối vơi hidro bằng 19. Tính thể tích hỗn hợp khí X.
A. 3,36l B. 4,48l
C. 5,6l D. 1,2 l
Lời giải:
Ta có: Mx = 38 = (30 + 46)/2 là trung bình cộng nên nNO = nNO2
Trong 12 gam hỗn hợp có 0,1 mol Fe và 0,1 mol Cu
Fe → Fe3+ + 3e
Cu → Cu2+ + 2e
⇒ ∑nelectron do chất khử cho = 0,5(mol)

Áp dụng định luật bảo toàn electron: 4x = 0,5 ⇒ x = 0,125(mol)
Vậy V = 0,125. 2. 22,4 = 5,6(lít)
→ Đáp án C
Câu 126. Hòa tan hoàn toàn 13,00 gam Zn trong dung dịch HNO3 loãng dư thu được dung dịch X và 0,448 lít khí N2 (đktc). Khối lượng muối trong dung dịch X là:
A. 18,90 gam B. 37,80 gam
C. 39,80 gam D. 28,35 gam
Lời giải:
Ta có: nZn = 13/65 = 0,2 mol và nN2 = 0,448/22,4 = 0,02 mol
ne nhường = 2.nZn = 0,4 mol > ne nhận = 10.nN2 = 0,2 mol → phản ứng tạo thành NH4NO3.
nNH4NO3 = (0,4 - 0,2)/8 = 0,025 mol
Khối lượng muối trong dung dịch X là = 180.0,2 + 80.0,025 = 39,80 gam
→ Đáp án C
Câu 127. Cho tan hoàn toàn 58 gam hỗn hợp gồm Fe, Cu, Ag trong dung dịch HNO3 2M thu được 0,15 mol NO; 0,05 mol N2O và dung dịch D. Cô cạn dung dịch D, khối lượng muối khan thu được là:
A. 120,4 gam B. 89,8 gam
C. 116,9 gam D. 110,7 gam
Lời giải:
Nhận xét: Nếu chỉ dùng phương pháp bảo toàn electron thông thường, ta cũng chỉ lập được 2 phương trình 3 ẩn số và sẽ gặp khó khăn trong việc giải. Để tính khối lượng muối NO_3^- trong bài toán trên ta có công thức:
nNO2 (trong muối) - a.nX
Trong đó: a là số electron mà N nhận để tạo X
Như vậy: mmuối khan = mFe, Cu, Ag + mNO3-
nNO3- = 3.nNO + 8.nN2O = 3.0,15 + 8.0,05 = 0,85 mol
mmuối khan = 58 + 0,95.62 = 110,7 (g)
→ Đáp án D
Câu 128. Để m gam phôi bào sắt ngoài không khí, sau một thời gian Fe bị oxi hóa thành hỗn hợp X gồm 4 chất rắn có khối lượng 27,2 gam. Hòa tan vừa hết X trong 300 ml dung dịch HCl nồng độ a mol/l thấy thoát ra 3,36 lít khí H2 (đktc) và dung dịch Y. Cho tiếp dung dịch HNO3 tới dư vào dung dịch Y được dung dịch Z chứa hỗn hợp FeCl3, Fe(NO3)3, HNO3 dư và có 2,24 lít NO duy nhất thoát ra (đktc). Giá trị của m và a lần lượt là
A. 22,4 gam và 3M
B. 16,8 gam và 2M
C. 22,4 gam và 2M
D. 16,8 gam và 3M
Lời giải:
Giả sử X gồm Fe và O:
nFe = x; nO = y
⇒ mX = 56a + 16b = 27,2 (1)
BT e: 3ne = 2nO + 3nNO + 2nH2
⇒ 3x = 2y + 3. 0,1 + 0,15 .2 ⇒ 3x = 2y + 0,6 (2)
Từ (1) và (2) ⇒ x = 0,4 mol; y = 0,3 mol
⇒ mFe = 0,4. 56 = 22,4 g
mH+ = 2.nO + 2.nH2 = 2. 0,3 + 2. 0,15 = 0,9 mol ⇒ a= 3M
→ Đáp án C
Câu 129. Nung nóng m gam PbS ngoài không khí sau một thời gian, thu được hỗn hợp rắn (có chứa một oxit) nặng 0,95 m gam. Phần trăm khối lượng PbS đã bị đốt cháy là:
A. 74,69% B. 95,00%
C. 25,31% D. 64,68%
Lời giải:
Sơ đồ: m(g) 0,95m (g) hh (PbO và PbS dư) + SO2
Áp dụng ĐLBTKL ta có:
mO = m - 0,95m = 0,05m (g) ⇒ nO = 3,125.10-3m (mol)
Ta có: nPbS phản ứng = nPbO = nO = 3,125.10-3m (mol)
⇒ %PbS (đã bị đốt cháy) =
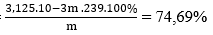
→ Đáp án A
Câu 130. Đốt cháy hòa toàn 15,4g hỗn hợp X gồm các kim loại Fe, Mg, Al thu được 25,1 g hỗn hợp các oxit Y. Hòa tan B bằng HCl 2M thì cần dùng thể tích là:
A. 0,6 lít B. 0,525 lít
C. 0,6125 lít D. 0,74 lít
Lời giải:
m = moxit - mkim loại = 25,1 - 15,3 = 9,8g
nO = 9,8/16 = 0,6125 mol
nH+ = 2nO = 0,6125. 2 = 1,225 mol
VHCl = 1,25/2 = 0,6125 (lít)
→ Đáp án C
Câu 131. Nhúng một đinh sắt vào 150ml dung dịch CuSO4. Sau khi phản ứng xảy ra hoàn toàn, lấy đinh sắt sấy khô, thấy khối lượng tăng lên 1,2g. Vậy nồng độ ban đầu của CuSO4 là:
A. 1M B. 2,5M
C. 2M D. 0,5M
Lời giải:
Phương trình phản ứng:
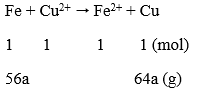
Ta có: Δm↑ = 64a - 56a = 1,2
a = 0,15 mol
CM (CuSO4) = 0,15/0,15 = 1M
→ Đáp án A
Câu 132. Cho 4,32 gam hỗn hợp gồm Zn, Fe và Cu vào cốc đựng dung dịch chứa 0,08 mol CuSO4. Sau phản ứng thu được dung dịch B và kết tủa C. Kết tủa C có:
A. Cu B. Cu, Fe, Zn
C. Cu, Fe D. Cu, Zn
Lời giải:
4,32/65 < n(Fe,Zn) < 4,32/56 → 0,0664 < nFe, Zn < 0,077
Ta thấy chỉ có Zn và Fe phản ứng hết với CuSO4 mà nFe, Zn < nCuSO4 nên Zn và Fe phản ứng hết.
CuSO4 dư → Kết tủa chỉ có Cu
→ Đáp án A
Câu 133. Hòa tan 5,6g Fe trong dung dịch HNO3 thu được khí NO duy nhất và dung dịch X. Thêm NaOH dư vào dung dịch X thu được kết tủa Y. Nung Y trong điều kiện không có oxi thu được chất rắn Z. Còn nung Y trong không khí thì thu được chất rắn T có khối lượng mT = mZ + 0,32. Vậy Y có khối lượng là:
A. 10,42 B. 11,2
C. 10,36 D. 13,4
Lời giải:
Z có FeO và Fe2O3
Ta có: nFeO = nO = 0,32/16 = 0,02 mol
nFe(OH)2 = 0,02 mol
nFe(OH)3 = nFe - nFe(OH)2 = 0,1 - 0,02 = 0,08 mol
mY = 0,02.90 + 0,08.107 = 10,36g
→ Đáp án C
Câu 134. Hòa tan hoàn toàn 13,00 gam Zn trong dung dịch HNO3 loãng dư thu được dung dịch X và 0,448 lít khí N2 (đktc). Khối lượng muối trong dung dịch X là:
A. 18,90 gam B. 37,80 gam
C. 39,80 gam D. 28,35 gam
Lời giải:
Ta có: nZn = 13/65 = 0,2 mol và nN2 = 0,448/22,4 = 0,02 mol
ne nhường = 2.nZn = 0,4 mol > ne nhận = 10.nN2 = 0,2 mol → phản ứng tạo thành NH4NO3.
nNH4NO3 = (0,4 - 0,2)/8 = 0,025 mol
Khối lượng muối trong dung dịch X là = 180.0,2 + 80.0,025 = 39,80 gam
Lưu ý: Đề bài không nói thu được khí X duy nhất nên có thể có muối NH4NO3 tạo thành.
→ Đáp án C
Câu 135. Hòa tan 4,76 gam hỗn hợp Zn, Al có tỉ lệ mol 1:2 trong 400ml dung dịch HNO3 1M vừa đủ, được dung dịch X chứa m gam muối khan và thấy có khí thoát ra. Giá trị của m là:
A. 25,8 gam B. 26,9 gam
C. 27,8 gam D. 28,8 gam
Lời giải:
Ta có: nZn = 0,04 mol; nAl = 0,08 mol
Do phản ứng không tạo khí nên trong dung dịch tạo NH4NO3. Trong dung dịch có: 0,04 mol Zn(NO3)2 và 0,08 mol Al(NO3)3.
Vậy số mol NO3- còn lại để tạo NH4NO3 là:
0,4 - 0,04.2 - 0,08.3 = 0,08 mol
Do đó trong dung dịch tạo 0,04 mol NH4NO3
m = 0,04.189 + 0,08.213 + 0,04.80 = 27,8 gam
→ Đáp án C
Câu 136. Cho hỗn hợp gồm 2 gam Fe và 3 gam Cu vào dung dịch HNO3 thấy thoát ra 0,448 lít khí NO(đktc). Tính khối lượng muối thu được trong dung dịch, biết các phản ứng xảy ra hoàn toàn.
A. 4,5g B. 3,6g
C. 2,4g D. 5,4g
Lời giải:
Phản ứng:
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O (1)
Fe + 2Fe(NO3)3 → 3Fe(NO3)2 (2)
Từ (1) ⇒ nFe = nFe(NO3)3 = nNO = 0,448/22,4 = 0,02(mol)
Từ (2) ⇒ nFe = 1/2 nFe(NO3)2 = 0,01(mol)
nFe(NO3)2 = 3/2 nFe(NO3)3 = 0,03(mol)
nFedu = 0,0375 - 0,02 - 0,01 = 0,0075(mol)
Fe dư nên Cu chưa phản ứng.
⇒ mFe(NO3)3 = 180. 0,03 = 5,4(gam)
→ Đáp án D
Câu 137. Khử m gam Fe3O4 bằng khí H2 thu được hổn hợp X gồm Fe và FeO, hỗn hợp X tác dụng vừa hết với 3 lít dung dịch H2SO4 0,2M (loãng). Giá trị của m là
A. 46,4 gam B. 23,2 gam
C. 11,6 gam D. 34,8 gam
Lời giải:
Fe3O4 -+H2, to→ FeO , Fe -H2SO4 (0,6 mol)→ FeSO4
Nhận thấy sau phản ứng chỉ thu được FeSO4 → nFeSO4 = nSO42- = 0,6 mol
Bảo toàn nguyên tố Fe → nFe3O4 = 0,6 : 3 = 0,2 mol
→ m = 46,4 gam.
→ Đáp án A
Câu 138. Đốt cháy hòa toàn 3,86g hỗn hợp gồm Fe, Al, Cu thu được 4,66g oxit. Cho toàn bộ lượng oxit này tác dụng với dung dịch axit H2SO4 20% (d = 1,14 g/ml). Vậy thể tích H2SO4 cần dùng tối thiểu là:
A. 21,1 ml B. 21,5 ml
C. 23,4 ml D. 19,6 ml
Lời giải:
mO = moxit - mkim loại = 4,66 - 3,86 = 0,8g
nO = 0,8/16 = 0,05 mol
nO = 2nH+ = nH2SO4 = 0,05 mol
V = (0,05. 98. 100)/(20. 1,14) = 21,5 ml
→ Đáp án C
Câu 139. Để định lượng Fe2+ trong mẫu phân tích người ta dùng phương pháp chuẩn độ đicromat dựa vào sơ đồ phản ứng sau:
Fe2+ + H+ + Cr2O72- → Fe3+ + Cr2+ + H2O
Hãy tính khối lượng Fe2+ trong dung dịch X biết đã dùng hết 30ml K2Cr2O7 0,1M.
A. 0,56 B. 0,112
C. 1,008 D. 1,56
Lời giải:
nK2Cr2O7 = 0,03.0,1 = 0,003 mol
Phương trình phản ứng:
6Fe2+ (0,03.6) + 14H+ + Cr2O72- (0,03) → 6Fe3+ +2Cr3+ + 7H2O
mFe = 0,03. 6. 56 = 1,008g
→ Đáp án C
Câu 140. Thể tích dung dịch HNO3 1M loãng ít nhất cần dùng để hòa tan hoàn toàn một hỗn hợp gồm 0,15 mol Fe và 0,15 mol Cu là: (Biết phản ứng tạo chất khử duy nhất là NO)
A. 1,0 lít B. 0,6 lít
C. 0,8 lít D. 1,2 lít
Lời giải:
Fe (0,15) + 4HNO3 (0,6) → Fe(NO3)3 (0,15) + NO + 2H2O
Cu (0,075) + 2Fe(NO3)3 (0,15) → 2Fe(NO3)2 + Cu(NO3)2
3Cu (0,075) + 8HNO3 (0,2) → 3Cu(NO3)2 + 2NO + 4H2O
Số mol HNO3 cần dùng là: 0,6 + 0,2 = 0,8 mol
Thể tích dung dịch HNO3 1M cần dùng là:
VHNO3 = 0,8/1 = 0,8 (l)
→ Đáp án C
Câu 141. Nung nóng 29 gam oxit sắt với khí CO dư, sau phản ứng, khối lượng chất rắn còn lại là 21 gam. Công thức oxit là
A. FeO B. Fe3O4
C. Fe2O3 D. FeO hoặc Fe3O4
Lời giải:
Gọi số mol CO tham gia phản ứng là x → số mol CO2 tạo thành là x mol
Vì lượng CO dư → chất rắn chỉ chứa Fe → nFe = 0,375 mol
Bảo toàn khối lượng → 29 + 28x = 44x + 21 → x = 0,5 mol → nO = 0,5
→ nFe : nO = 0,375 : 0,5 = 3:4 → Công thức của oxit sắt là Fe3O4
→ Đáp án B
Câu 142. Thể tích dung dịch HNO3 1M (loãng) ít nhất cần dùng để hòa tan hoàn toàn một hốn hợp gồm 0,15 mol Fe và 0,15 mol Cu là (biết phản ứng tạo chất khử duy nhất là NO)
A. 1,0 lít B. 0,6 lít
C. 0,8 lít D. 1,2 lít
Lời giải:
→ Đáp án C
Fe (0,15) + 4HNO3 (0,6) → Fe(NO3)3 (0,15) + NO + 2H2O
Cu (0,075) + 2Fe(NO3)3 (0,15) → 2Fe(NO3)2 + Cu(NO3)2
3Cu (0,075) + 8HNO3 (0,2) → 3Cu(NO3)2 + 2NO + 4H2O
Số mol HNO3 cần dùng là: 0,6 + 0,2 = 0,8 mol
Thể tích dung dịch HNO3 1M cần dùng là:
VHNO3 = 0,8/1 = 0,8 (l)
→ Đáp án C
Câu 143. Cho 18,5 gam hỗn hợp X gồm Fe và Fe3O4 tác dụng với 200ml dung dịch HNO3 loãng, đun nóng và khuấy đều. Sau khi phản ứng xảy ra hoàn toàn thu được 2,24 lít khí NO duy nhất (đktc), dung dịch Y và 1,46 gam kim loại. Nồng độ mol của dung dịch HNO3 là:
A. 2M B. 2,4M
C. 2,5M D. 3,2M
Lời giải:
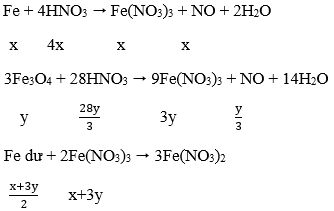
Ta có:
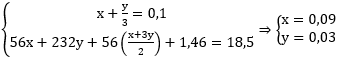
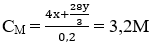
Câu 144. Khử hoàn toàn m gam hỗn hợp các oxit FeO, Fe2O3 và Fe3O4 thu được khí CO2 và Fe. Hấp thụ khí CO2 bằng nước vôi trong dư thu được a gam kết tủa. Hòa tan hoàn toàn Fe trong dung dịch HCl dư thu được V lít H2 (đktc). Mối liên hệ giữa m, V và a là:
A. m = 5V + 1,6a
B. m = 1,25V + 0,16a
C. m = 2,5V + 0,16a
D. m = 2,5V + 1,6a
Lời giải:
(FeO, Fe2O3, Fe3O4) + CO → Fe + CO2
CO2 + Ca(OH)2 dư → a gam ↓ CaCO3
Fe + HCl dư → V lít H2↑
• nFe = nH2 = V/22,4 mol; nCO = nCO2 = a/100 mol.
Theo bảo toàn khối lượng mhỗn hợp oxit = mFe + mCO2 - mCO
→ m = V/22,4 x 56 + a/100 x 44 - a/100 x 28 = 2,5V - 0,16a
→ Đáp án C
Câu 145. Dẫn từ từ V lít khí CO ở (đktc) đi qua một ống sứ đựng lượng dư hỗn hợp rắn gồm CuO, Fe2O3 (ở nhiệt độ cao). Sau khi các phản ứng xảy ra hoàn toàn, thu được khí X. Dẫn toàn bộ khí X ở trên vào lượng dư dung dịch Ca(OH)2 thì tạo thành 4 gam kết tủa. V có giá trị là:
A. 1,120 B. 0,896
C. 0,448 D. 0,224
Lời giải:
Ta có: nCaCO3 = 4/100 = 0,04 mol
Ca(OH)2 + CO2 (0,04) → CaCO3↓ (0,04) + H2O
Trong phản ứng khử CuO, Fe2O3 bằng CO, ta luôn có:
nCO = nCO2 = 0,04 mol
⇒ VCO = 0,04. 22,4 = 0,896 lít
→ Đáp án B
Câu 146. Điện phần 500ml dung dịch CuSO4 0,2M (điện cực trơ) cho đến khi catot thu được 3,2 gam kim loại thì thể tích khí (đktc) thu được ở anot là:
A. 3,36 lít B. 1,12 lít
C. 0,56 lít D. 2,24 lít
Lời giải:
Ta có: nCu = 0,05 mol < nCuSO4 = 0,1 mol → CuSO4 dư, catot chỉ có Cu2+ bị điện phân, ở anot nước bị điện phân.
Tại catot:
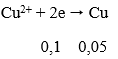
Tại anot:
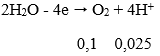
⇒ nO2 = 0,025 → VO2 = 0,56 lít
→ Đáp án C
Câu 147. Đun nóng m gam hỗn hợp Cu và Fe có tỉ lệ khối lượng tương ứng 7:3 với một lượng dung dịch HNO3. Khi các phản ứng kết thúc, thu được 0,75m gam chất rắn, dung dịch X và 5,6 lít hỗn hợp khí (đktc) gồm NO và NO2 (không có sản phẩm khử khác của N+5). Biết lượng HNO3 đã phản ứng là 44,1 gam. Giá trị của m là:
A. 448 B. 40,5
C. 33,6 D. 50,4
Lời giải:
Khối lượng Fe = 0,3m gam và khối lượng Cu = 0,7m gam
Sau phản ứng còn 0,75m gam → Fe chỉ phản ứng 0,25m gam; Fe dư vậy sau phản ứng chỉ thu được muối Fe2+.
Ta có: nHNO3 = 0,7; nNO + nNO2 = 0,25 mol; số mol của Fe(NO3)2 = 0,25m/56
Sơ đồ phản ứng:
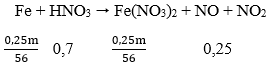
Áp dụng ĐLBT nguyên tố N ta có:
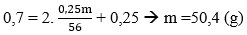
→ Đáp án D
Câu 148. Thổi một luồng khí CO dư qua ống sứ đựng m gam hỗn hợp gồm CuO, Fe2O3, FeO, Al2O3 nung nóng thu được 2,5 gam chất rắn. Toàn bộ khí thoát ra sục vào nước vôi trong dư thấy có 15 gam kết tủa trắng. Khối lượng của hỗn hợp oxit kim loại ban đầu là:
A. 7,4 gam B. 4,9 gam
C. 9,8 gam D. 23 gam
Lời giải:
Các phương trình hóa học:
MxOy + yCO -to→ xM + yCO2
Ca(OH)2 + CO2 → CaCO3 + H2O
Ta có: moxit = mkim loại + moxi
Trong đó: n[O] = nCO = nCO2 = nCaCO3 = 15/100 = 0,15 mol
moxit = 2,5 + 0,15.16 = 4,9 gam
→ Đáp án B
Câu 149. Nhúng một đinh sắt vào 150ml dung dịch CuSO4. Sau khi phản ứng xảy ra hoàn toàn, lấy đinh sắt sấy khô, thấy khối lượng tăng lên 1,2g. Vậy nồng độ ban đầu của CuSO4 là:
A. 1M B. 2,5M
C. 2M D. 0,5M
Lời giải:
Phương trình phản ứng:
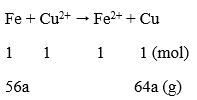
Ta có: Δm↑ = 64a - 56a = 1,2
a = 0,15 mol
CM (CuSO4) = 0,15/0,15 = 1M
⇒ Đáp án A
Câu 150. Hòa tan hỗn hợp gồm 0,1 mol Fe và a mol Cu vào dung dịch HNO3 loãng dư thu được 5,6 lít hỗn hợp NO và N2 (đktc) có tỷ khối hơi so với H2 là 14,5. Vậy a có giá trị là:
A. 0,6625 B. 0,6225
C. 0,0325 D. 0,165
Lời giải:
Gọi x, y là số mol của N2 và NO trong hỗn hợp.
Ta có:
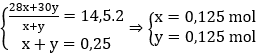
Quá trình cho electron
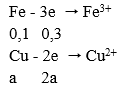
Quá trình nhận electron:
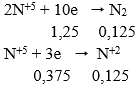
Ta có: ∑ne cho = ∑ne nhận → 0,3 + 2a = 1,25 + 0,375
→ a = 0,6625 mol
→ Đáp án A
Bài giảng: Bài tập sắt, hợp chất của sắt tác dụng với chất oxi hóa mạnh - Cô Nguyễn Thị Thu (Giáo viên VietJack)
Thi online Hóa 12 KNTTThi online Hóa 12 CDThi online Hóa 12 CTST
Xem thêm các dạng bài tập Hóa học lớp 12 ôn thi Tốt nghiệp có lời giải hay khác:
- 150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải (cơ bản – phần 1)
- 150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải (cơ bản – phần 2)
- 150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải (cơ bản – phần 3)
- 150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải (cơ bản – phần 4)
- 150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải (nâng cao – phần 1)
- 150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải (nâng cao – phần 2)
- 150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải (nâng cao – phần 3)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Lớp 12 Kết nối tri thức
- Soạn văn 12 (hay nhất) - KNTT
- Soạn văn 12 (ngắn nhất) - KNTT
- Giải sgk Toán 12 - KNTT
- Giải sgk Vật Lí 12 - KNTT
- Giải sgk Hóa học 12 - KNTT
- Giải sgk Sinh học 12 - KNTT
- Giải sgk Lịch Sử 12 - KNTT
- Giải sgk Địa Lí 12 - KNTT
- Giải sgk Giáo dục KTPL 12 - KNTT
- Giải sgk Tin học 12 - KNTT
- Giải sgk Công nghệ 12 - KNTT
- Giải sgk Hoạt động trải nghiệm 12 - KNTT
- Giải sgk Giáo dục quốc phòng 12 - KNTT
- Giải sgk Âm nhạc 12 - KNTT
- Giải sgk Mĩ thuật 12 - KNTT
- Lớp 12 Chân trời sáng tạo
- Soạn văn 12 (hay nhất) - CTST
- Soạn văn 12 (ngắn nhất) - CTST
- Giải sgk Toán 12 - CTST
- Giải sgk Vật Lí 12 - CTST
- Giải sgk Hóa học 12 - CTST
- Giải sgk Sinh học 12 - CTST
- Giải sgk Lịch Sử 12 - CTST
- Giải sgk Địa Lí 12 - CTST
- Giải sgk Giáo dục KTPL 12 - CTST
- Giải sgk Tin học 12 - CTST
- Giải sgk Hoạt động trải nghiệm 12 - CTST
- Giải sgk Âm nhạc 12 - CTST
- Lớp 12 Cánh diều
- Soạn văn 12 Cánh diều (hay nhất)
- Soạn văn 12 Cánh diều (ngắn nhất)
- Giải sgk Toán 12 Cánh diều
- Giải sgk Vật Lí 12 - Cánh diều
- Giải sgk Hóa học 12 - Cánh diều
- Giải sgk Sinh học 12 - Cánh diều
- Giải sgk Lịch Sử 12 - Cánh diều
- Giải sgk Địa Lí 12 - Cánh diều
- Giải sgk Giáo dục KTPL 12 - Cánh diều
- Giải sgk Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 - Cánh diều
- Giải sgk Giáo dục quốc phòng 12 - Cánh diều
- Giải sgk Âm nhạc 12 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

