30 Bài tập về Crom (Cr) cực hay, có lời giải chi tiết
Với 30 Bài tập về Crom (Cr) có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm Bài tập về Crom (Cr)
30 Bài tập về Crom (Cr) cực hay, có lời giải chi tiết
Thi online Hóa 12 KNTTThi online Hóa 12 CDThi online Hóa 12 CTST
Bài giảng: Bài tập tổng hợp về sắt và hợp chất của sắt - Cô Nguyễn Thị Thu (Giáo viên VietJack)
Bài 1: Cấu hình electron không đúng là (biết Cr có Z = 24)
A. Cr: [Ar] 3d5 4s1. B. Cr: [Ar] 3d4 4s2.
C. Cr2+: [Ar] 3d4. D. Cr3+: [Ar] 3d3.
Lời giải:
Đáp án: B
Ta có cấu hình electron của Cr: [Ar] 3d5 4s1
→ Cr2+: [Ar] 3d4
→ Cr3+: [Ar] 3d3.
Bài 2: Vị trí của Crom (z = 24) trong bảng tuần hoàn là
A. ô 24, chu kỳ 4, nhóm VIA.
B. ô 24, chu kỳ 4, nhóm VIB.
C. ô 24, chu kỳ 4, nhóm IB.
D. ô 24, chu kỳ 4, nhóm IIB.
Lời giải:
Đáp án: B
Ta có cấu hình electron của Cr: [Ar] 3d5 4s1
→ Crom ở ô thứ 24 do z = 24, chu kỳ 4 do có 4 lớp electron, nhóm VIB do có 6 electron hóa trị, nguyên tố d.
Bài 3: Các số oxi hóa phổ biến của crom trong hợp chất là
A. +2, +4 và +6. B. +2, +3 và +6.
C. +1, +3 và +6. D. +3, +4 và +6.
Lời giải:
Đáp án: B
Trong hợp chất Cr có số oxi hóa biến đổi từ + 1 đến +6, trong đó phổ biến nhất là các số oxi hóa +2, +3 và +6.
Bài 4: Nhận xét nào không đúng về tính chất vật lý của crom?
A. Crom có màu trắng ánh bạc.
B. Crom cứng nhất trong số các kim loại.
C. Crom khó nóng chảy.
D. Crom là kim loại nhẹ.
Lời giải:
Đáp án: D
Crom là kim loại nặng.
Bài 5: Nhận định nào sau đây là đúng?
A. Crom có tính khử mạnh hơn sắt.
B. Crom chỉ tạo được basic oxide.
C. Trong tự nhiên, crom có ở dạng đơn chất.
D. Phương pháp thường dùng để điều chế crom là điện phân Cr2O3.
Lời giải:
Đáp án: A
B sai vì crom có thể tạo oxit lưỡng tính.
C sai vì trong tự nhiên crom chỉ có ở dạng hợp chất.
D sai vì phương pháp thường dùng để điều chế crom là phương pháp nhiệt nhôm.
Bài 6: Ứng dụng nào sau đây không phải của crom?
A. Crom là kim loại rất cứng có thể dùng để cắt thủy tinh.
B. Crom dùng để tạo thép cứng, không gỉ, chịu nhiệt.
C. Crom là kim loại nhẹ, được sử dụng tạo các hợp kim của ngành hàng không.
D. Điều kiện thường, crom tạo lớp màng oxit mịn, bền được dùng để mạ bảo vệ thép.
Lời giải:
Đáp án: C
Crom là kim loại nặng.
Bài 7: Kim loại không tác dụng với nước ở nhiệt độ thường là
A. Al và Ba. B. Mg và Ca.
C. Cr và Sr. D. Cr và Be.
Lời giải:
Đáp án: D
Cr và Be không tác dụng với nước ở nhiệt độ thường.
Bài 8: Ở nhiệt độ thường, crom có cấu trúc mạng tinh thể là
A. lập phương tâm diện. B. lập phương.
C. lập phương tâm khối. D. lục phương.
Lời giải:
Đáp án: C
Crom có cấu trúc mạng tinh thể lập phương tâm khối.
Bài 9: Hiện nay, từ quặng cromit người ta điều chế Cr bằng phương pháp nào?
A. Tách quặng rồi thực hiện điện phân nóng chảy Cr2O3.
B. Tách quặng rồi thực hiện phản ứng nhiệt nhôm Cr2O3.
C. Tách quặng rồi thực hiện phản ứng khử Cr2O3 bởi CO.
D. hòa tan quặng bằng HCl rồi điện phân dung dịch CrCl3.
Lời giải:
Đáp án: B
Cr2O3 được tách ra từ quặng, sau đó thực hiện phản ứng nhiệt nhôm để điều chế Cr.
Bài 10: Cr không phản ứng với axit nào sau đây?
A. HCl loãng, nóng. B. H2SO4 loãng, nóng.
C. H2SO4 đặc, nóng. D. H2SO4 đặc, nguội.
Lời giải:
Đáp án: D
Cr thụ động trong H2SO4 đặc, nguội.
Bài 11: Quặng phổ biến nhất của crom là?
A. Pirit. B. Canxit.
C. Cromit. D. Đolomit.
Lời giải:
Đáp án: D
Quặng phổ biến nhất của crom là cromit.
Bài 12: Đốt cháy hoàn toàn bột crom trong oxi dư thu được 4,56 gam một oxit duy nhất. Khối lượng crom bị đốt cháy là
A. 0,78g. B. 3,12g.
C. 1,74g. D. 1,19g.
Lời giải:
Đáp án: B
4Cr (0,06) + 3O2 → 2Cr2O3 (0,03 mol)
→ mCr = 0,06.52 = 3,12 gam.
Bài 13: Hòa tan hết 2,16 gam hỗn hợp Cr và Fe trong dung dịch HCl đun nóng thu được 896 ml khí ở đktc. Khối lượng crom trong hỗn hợp ban đầu là
A. 0,065g. B. 1,040g.
C. 0,560g. D. 1,015g.
Lời giải:
Đáp án: B
Gọi số mol của Cr và Fe lần lượt là x và y mol
→ 52x + 56y = 2,16
PTHH:
Cr (x) + 2HCl → CrCl2 + H2 (x mol)
Fe (y) + 2HCl → FeCl2 + H2 (y mol)
nkhí = x + y = 0,04
Giải hệ phương trình được x = y = 0,02.
Vậy mCr = 0,02.52 = 1,04 gam.
Bài 14: Trong số các cặp kim loại sau đây, cặp nào bền vững trong môi trường không khí và nước nhờ có màng oxit bảo vệ?
A. Cu và Al. B. Al và Cr.
C. Fe và Al. D. Fe và Cr.
Lời giải:
Đáp án: B
Al và Cr bền vững trong môi trường không khí và nước do có màng oxit bảo vệ.
Bài 15: Cho m gam Cr tác dụng hoàn toàn với dung dịch HCl nóng, dư thu được 6,72 lít khí H2 (đktc). Giá trị của m là
A. 7,8 gam B. 15,6 gam
C. 10,4 gam D. 5,2 gam.
Lời giải:
Đáp án: B
Cr (0,3) + 2HCl → CrCl2 + H2 (0,3 mol)
→ m = 0,3.52 = 15,6 gam.
Bài 16: Dung dịch HCl, H2SO4 loãng sẽ oxi hóa crom đến mức oxi hóa nào?
A. +2. B. +6.
C. +3. D. +4.
Lời giải:
Đáp án: A
Cr + 2HCl → CrCl2 + H2
Cr + H2SO4 → CrSO4 + H2
Sau phản ứng Cr có số oxi hóa +2.
Bài 17: Cho 5,2g Cr tác dụng với HNO3 loãng dư thu được V lít khí NO (đktc, sản phẩm khử duy nhất). V có giá trị là
A. 2,24. B. 3,36.
C. 4,48. D. 6,72.
Lời giải:
Đáp án: A
Cr (0,1) + 4HNO3 → Cr(NO3)3 + NO (0,1 mol) + 2H2O
V = 0,1.22,4 = 2,24 lít.
Bài 18: Cho 100 gam hợp kim của Fe, Cr, Al tác dụng với dung dịch NaOH dư thoát ra 5,04 lít khí (đktc) và một phần rắn không tan. Lọc lấy phần không tan đem hòa tan hết bằng dung dịch HCl nóng, dư thấy thoát ra 38,8 lít khí (đktc). Phần trăm khối lượng các chất trong hợp kim là
A. 13,66% Al; 82,29% Fe và 4,05% Cr.
B. 4,05% Al; 83,66% Fe và 12,29% Cr.
C. 4,05% Al; 82,29% Fe và 13,66% Cr.
D. 4,05% Al; 13,66% Fe và 82,29% Cr.
Lời giải:
Đáp án:
Gọi số mol Fe, Cr và Al lần lượt là x, y và z mol
→ 56x + 52y + 27z = 100 (1)
Cho hợp kim tác dụng với NaOH chỉ có Al phản ứng:
2Al (0,15) + 2NaOH + 2H2O → 2NaAlO2 + 3H2 (0,225 mol)
→ z = 0,15
Sau phản ứng còn Fe, Cr cho vào HCl nóng, dư có phản ứng
Cr (y) + 2HCl → CrCl2 + H2 (y mol)
Fe (x) + 2HCl → FeCl2 + H2 (x mol)
→ x + y = 1,7321
Giải hệ pt được x = 1,4702; y = 0,2691; z = 0,15.
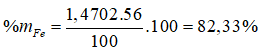
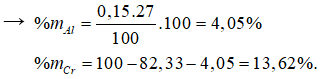
Bài 19: Dãy kim loại bị thụ động trong axit HNO3 đặc, nguội là
A. Fe, Al và Cr. B. Fe, Al và Zn.
C. Mg, Al và Cu. D. Fe, Zn và Cr.
Lời giải:
Đáp án: A
Fe, Al và Cr bị thụ động trong HNO3 đặc nguội.
Bài 20: Cho 10,8 g hỗn hợp Cr và Fe tác dụng hoàn toàn với dung dịch HCl nóng, dư thu được 4,48 lít khí (đktc). Tổng khối lượng muối thu được trong dung dịch sau phản ứng là
A. 18,7g. B. 25,0g.
C. 19,7g. D. 16,7g.
Lời giải:
Đáp án: B
Bảo toàn H có nHCl = 2.nkhí = 2.0,2 = 0,4 mol
Áp dụng định luật bảo toàn khối lượng ta có:
mKL + maxit = mmuối + mkhí
→ mmuối = 10,8 + 0,4.36,5 – 0,2.2 = 25 gam.
Bài giảng: Bài tập sắt, hợp chất của sắt tác dụng với chất oxi hóa mạnh - Cô Nguyễn Thị Thu (Giáo viên VietJack)
Thi online Hóa 12 KNTTThi online Hóa 12 CDThi online Hóa 12 CTST
Xem thêm các dạng bài tập Hóa học lớp 12 ôn thi Tốt nghiệp có lời giải hay khác:
- Bài tập về Đồng (Cu) và hợp chất của đồng cực hay, có lời giải chi tiết
- Bài tập về Hợp chất của Crom cực hay, có lời giải chi tiết
- Bài tập về Hợp chất của Sắt cực hay, có lời giải chi tiết
- Bài tập về Niken (Ni), Kẽm (Zn), Thiếc (Sn), Chì (Pb) cực hay, có lời giải chi tiết
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Lớp 12 Kết nối tri thức
- Soạn văn 12 (hay nhất) - KNTT
- Soạn văn 12 (ngắn nhất) - KNTT
- Giải sgk Toán 12 - KNTT
- Giải sgk Vật Lí 12 - KNTT
- Giải sgk Hóa học 12 - KNTT
- Giải sgk Sinh học 12 - KNTT
- Giải sgk Lịch Sử 12 - KNTT
- Giải sgk Địa Lí 12 - KNTT
- Giải sgk Giáo dục KTPL 12 - KNTT
- Giải sgk Tin học 12 - KNTT
- Giải sgk Công nghệ 12 - KNTT
- Giải sgk Hoạt động trải nghiệm 12 - KNTT
- Giải sgk Giáo dục quốc phòng 12 - KNTT
- Giải sgk Âm nhạc 12 - KNTT
- Giải sgk Mĩ thuật 12 - KNTT
- Lớp 12 Chân trời sáng tạo
- Soạn văn 12 (hay nhất) - CTST
- Soạn văn 12 (ngắn nhất) - CTST
- Giải sgk Toán 12 - CTST
- Giải sgk Vật Lí 12 - CTST
- Giải sgk Hóa học 12 - CTST
- Giải sgk Sinh học 12 - CTST
- Giải sgk Lịch Sử 12 - CTST
- Giải sgk Địa Lí 12 - CTST
- Giải sgk Giáo dục KTPL 12 - CTST
- Giải sgk Tin học 12 - CTST
- Giải sgk Hoạt động trải nghiệm 12 - CTST
- Giải sgk Âm nhạc 12 - CTST
- Lớp 12 Cánh diều
- Soạn văn 12 Cánh diều (hay nhất)
- Soạn văn 12 Cánh diều (ngắn nhất)
- Giải sgk Toán 12 Cánh diều
- Giải sgk Vật Lí 12 - Cánh diều
- Giải sgk Hóa học 12 - Cánh diều
- Giải sgk Sinh học 12 - Cánh diều
- Giải sgk Lịch Sử 12 - Cánh diều
- Giải sgk Địa Lí 12 - Cánh diều
- Giải sgk Giáo dục KTPL 12 - Cánh diều
- Giải sgk Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 - Cánh diều
- Giải sgk Giáo dục quốc phòng 12 - Cánh diều
- Giải sgk Âm nhạc 12 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

