Muối sulfate là gì (chi tiết nhất)
Bài viết Muối sulfate là gì lớp 11 chi tiết nhất là kiến thức có trong chương trình Hóa học 11 giúp học sinh nắm vững kiến thức trọng tâm về Muối sulfate.
Muối sulfate là gì (chi tiết nhất)
1. Muối sulfate là gì?
Muối sulfate là muối được tạo bởi ion kim loại với gốc sulfate ()
Vd: CuSO4, MgSO4,...
2. Kiến thức mở rộng
2.1. Ứng dụng
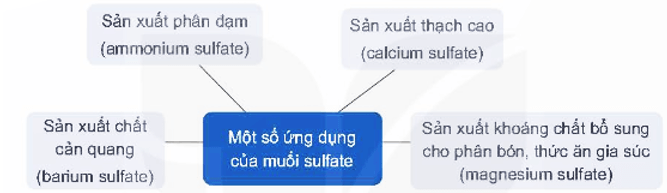
Một số ứng dụng của muối sulfate được thể hiện trong sơ đồ sau:
2.2 Nhận biết
Thuốc thử nhận biết ion sulfate là dung dịch muối barium hoặc dung dịch Ba(OH)2. Sản phẩm phản ứng là barium sulfate BaSO4 kết tủa trắng, không tan trong acid.
H2SO4 + BaCl2 →BaSO4↓ + 2HCl
Na2SO4 + Ba(OH)2 →BaSO4↓ + 2NaOH
Kết tủa trắng BaSO4
3. Bài tập minh họa
Câu 1: Phân biệt được dung dịch Na2SO4 và NaCl bằng dung địch nào sau đây?
A. MgCl2.
B. FeCl2.
C. HCl.
D. BaCl2.
Hướng dẫn giải
Đáp án đúng là: D
Hiện tượng: Ống đựng Na2SO4 xuất hiện kết tủa trắng BaSO4.
PTHH: BaCl2 + Na2SO4 → BaSO4↓ + 2NaCl
Câu 2: Cho các phát biểu sau:
(a) Sulfuric acid đặc có tính háo nước, gây bỏng nặng khi tiếp xúc với da tay.
(b) Khi pha loãng sulfuric acid đặc cần cho từ từ nước vào acid, không làm ngược lại gây nguy hiểm.
(c) Khi bị bỏng sulfuric acid đặc, điều đầu tiên cần làm là xả nhanh chỗ bỏng với nước lạnh.
(d) Sulfuric acid loãng có tính oxi hóa mạnh, khi tác dụng với kim loại không sinh ra khí hydrogen.
(e) Thuốc thử nhận biết sulfuric acid và muối sulfate là ion Ba2+ trong BaCl2, Ba(OH)2, Ba(NO3)2.
Số phát biểu đúng là
A. 1.
B. 2.
C. 3.
D. 4.
Hướng dẫn giải
Đáp án đúng là: C
(b) sai vì khi pha loãng sulfuric acid đặc cần cho từ từ acid vào nước, không làm ngược lại gây nguy hiểm.
(d) sai vì sulfuric acid loãng có tính acid mạnh, khi tác dụng với kim loại sinh ra khí hydrogen.
Câu 3: Muối X không tan trong nước và các dung môi hữu cơ. Trong y học, X thường được dùng làm chất cản quang trong xét nghiệm X-quang đường tiêu hoá. Công thức của X là
A. BaSO4.
B. Na2SO4.
C. K2SO4.
D. MgSO4.
Hướng dẫn giải
Đáp án đúng là: A
BaSO4 là muối sunfate không tan trong nước, acid và các dung môi hữu cơ; được ứng dụng làm chất cản quang trong xét nghiệm X-quang.
Câu 4: Kết quả phân tích thành phần một muối sulfate cho thấy nguyên tố kim loại M chiếm 28% về khối lượng, còn lại là oxygen và lưu huỳnh. Kim loại M là
A. Fe.
B. Cu.
C. Mg.
D. Ca.
Hướng dẫn giải
Đáp án đúng là: A
Gọi muối sulfate có công thức Mn(SO4)m, ta có:
. Chọn được n = 2, m = 3, M = 56 ⟹ M là Fe.
Câu 5: Hoà tan hết m gam oxide của kim loại M (hoá trị II) vào dung dịch H2SO4 loãng, thu được 3m gam muối sulfate. Công thức của oxide kim loại là
A. ZnO.
B. CuO.
C. CaO.
D. MgO.
Hướng dẫn giải
Đáp án đúng là: D
MO + H2SO4 → MSO4 + H2O
Mol: a a a
Theo định luật bảo toàn khối lượng có: 80.a = 2m (g)
⟹ M = 24. M là Mg
Câu 6: Cho những phát biểu sau
(a) Nhiều muối sulfate tan tốt trong nước nhưng một số muối như CaSO4, BaSO4 rất ít tan trong nước.
(b) Magnesium sulfate được dùng làm thuốc điều trị bệnh liên quan đến hồng cầu, dùng làm chất hút mồ hôi tay cho các vận động viên,…
(c) Calcium sulfate là thành phần chính của các loại thạch cao. Phân tử chất này thường ngậm nước với số lượng các phân tử H2O khác nhau, tạo ra các loại thạch cao có ứng dụng khác nhau.
(d) Barium sulfate là chất rắn màu trắng, hầu như không tan trong nước. Chất này được dùng tạo màu trắng cho các loại giấy chất lượng cao.
Số phát biểu đúng là
A. 1.
B. 2.
C. 3.
D. 4.
Hướng dẫn giải
Đáp án đúng là: C
Các phát biểu đúng là (a), (c), (d).
Phát biểu (b) sai vì magnesium sulfate chủ yếu được sử dụng để làm phân bón, làm thuốc để giảm các cơn đau cơ, hiện tượng co cơ …
Câu 7: Muối nào sau đây được sử dụng để sản xuất phân đạm
A. BaSO4.
B. (NH4)2SO4.
C. K2SO4.
D. MgSO4.
Hướng dẫn giải
Đáp án đúng là: B
Muối được sử dụng để sản xuất phân đạm là (NH4)2SO4.
Câu 8: Muối nào sau đây được sử dụng để sản xuất khoáng chất bổ sung cho phân bón, thức ăn gia súc
A. BaSO4.
B. (NH4)2SO4.
C. K2SO4.
D. MgSO4.
Hướng dẫn giải
Đáp án đúng là: D
Muối được sử dụng để sản xuất khoáng chất bổ sung cho phân bón, thức ăn gia súc là MgSO4.
Xem thêm các bài viết về định nghĩa & khái niệm môn Hóa học hay, chi tiết khác:
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Lớp 12 Kết nối tri thức
- Soạn văn 12 (hay nhất) - KNTT
- Soạn văn 12 (ngắn nhất) - KNTT
- Giải sgk Toán 12 - KNTT
- Giải sgk Vật Lí 12 - KNTT
- Giải sgk Hóa học 12 - KNTT
- Giải sgk Sinh học 12 - KNTT
- Giải sgk Lịch Sử 12 - KNTT
- Giải sgk Địa Lí 12 - KNTT
- Giải sgk Giáo dục KTPL 12 - KNTT
- Giải sgk Tin học 12 - KNTT
- Giải sgk Công nghệ 12 - KNTT
- Giải sgk Hoạt động trải nghiệm 12 - KNTT
- Giải sgk Giáo dục quốc phòng 12 - KNTT
- Giải sgk Âm nhạc 12 - KNTT
- Giải sgk Mĩ thuật 12 - KNTT
- Lớp 12 Chân trời sáng tạo
- Soạn văn 12 (hay nhất) - CTST
- Soạn văn 12 (ngắn nhất) - CTST
- Giải sgk Toán 12 - CTST
- Giải sgk Vật Lí 12 - CTST
- Giải sgk Hóa học 12 - CTST
- Giải sgk Sinh học 12 - CTST
- Giải sgk Lịch Sử 12 - CTST
- Giải sgk Địa Lí 12 - CTST
- Giải sgk Giáo dục KTPL 12 - CTST
- Giải sgk Tin học 12 - CTST
- Giải sgk Hoạt động trải nghiệm 12 - CTST
- Giải sgk Âm nhạc 12 - CTST
- Lớp 12 Cánh diều
- Soạn văn 12 Cánh diều (hay nhất)
- Soạn văn 12 Cánh diều (ngắn nhất)
- Giải sgk Toán 12 Cánh diều
- Giải sgk Vật Lí 12 - Cánh diều
- Giải sgk Hóa học 12 - Cánh diều
- Giải sgk Sinh học 12 - Cánh diều
- Giải sgk Lịch Sử 12 - Cánh diều
- Giải sgk Địa Lí 12 - Cánh diều
- Giải sgk Giáo dục KTPL 12 - Cánh diều
- Giải sgk Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 - Cánh diều
- Giải sgk Giáo dục quốc phòng 12 - Cánh diều
- Giải sgk Âm nhạc 12 - Cánh diều







 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

