Tinh chế kim loại là gì (chi tiết nhất)
Bài viết Tinh chế kim loại là gì lớp 12 chi tiết nhất là kiến thức có trong chương trình Hóa học 12 giúp học sinh nắm vững kiến thức trọng tâm về Tinh chế kim loại.
Tinh chế kim loại là gì (chi tiết nhất)
1. Tinh chế kim loại là gì?
- Từ nguồn kim loại thô (kim loại phế liệu hoặc sau quá trình nhiệt luyện, thuỷ luyện), các kim loại như Zn, Ni, Co, Cu, Ag, Au, ... được tinh chế bằng phương pháp điện phân.
2. Kiến thức mở rộng Tinh chế kim loại là gì
2.1. Khái niệm điện phân
- Điện phân là một quá trình oxi hoá - khử xảy ra tại các điện cực khi có dòng điện một chiều với hiệu điện thế đủ lớn đi qua chất điện li nóng chảy hoặc dung dịch chất điện li.
- Phản ứng oxi hoá - khử xảy ra trong quá trình điện phân là phản ứng không tự xảy ra mà phải nhờ tác động của điện năng để gây ra phản ứng đó.
- Các chất tham gia vào quá trình điện phân có thể ở trạng thái nóng chảy (điện phân nóng chảy) hoặc dung dịch (điện phân dung dịch). Trong quá trình điện phân, dưới tác dụng của điện trường, các ion âm sẽ di chuyển về điện cực dương, các ion dương sẽ di chuyển về điện cực âm.
- Khi điện phân dung dịch, nước cũng có thể tham gia điện phân với vai trò chất khử (2H2O → O2 + 4H+ + 4e) hoặc chất oxi hoá (2H2O + 2e → H2 + 2OH-).
- Theo quy ước chung, đối với cả pin điện và bình điện phân, tại cathode xảy ra quá trình khử và tại anode xảy ra quá trình oxi hoá. Do vậy, trong điện phân cathode là cực âm, anode là cực dương.
- Ví dụ: Sodium chloride (NaCl) nóng chảy điện li thành các ion Na+ và Cl− chuyển động tự do. Trong điện trường, các ion sẽ di chuyển về các cực trái dấu. Ở một hiệu điện thế đủ lớn, trên bề mặt các điện cực xảy ra các quá trình:
|
Cực âm (cathode) |
Quá trình khử ion Na+ |
Na+ + 1e → Na |
|
Cực dương (anode) |
Quá trình oxi hoá ion Cl− |
Phương trình hoá học của phản ứng điện phân NaCl nóng chảy:
2.2. Nguyên tắc tinh chế kim loại
- Các kim loại như Zn, Ni, Co, Cu, Ag, Au,… được tinh chế bằng phương pháp điện phân.
- Quá trình tinh chế được thực hiện bằng cách điện phân dung dịch chất tan (muối hoặc phức chất) của kim loại đó với anode làm bằng kim loại thô tương ứng:
+ Anode: Kim loại bị oxi hóa thành ion kim loại, đi vào dung dịch ⇒ Anode dần bị hòa tan.
+ Cathode: Ion kim loại bị khử thành kim loại, bám trên cathode.
- Kết thúc quá trình điện phân thu được kim loại tinh khiết ở cathode.
⇒ Sự chuyển dời kim loại từ anode (ở dạng kim loại thô) về cathode (ở dạng kim loại tinh khiết).
3. Bài tập minh họa Tinh chế kim loại là gì
Câu 1. Trong công nghiệp, việc tinh chế đồng từ đồng thô được thực hiện bằng phương pháp điện phân dung dịch với anode làm bằng
A. graphite.
B. platinum.
C. thép.
D. đồng thô.
Hướng dẫn giải
Đáp án đúng là: D
Trong công nghiệp, việc tinh chế đồng từ đồng thô được thực hiện bằng phương pháp điện phân dung dịch với anode làm bằng đồng thô. Do anode sẽ tan vào dung dịch (gọi là hiện tượng dương cực tan).
Câu 2. Cho các phát biểu sau:
a. Điện phân dung dịch Na2SO4 bão hòa với điện cực trơ, thu được khí O2 ở anode.
b. Thứ tự điện phân tại anode:
c. Thứ tự điện phân tại cathode:
d. Từ nguồn kim loại thô, các kim loại như Zn, Ni, Co, Cu, Ag ... được tinh chế bằng phương pháp điện phân.
Số phát biểu đúng là
A. 1.
B. 2.
C. 3.
D. 4.
Hướng dẫn giải
Đáp án đúng là: B
Bao gồm: a, d.
a. Đúng vì Na2SO4 + 2H2O H2 + 2O2 + 2NaOH.
b. Sai vì F- không bị điện phân.
c. Sai vì thứ tự đúng như sau:
d. Đúng.
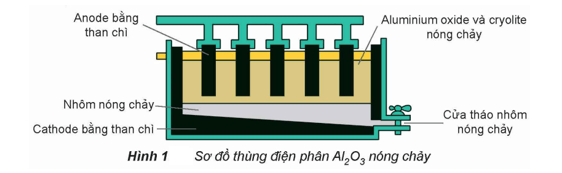
Câu 3. Trong công nghiệp, nhôm được sản xuất từ quặng bauxite theo hai giai đoạn chính:
Giai đoạn 1: Tinh chế quặng bauxite.
Giai đoạn 2: Điện phân Al2O3 nóng chảy.
Cho các nhận định sau:
a. Tại cathode xảy ra quá trình khử, tại anode xảy ra quá trình oxi hóa ion .
b. Thành phần chính của quặng bauxite là Al2O3.2H2O.
c. Có thể thay điện cực thay điện cực than chì bằng điện cực Ag hoặc Cu để dẫn điện tốt hơn.
d. Cryolite có công thức Na3AlF6.
Số nhận định đúng là
A. 1.
B. 2.
C. 3.
D. 4.
Hướng dẫn giải
Đáp án đúng là: C
Bao gồm: a, b, d.
Quặng bauxite (Al2O3.2H2O) được trộn cùng với cryolite (Na3AlF6) để tạo thành hỗn hợp nóng chảy.
Ở anode xảy ra quá trình oxi hóa thành O2. Ở cathode xảy ra quá trình khử thành Al.
c. Sai vì Ag và Cu tham gia phản ứng trong quá trình điện phân nóng chảy Al2O3, tạo ra sản phẩm phụ.
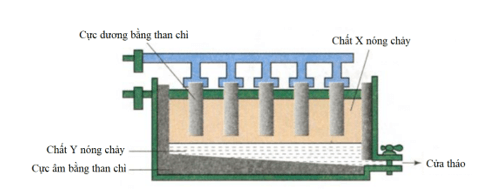
Câu 4. Kim loại nhôm được sản xuất trong công nghiệp bằng phương pháp điện phân nóng chảy aluminium oxide (Al2O3), điện cực than chì, khi có mặt cryolite(Na3AlF6) nóng chảy theo sơ đồ sau:
Cho các phát biểu:
a. Chất X là Aluminium nóng chảy
b. Ở anode, xảy ra quá trình: 2O2- → O2 + 4e
c. Phương pháp điện phân với anode tan được dùng để tinh chế một số kim loại như Cu, Ag,…
d. Ở nhiệt độ cao, điện cực than chì sẽ tác dụng với Oxygen tạo thành Carbon monoxide
Số phát biểu đúng là
A. 1.
B. 2.
C. 3.
D. 4.
Hướng dẫn giải
Đáp án đúng là: B
a. Sai vì Chất X là Aluminium oxide (Al2O3) và cryolite (Na3AlF6) nóng chảy.
b. Đúng
c. Đúng
d. Sai vì Ở nhiệt độ cao, điện cực than chì sẽ tác dụng với Oxygen tạo thành Carbon dioxide (CO2).
Câu 5. Trong quá trình điện phân KCl nóng chảy với các điện cực trơ, ở cathode xảy ra quá trình
A. oxi hóa ion K+.
B. khử ion K+.
C. oxi hóa ion Cl–.
D. khử ion Cl–.
Hướng dẫn giải
Đáp án đúng là: B
Trong quá trình điện phân KCl nóng chảy với các điện cực trơ, ở cathode xảy ra quá trình khử ion K+ thành kim loại K, ở anode xảy ra quá trình oxi hóa ion thành khí Cl2.
Câu 6. Phản ứng hóa học chính xảy ra trong quá trình điện phân nóng chảy Al2O3 trong 3NaF.AlF3 là
A. 2AlF3 → 2Al + 3F2.
B. 2NaF → Na + F2.
C. 2H2O → 2H2 + O.
D. 2Al2O3 → 4Al + 3O2.
Hướng dẫn giải
Đáp án đúng là: D
Phản ứng hóa học chính xảy ra trong quá trình điện phân nóng chảy Al2O3 trong 3NaF.AlF3 là: 2Al2O3 → 4Al + 3O2.
Câu 7. Dung dịch X chứa hỗn hợp các muối: MgCl2, CuCl2, FeCl2 và KCl. Kim loại tách ra đầu tiên ở cathode khi điện phân dung dịch là
A. Cu. .
B. Mg.
C. K.
D. Fe.
Hướng dẫn giải
Đáp án đúng là: A
Do Cu2+ có tính oxi hóa mạnh nhất trong các ion kim loại trên nên sẽ bị khử đầu tiên, tách ra đầu tiên ở cathode khi điện phân dung dịch.
Xem thêm các bài viết về định nghĩa & khái niệm môn Hóa học hay, chi tiết khác:
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Lớp 12 Kết nối tri thức
- Soạn văn 12 (hay nhất) - KNTT
- Soạn văn 12 (ngắn nhất) - KNTT
- Giải sgk Toán 12 - KNTT
- Giải sgk Vật Lí 12 - KNTT
- Giải sgk Hóa học 12 - KNTT
- Giải sgk Sinh học 12 - KNTT
- Giải sgk Lịch Sử 12 - KNTT
- Giải sgk Địa Lí 12 - KNTT
- Giải sgk Giáo dục KTPL 12 - KNTT
- Giải sgk Tin học 12 - KNTT
- Giải sgk Công nghệ 12 - KNTT
- Giải sgk Hoạt động trải nghiệm 12 - KNTT
- Giải sgk Giáo dục quốc phòng 12 - KNTT
- Giải sgk Âm nhạc 12 - KNTT
- Giải sgk Mĩ thuật 12 - KNTT
- Lớp 12 Chân trời sáng tạo
- Soạn văn 12 (hay nhất) - CTST
- Soạn văn 12 (ngắn nhất) - CTST
- Giải sgk Toán 12 - CTST
- Giải sgk Vật Lí 12 - CTST
- Giải sgk Hóa học 12 - CTST
- Giải sgk Sinh học 12 - CTST
- Giải sgk Lịch Sử 12 - CTST
- Giải sgk Địa Lí 12 - CTST
- Giải sgk Giáo dục KTPL 12 - CTST
- Giải sgk Tin học 12 - CTST
- Giải sgk Hoạt động trải nghiệm 12 - CTST
- Giải sgk Âm nhạc 12 - CTST
- Lớp 12 Cánh diều
- Soạn văn 12 Cánh diều (hay nhất)
- Soạn văn 12 Cánh diều (ngắn nhất)
- Giải sgk Toán 12 Cánh diều
- Giải sgk Vật Lí 12 - Cánh diều
- Giải sgk Hóa học 12 - Cánh diều
- Giải sgk Sinh học 12 - Cánh diều
- Giải sgk Lịch Sử 12 - Cánh diều
- Giải sgk Địa Lí 12 - Cánh diều
- Giải sgk Giáo dục KTPL 12 - Cánh diều
- Giải sgk Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 - Cánh diều
- Giải sgk Giáo dục quốc phòng 12 - Cánh diều
- Giải sgk Âm nhạc 12 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

