Cách nhận biết muối sunfit không tan trong nước nhanh nhất
Muối sunfit là muối của sulfurous acid. Các bài tập về muối sunfit cũng khá đa dạng và hay gặp trong các đề thi. Bài viết sau đây, sẽ hướng dẫn các em nhận biết muối sunfit không tan.
Cách nhận biết muối sunfit không tan trong nước
I. Cách nhận biết muối sunfit không tan trong nước
- Các muối thường gặp: CaSO3, MgSO3, BaSO3.
- Cách nhận biết: Cho tác dụng với axit như HCl, H2SO4 loãng…
- Hiện tượng: Sủi bọt khí SO2.
Ví dụ:
BaSO3 + 2HCl → BaCl2 + SO2↑ + H2O
Lưu ý: Ta có thể phân biệt được muối MgSO3 với BaSO3 khi cho tác dụng với dung dịch axit H2SO4 loãng, dư.
Hiện tượng:
Chất rắn tan thu được dung dịch và sủi bọt khí: MgSO3
Thấy sủi bọt khí, sau phản ứng vẫn còn kết tủa trắng: BaSO3
Phương trình:
MgSO3 + H2SO4 → MgSO4 + SO2↑ + H2O
BaSO3 + H2SO4 → BaSO4↓ + SO2↑ + H2O
II. Mở rộng
Các muối sunfit không tan thì bị nhiệt phân hủy tạo thành basic oxide và SO2.
Ví dụ:
BaSO3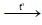 BaO + SO2↑
BaO + SO2↑
III. Bài tập nhận biết muối sunfit không tan
Bài 1: Bằng phương pháp hóa học, hãy nhận biết các chất rắn đựng trong các lọ mất nhãn sau: BaSO3; MgSO3; Na2SO3.
Hướng dẫn giải:
- Đánh số thứ tự từng lọ mất nhãn, trích mỗi lọ một ít sang ống nghiệm đánh số tương ứng (trích mẫu thử).
- Cho các mẫu thử vào nước và khuấy đều.
+ Mẫu thử tan hoàn toàn: Na2SO3.
+ Mẫu thử không tan: BaSO3 và MgSO3 (nhóm I)
- Cho các mẫu thử ở nhóm I phản ứng hết với lượng dư H2SO4.
+ Chất rắn tan hết tạo dung dịch đồng nhất và sủi bọt khí: MgSO3
MgSO3 + H2SO4 → MgSO4 + SO2↑ + H2O
+ Thấy sủi bọt khí, vẫn còn kết tủa sau khi phản ứng kết thúc: BaSO3
BaSO3 + H2SO4 → BaSO4↓ + SO2↑ + H2O
- Dán nhãn các chất đã nhận biết.
Bài 2: Khi cho khí SO2 vào lượng dư các dung dịch Ca(OH)2, Ba(OH)2, NaOH, NaCl. Số trường hợp thu được kết tủa là:
A. 1
B. 2
C. 3
D. 4
Hướng dẫn giải:
SO2 + Ca(OH)2 dư → CaSO3↓ + H2O
SO2 + Ba(OH)2 dư → BaSO3↓ + H2O
SO2 + 2NaOH dư → Na2SO3 + H2O
SO2 + NaCl → không phản ứng.
→ Chỉ có hai trường hợp sinh ra kết tủa.
→ Đáp án B
Xem thêm cách nhận biết các chất hóa học nhanh, chi tiết khác:
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)








 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



