Đồng vị của Manganese (Mn) (chi tiết nhất)
Bài viết đồng vị của Manganese hay đồng vị của Mn chi tiết nhất giúp học sinh các cấp có thêm thông tin về đồng vị của Mn từ đó học tốt môn Hóa hơn.
Đồng vị của Manganese (Mn) (chi tiết nhất)
Mỗi nguyên tố hóa học đều có nhiều đồng vị, bài viết sau sẽ cung cấp cho các em kiến thức về đồng vị của manganese.
I. Đồng vị của Manganese
- Manganese chỉ có 1 đồng vị bền, ổn định, được tìm thấy trong tự nhiên với hàm lượng như sau:
|
Đồng vị |
Nguồn tự nhiên |
Chu kỳ bán rã |
Kiểu phân rã |
Năng lượng phân rã (MeV) |
Sản phẩm phân rã |
|
55Mn |
100% |
Bền |
|||
- Ngoài đồng vị ổn định trên, manganese còn có 18 đồng vị phóng xạ, trong đó đồng vị phóng xạ ổn định gồm 53Mn và 54Mn.
II. Kiến thức mở rộng
1. Ứng dụng của một số đồng vị
a. Đồng vị manganese bền (55Mn)
- Sản xuất thép: Đây là ứng dụng phổ biến nhất của manganese. Manganese giúp tăng độ cứng, độ bền và khả năng chống mài mòn của thép. Nó cũng cải thiện khả năng gia công và hàn của thép.
- Pin: Manganese dioxide (MnO2) được sử dụng làm cực dương trong pin kiềm và pin khô.
- Chế tạo hợp kim: Manganese được sử dụng để tạo ra nhiều loại hợp kim khác nhau, chẳng hạn như nhôm-manganese, đồng-manganese, và sắt-manganese. Các hợp kim này có nhiều ứng dụng trong các ngành công nghiệp khác nhau.
- Phân bón: Các hợp chất của manganese được sử dụng làm phân bón để cung cấp chất dinh dưỡng cho cây trồng.
- Chất xúc tác: Một số hợp chất của manganese được sử dụng làm chất xúc tác trong các phản ứng hóa học.
b. Đồng vị manganese phóng xạ
- Y học:
+ Chẩn đoán hình ảnh: Một số đồng vị phóng xạ của manganese được sử dụng trong các kỹ thuật chẩn đoán hình ảnh như PET (Positron Emission Tomography) để nghiên cứu chức năng của não và các cơ quan khác.
+ Điều trị ung thư: Manganese được sử dụng trong một số kỹ thuật trị liệu bằng hạt nhân để tiêu diệt các tế bào ung thư.
- Công nghiệp:
+ Đo lường độ mòn: Các đồng vị phóng xạ của manganese được sử dụng để đo lường độ mòn của các thiết bị và vật liệu.
+ Kiểm soát chất lượng: Đồng vị phóng xạ của manganese được sử dụng để kiểm soát chất lượng trong các quá trình sản xuất.
2. Công thức tính nguyên tử khối trung bình
- Nguyên tử khối của một nguyên tố hóa học có nhiều đồng vị là nguyên tử khối trung bình của các đồng vị, có tính đến tỉ lệ số nguyên tử các đồng vị tương ứng.
- Công thức tính nguyên tử khối trung bình của nguyên tố X:
Trong đó:
: là nguyên tử khối trung bình của X
X, Y, Z …: lần lượt là số khối của các đồng vị.
x, y, z… là phần trăm số nguyên tử của các đồng vị tương ứng.
III. Bài tập minh họa
Câu 1: Nguyên tố A có hai đồng vị X và Y. Tỉ lệ số nguyên tử của X: Y là 45: 455. Tổng số hạt trong nguyên tử của X bằng 32. Trong Y số hạt mang điện gấp 2 lần số hạt không mang điện. Tính nguyên tử khối trung bình của A.
Hướng dẫn giải
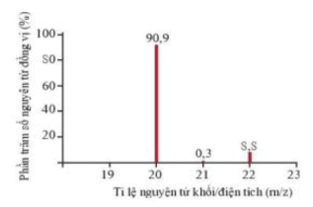
Câu 2. Phổ khối, hay phổ khối lượng chủ yếu được sử dụng để xác định phân tử khối, nguyên tử khối của các chất và hàm lượng các đồng vị bền của một nguyên tố. Phổ khối của neon được biểu diễn như hình dưới. Trục tung biểu thị hàm lượng phần trăm về số nguyên tử của từng đồng vị, trục hoành biểu thị tỉ số của nguyên tử khối (m) của mỗi đồng vị với điện tích của các ion đồng vị tương ứng (điện tích Z của các ion đồng vị neon đều bằng +1).
a) Neon có bao nhiêu đồng vị bền?
b) Tính nguyên tử khối trung bình của neon.
Hướng dẫn giải
a) Neon có 3 đồng vị bền: 20Ne (90,9%), 21Ne (0,3%) và 22Ne (8,8%).
b)
Câu 3: Đồng vị phóng xạ cobalt (Co-60) phát ra tia γ có khả năng đâm xuyên mạnh, dùng điều trị các khối u ở sâu trong cơ thể. Cobalt có ba đồng vị: 59Co (chiếm 98%), 58Co và 60Co; nguyên tử khối trung bình của cobalt là 58,982. Xác định hàm lượng phần trăm của đồng vị Co-60.
Hướng dẫn giải
Xem thêm các bài viết về đồng vị của các nguyên tố hóa học hay khác:
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)








 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



