C4H10 → C2H4 + C2H6 | Butan ra etilen và etan
Phản ứng cracking butan ra etilen và etan hay C4H10 tạo ra C2H6 và C2H4 thuộc loại phản ứng tách đã được cân bằng chính xác và chi tiết nhất. Bên cạnh đó là một số bài tập có liên quan về C4H10 có lời giải, mời các bạn đón xem:
C4H10 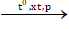 C2H6 + C2H4
C2H6 + C2H4
1. Phương trình phản ứng butan ra etilen
Phản ứng trên là phản ứng tách alkane hay phản ứng cracking.
2. Hiện tượng của phản ứng butan ra etilen
- Tạo khí C2H4, C2H6. Thực tế phản ứng tạo ra hỗn hợp các sản phẩm.
- Dẫn sản phẩm sinh ra vào ống nghiệm có chứa dung dịch brom thấy dung dịch brom nhạt màu dần.
3. Cách tiến hành phản ứng butan ra etilen
- cracking butan trong điều kiện nhiệt độ, xúc tác thích hợp.
4. Mở rộng về tính chất hoá học của alkane
- Ở nhiệt độ thường, các alkane không tác dụng với dung dịch axit, dung dịch kiềm và các chất oxi hóa như dung dịch KMnO4 (thuốc tím)...
- Khi chiếu sáng hoặc đun nóng, các alkane dễ dàng tham gia các phản ứng thế, phản ứng tách hiđro và phản ứng cháy.
4.1. Phản ứng thế bởi halogen
- Clo có thể thay thế lần lượt từng nguyên tử H trong phân tử methane.
Phương trình hóa học:
CH4 + Cl2 CH3Cl + HCl
CH3Cl + Cl2 CH2Cl2 + HCl
CH2Cl2 + Cl2 CHCl3 + HCl
CHCl3 + Cl2 CCl4 + HCl
- Các đồng đẳng của methane cũng tham gia phản ứng thế tương tự methane.
Nhận xét:
- Nguyên tử hiđro liên kết với nguyên tử cacbon bậc cao hơn dễ bị thế hơn nguyên tử hiđro liên kết với nguyên tử cacbon bậc thấp hơn.
4.2. Phản ứng tách
- Dưới tác dụng của nhiệt và chất xúc tác thích hợp, các alkane có phân tử khối nhỏ bị tách hiđro thành hydrocarbon không no tương ứng.
Thí dụ:
CH3 – CH3 CH2 = CH2 + H2
- Ở nhiệt độ cao và chất xúc tác thích hợp, ngoài việc bị tách hiđro, các alkane còn có thể bị phân cắt mạch cacbon tạo thành các phân tử nhỏ hơn.
Thí dụ:
CH3 – CH2 – CH3
4.3. Phản ứng oxi hóa
- Khi bị đốt, các alkane đều cháy, tỏa nhiều nhiệt.
CnH2n + 2 + O2 nCO2 + (n + 1)H2O
5. Bài tập vận dụng liên quan
Câu 1: Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm methane, etan, propane bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (đktc) và 9,9 gam nước. Thể tích không khí (đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên niên trên là
A. 70,0 lít B. 78,4 lít C. 84,0 lít D. 56,0 lít.
Hướng dẫn giải
Đáp án A
= 7,84 : 22,4 = 0,35 mol;
= 9,9 : 18 = 0,55 mol
Bảo toàn nguyên tố O: 2.= 2. +
→ 2.= 2.0,35 + 0,55 → = 0,625 mol
= 0,625.22,4 = 14 lít
Vì oxi chiếm Vkk → Vkk = 5.14 = 70 lít
Câu 2: Khi brom hóa một alkane chỉ thu được một dẫn xuất monobrom duy nhất có tỉ khối hơi đối với hiđro là 75,5. Tên của alkane là
A. 3,3-dimethylhexan B. 2,2-dimethylpropan
C. isopentane D. 2,2,3-trimethylpentan.
Hướng dẫn giải
Đáp án B
CnH2n+2 + Br2 → CnH2n+1Br + HBr
→ 14n + 81 = 75,5.2 → n = 5 → CTPT: C5H12
Khi brom hóa alkane chỉ thu được một dẫn xuất monobrom duy nhất
nên CTCT của X là:
Câu 3: Trong công nghiệp alkane có ứng dụng là:
A. Làm nhiên liệu, nguyên liệu. B. Làm thực phẩm.
C. Làm hương liệu. D. Làm mĩ phẩm.
Hướng dẫn giải
Đáp án A
Khi đốt, alkane dễ cháy tạo ra CO2, H2O và tỏa nhiều nhiệt. Đặc biệt alkane còn có nhiều trong khí thiên nhiên và dầu mỏ nên được dùng làm nhiên liệu cho động cơ hoặc chất làm đốt.
→ Các alkane có ứng dụng làm nhiên liệu, nguyên liệu cho ngành công nghiệp.
VD: Nhiên liệu cho động cơ, chất bôi trơn, chất đốt (gas), nến thắp, giấy dầu, giấy nến,...
Câu 4: Trong phương pháp điều chế etan dưới đây, phương pháp nào sai?
A. Đun natri propionat với vôi xút. B. Cho etilen cộng hợp với H2.
C. Tách nước khỏi ethyl alcohol. D. Cracking butan.
Hướng dẫn giải
Đáp án C
A. Đúng. C2H5COONa + NaOH C2H6 + Na2CO3
B. Đúng. CH2=CH2 + H2 CH3-CH3
C. Sai. Khi tách H2O khỏi ethylic alcohol ta được etilen chứ không được etan.
CH3-CH2OH CH2=CH2.
D. Đúng. CH3-CH2-CH2-CH3 CH3-CH3 + CH2=CH2
Câu 5:Hỗn hợp khí A gồm etan và propan. Đốt cháy hỗn hợp A thu được khí CO2 và hơi nước theo tỷ lệ thể tích 11:15. Thành phần phần trăm theo khối lượng của hai chất lần lượt là:
A. 18,5% và 81,5% B. 45% và 55%
C. 28,1% và 71,9% D. 25% và 75%
Hướng dẫn giải
Đáp án A
Đặt = a ; = b;
Có : = 11 : 15
→ (2a+3b) : (3a+4b) = 11 : 15
→ b = 3a
Tỉ lệ thể tích bằng tỉ lệ số mol
Giả sử = 1 mol→ = 3 mol
→ mA = 1.30 + 3.44 = 162 gam
→ % = = 18,5%
% = = 81,5%
Câu 6: Công thức cấu tạo của gốc isopropyl là
A. CH3-CH2- B. CH3-CH2-CH2-
C. CH3-CH(CH3)- D. CH3-CH(CH3)-CH2-CH2-
Hướng dẫn giải
Đáp án C
A. CH3-CH2- etyl
B.CH3-CH2-CH2- propyl
C. CH3-CH(CH3)-isopropyl
D. CH3-CH(CH3)-CH2-CH2- isoamyl
Câu 7: Trong các khẳng định sau đây, khẳng định nào đúng?
A. alkane từ C4H10 trở đi có đồng phân cấu tạo.
B. alkane mà phân từ chỉ chứa C bậc I và C bậc II là alkane không phân nhánh.
C. alkane có cả dạng mạch hở và mạch vòng.
D. A và B đúng.
Hướng dẫn giải
Đáp án D
A. Đúng. Từ C4H10 trở đi, ứng với những công thức phân tử có các công thức cấu tạo mạch cacbon không phân nhánh và mạch cacbon phân nhánh.
B. Đúng.
C. Sai vì alkane không có dạng mạch vòng
Câu 8: Đốt cháy hoàn toàn hỗn hợp X gồm hai hydrocarbon kế tiếp nhau trong dãy đồng đẳng thu được 2,24 lít CO2 (đktc) và 3,24 gam H2O. Hai hydrocarbon trong X là
A. C2H6 và C3H8 B. CH4 và C2H6 .
C. C2H2 và C3H4 D. C2H4 và C3H6
Hướng dẫn giải
Đáp án B
= 2,24 : 22,4 = 0,1 mol;
= 3,24 : 18 = 0,18 mol
>→ X là alkane → X có CTPT chung là CnH2n+2
nX = - = 0,18 – 0,1 = 0,08 mol
→ n = = = 1,25
→Hai hydrocarbon kế tiếp là CH4 và C2H6
Câu 9: Đốt cháy hoàn toàn một hydrocarbon X, dẫn sản phẩm cháy lần lượt qua bình đựng P2O5 và Ca(OH)2 thì khối lượng các bình này tăng lên lần lượt là 0,9gam và 1,1 gam. Công thức phân tử của X là:
A. C4H10B. C3H8C. C2H6D. CH4
Hướng dẫn giải
Đáp án D
Khối lượng bình P2O5 tăng chính là khối lượng nước
→ = 0,9 gam → = 0,05 mol
Khối lượng bình Ca(OH)2 tăng chính là khối lượng CO2
→= 1,1 gam → = 0,025 mol
> → X là alkane
→ X có CTPT chung là CnH2n+2
nX = - = 0,05 – 0,025 = 0,025 mol
→ n = = = 1
→ X là CH4
Câu 10: Đốt cháy hoàn toàn 0,15 mol hỗn hợp 2 alkane thu được 9,45 gam H2O. Cho sản phẩm cháy vào dung dịch Ca(OH)2 dư thì khối lượng kết tủa thu được là:
A. 37,5 B. 52,5 C. 15 D. 42,5
Hướng dẫn giải
Đáp án A
Đốt cháy alkane ta có: nalkane = -
→ 0,15 = 0,525 - → = 0,375 mol
→= 0,375 mol
→= 0,375.100 = 37,5 gam.
Xem thêm các phương trình hóa học hay khác:
- C4H10 + Cl2 → C4H9Cl + HCl
- C4H10 + 2Cl2 → C4H8Cl2 + 2HCl
- C4H10 → C4H8 + H2
- C4H10 → C3H6 + CH4
- 2C4H10 + 13O2 → 8CO2 + 10H2O
- C4H10 + Br2 → C4H9Br + HBr
- C4H10 + 2Br2 → C4H8Br2 + 2HBr
- CH3CH2CH2CH3 + O2 → 2CH3COOH + H2O
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)

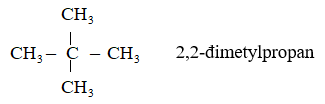







 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



