styrene + KMnO4 | C6H5-CH=CH2 + KMnO4 → C6H5COOK + K2CO3 + MnO2 + KOH + H2O
Phản ứng styrene + KMnO4 hay C6H5-CH=CH2 + KMnO4 thuộc loại phản ứng oxi hóa khử đã được cân bằng chính xác và chi tiết nhất. Bên cạnh đó là một số bài tập có liên quan về styrene có lời giải, mời các bạn đón xem:
3C6H5-CH=CH2 + 10KMnO4 3C6H5COOK +3K2CO3 +10MnO2↓+KOH+4H2O
1. Phương trình hóa học của phản ứng styrene tác dụng với KMnO4
3C6H5-CH=CH2 + 10KMnO4 → 3C6H5COOK + 3K2CO3 + 10MnO2 + KOH + 4H2O
2. Lập phương trình hóa học của phản ứng theo phương pháp thăng bằng electron
Bước 1: Xác định các nguyên tử có sự thay đổi số oxi hóa, từ đó xác định chất oxi hóa – khử:
Chất khử: C6H5-CH=CH2; chất oxi hóa: KMnO4
Bước 2: Biểu diễn quá trình oxi hóa, quá trình khử
- Quá trình oxi hóa:
- Quá trình khử:
Bước 3: Tìm hệ số thích hợp cho chất khử và chất oxi hóa
Bước 4: Điền hệ số của các chất có mặt trong phương trình hóa học. Kiểm tra sự cân bằng số nguyên tử của các nguyên tố ở hai vế.
3C6H5-CH=CH2 + 10KMnO4 → 3C6H5COOK + 3K2CO3 + 10MnO2 + KOH + 4H2O
3. Điều kiện để styrene tác dụng với KMnO4
- Nhiệt độ thường.
4. Cách tiến hành thí nghiệm
- Cho styrene vào ống nghiệm có chứa sẵn 1 – 2 ml dung dịch thuốc tím.
5. Hiện tượng phản ứng
- styrene phản ứng làm mất màu KMnO4 ở điều kiện thường.
6. Mở rộng kiến thức về styrene
6.1. Cấu tạo và tính chất vật lí
- Công thức phân tử: C8H8
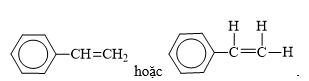
- Công thức cấu tạo:
- styrene (còn gọi là vinylbenzen) là chất lỏng không màu, sôi ở 146oC, tan nhiều trong dung môi hữu cơ.
6.2. Tính chất hoá học
a) Phản ứng với dung dịch brom
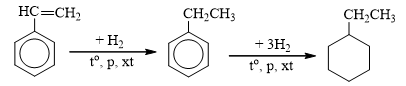
b) Phản ứng với hiđro
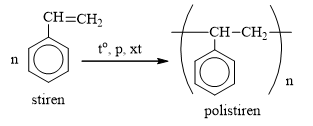
c) Phản ứng trùng hợp
7. Bài tập vận dụng liên quan
Câu 1: Để phân biệt benzene, toluene, styrene ta chỉ dùng 1 thuốc thử duy nhất là:
A. Brom (dd).
B. Br2 (Fe).
C. KMnO4 (dd).
D. Br2 (dd) hoặc KMnO4(dd).
Hướng dẫn giải:
Đáp án C
Thuốc thử phù hợp là KMnO4 (dd):
- Mất màu ngay ở nhiệt độ thường → styrene
- Mất màu khi đun nóng → toluene
- Không mất màu ở bất kì điều kiện nào → benzene
Câu 2: A có công thức phân tử là C8H8, tác dụng với dung dịch KMnO4 ở nhiệt độ thường tạo ra ancol 2 chức. 1 mol A cộng tối đa với bao nhiêu mol H2 (Ni, to) và bao nhiêu mol Br2 trong dung dịch?
A. 4 mol H2; 1 mol brom.
B. 3 mol H2; 1 mol brom.
C. 3 mol H2; 3 mol brom.
D. 4 mol H2; 4 mol brom.
Hướng dẫn giải:
Đáp án A
C8H8 có k = = 5 tác dụng với dung dịch KMnO4 ở nhiệt độ thường tạo ra ancol 2 chức → có chứa 1 nối đôi ngoài vòng và 1 vòng benzene
→ Chỉ cộng tối đa 4 mol H2 (3π trong vòng + 1π ngoài vòng) và 1 mol Br2 trong dung dịch (chỉ cộng vào 1π ngoài vòng)
Câu 3:Đề hiđro hoá etylbenzen ta được styrene; trùng hợp styrene ta được polistiren với hiệu suất chung 80%. Khối lượng etylbenzen cần dùng để sản xuất 10,4 tấn polisitren là:
A. 13,52 tấn.
B. 10,6 tấn.
C. 13,25 tấn.
D. 8,48 tấn.
Hướng dẫn giải:
Đáp án C
Sơ đồ phản ứng:
nC6H5-CH2-CH3 → nC6H5-CH=CH2 → PS
106n (gam)→104n (gam)
10,6 tấn←10,4 tấn
Do hiệu suất chỉ đạt 80% nên lượng etylbenzen thực tế cần dùng là:
= 13,25 tấn.
Câu 4: Tiến hành trùng hợp 10,4 gam styrene được hỗn hợp X gồm polistiren và styrene (dư). Cho X tác dụng với 200 ml dung dịch Br2 0,15M, sau đó cho dung KI dư vào thấy xuất hiện 1,27 gam iot. Hiệu suất trùng hợp styrene là
A. 60%.
B. 75%.
C. 80%.
D. 83,33%.
Hướng dẫn giải:
Đáp án B
nstyrene ban đầu = = 0,1 mol
(1) C6H5CH=CH2 + Br2 → C6H5CHBr-CH2Br
(2) Br2 + 2KI → 2KBr + I2
Theo (2): dư = = 0,005 mol → pư = 0,03 – 0,005 = 0,025 mol
Theo (1): nstyrene dư = pứ = 0,025 mol
→ nstyrene tham gia pứ trùng hợp = n ban đầu – n dư = 0,1 – 0,025 = 0,075 mol
Câu 5: Cho các hydrocarbon: eten; acetylene; benzene; toluene; isopentane; styrene. Số chất làm mất màu dung dịch KMnO4 là:
A. 4
B. 5
C. 6
D. 3
Hướng dẫn
Các chất làm mất màu dung dịch KMnO4 là 4 chất: eten; acetylene; toluene; styrene.
(Lưu ý: toluene làm mất màu dung dịch thuốc tím khi đun nóng).
Đáp án A
Câu 6: Cứ 49,125 gam cao su buna-S phản ứng vừa hết với 30 gam brom trong CCl4. Tỉ lệ số mắt xích styrene và butadiene trong loại cao su trên tương ứng là
A. 1 : 2.
B. 2 : 3.
C. 2 : 1.
D. 1 : 3.
Hướng dẫn giải:
Đáp án C
Giả sử số mắt xích C4H6 là 1 và số mắt xích C8H8 là k. Ta có công thức cao su: C4H6(C8H8)k
C4H6(C8H8)k + Br2 → C4H6Br2(C8H8)k
54 + 104k → 160 (g)
49,125 → 30 (g)
→ 30(54 + 104k) = 160.49,125 → k = 2
Tỉ lệ mắt xích styrene và butadiene là 2 : 1
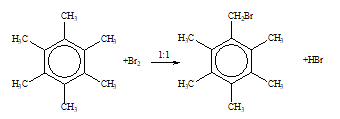
Câu 7: Trong phân tử X có vòng benzene. X không tác dụng với brom khi có mặt bột Fe, còn khi tác dụng với brom đun nóng tỉ lệ 1:1 tạo thành dẫn xuất monobrom duy nhất nên tên của X là
A. benzene
B. Hexamethyl benzene.
C. toluene
D. o - Xilen
Hướng dẫn giải:
Đáp án B
X là hexamethyl benzene:
- Khi có mặt Fe không thế vào nhân vì không còn H
- Thế Br2 phía ngoài vòng thu được sản phẩn duy nhất là:
Câu 8: Cho 100 ml benzene (D = 0,879 g/ml) tác dụng với một lượng vừa đủ brom lỏng (có mặt bột sắt, đun nóng) thu được 80 ml brombenzen (D = 1,495 g/ml). Hiệu suất brom hóa đạt là
A. 67,6%.
B. 73,49%.
C. 85,3%.
D. 65,35%
Hướng dẫn giải:
Đáp án A
Ta có:
m benzene = 100.0,879 = 87,9 gam → n benzene =
m brom benzene = 80.1,495 = 119,6 gam → n brom benzene =
Xem thêm các phương trình hóa học hay khác:
- C6H5CH=CH2 + Br2 → C6H5-CHBr-CH2Br
- C6H5-CH=CH2 + HBr → C6H5-CH(Br)-CH3
- C6H5CH3 + Br2 C6H5CH2Br + HBr
- C6H5CH3 + 2KMnO4 C6H5COOK + KOH + 2MnO2↓ + H2O
- C6H5 + Br2 C6H5Br + HBr
- C6H6 + HNO3 C6H5NO2 + H2O
- C6H5CH3 + HNO3 C6H2(NO2)3CH3 + 3H2O
- C6H6 + 3H2 C6H12
- C6H6 + 3Cl2 C6Cl6
- n-C6H5-CH=CH2 (CH2 -CH-C6H5)n
- 2C6H6 + 15O2 12CO2 + 6H2O
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)

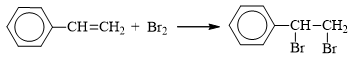







 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



