K2CO3 + AlCl3 + H2O → KCl + Al(OH)3 + CO2 | K2CO3 ra KCl | K2CO3 ra Al(OH)3 | K2CO3 ra CO2 | AlCl3 ra KCl | AlCl3 ra Al(OH)3 | AlCl3 ra CO2
Phản ứng K2CO3 + AlCl3 + H2O hay K2CO3 ra KCl hoặc K2CO3 ra Al(OH)3 hoặc K2CO3 ra CO2 hoặc AlCl3 ra KCl hoặc AlCl3 ra Al(OH)3 hoặc AlCl3 ra CO2 thuộc loại phản ứng trao đổi đã được cân bằng chính xác và chi tiết nhất. Bên cạnh đó là một số bài tập có liên quan về K2CO3 có lời giải, mời các bạn đón xem:
3K2CO3 + 2AlCl3 + 3H2O → 6KCl + 2Al(OH)3 + 3CO2
Điều kiện phản ứng
- điều kiện thường,
Cách thực hiện phản ứng
- Nhỏ K2CO3 vào ống nghiệm chứa AlCl3.
Hiện tượng nhận biết phản ứng
- Có kết tủa trắng và sủi bọt khí.
Bạn có biết
- Khi cho dung dịch muối của nhôm phản ứng với K2CO3 đều thấy có sủi bọt khí và xuất hiện kết tủa trắng.
Ví dụ minh họa
Ví dụ 1:
Khi cho AlCl3 vào ống nghiệm chứa K2CO3 thu được hiện tượng là
A. Có kết tủa trắng thoát ra và sủi bọt khí.
B. Có khí màu nâu đỏ thoát ra.
C. Có kết tủa vàng.
D. Không có hiện tượng gì.
Hướng dẫn giải
3K2CO3 + 2AlCl3 + 3H2O → 6KCl + 2Al(OH)3 + 3CO2
Al(OH)3: kết tủa trắng.
CO2: khí không màu,
Đáp án A.
Ví dụ 2:
Thể tích khí CO2 ở dktc thoát ra khi cho 13,8g K2CO3 phản ứng hoàn toàn với lượng dung dịch AlCl3 là
A. 1,12 lít. B. 2,24 lít. C. 3,36 lít. D. 4,48 lít.
Hướng dẫn giải
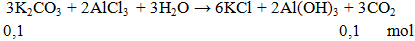
V = 0,1.22,4 = 2,24 lít.
Đáp án B.
Ví dụ 3:
Khối lượng kết tủa thu được khi cho 20,7g K2CO3 phản ứng hoàn toàn với lượng dung dịch AlCl3 là
A. 0,78g. B. 7,8g. C. 0,87g. D. 8,7g.
Hướng dẫn giải
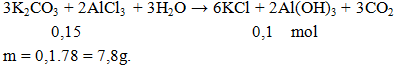
Đáp án B.
Xem thêm các phương trình hóa học hay khác:
- K2CO3 + 2HCl → 2KCl + CO2 + H2O
- K2CO3 + 2HBr → 2KBr + CO2 + H2O
- K2CO3 + H2SO4 → K2SO4 + CO2 + H2O
- K2CO3 + 2HNO3 → 2KNO3 + CO2 + H2O
- K2CO3 + Ba(OH)2 → 2KOH + BaCO3( ↓)
- K2CO3 + Ca(OH)2 → 2KOH + CaCO3( ↓)
- K2CO3 + CaCl2 → 2KCl + CaCO3( ↓)
- K2CO3 + BaCl2 → 2KCl + BaCO3( ↓)
- K2CO3 + Ba(NO3)2 → 2KNO3 + BaCO3( ↓)
- K2CO3 + Ca(NO3)2 → 2KNO3 + CaCO3( ↓)
- K2CO3 + Cl2 → KCl + KClO + CO2
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)








 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



