Ma trận đề thi Giữa kì 1 Hóa học 11 năm 2024
Tài liệu Ma trận đề thi Giữa kì 1 Hóa học 11 năm 2024 mới nhất gồm bảng đặc tả và 3 đề thi có đáp án và lời giải chi tiết. Hi vọng Ma trận đề thi Giữa kì 1 Hóa học 11 năm 2024 sẽ giúp học sinh có kế hoạch ôn tập, luyện đề hiệu quả từ đó đạt kết quả cao trong các bài thi môn Hóa học lớp 11.
Ma trận đề thi Giữa kì 1 Hóa học 11 năm 2024
MA TRẬN ĐỀ THI GIỮA HỌC KÌ 1
MÔN: HÓA HỌC 11 – THỜI GIAN LÀM BÀI: 45 PHÚT
|
TT |
Nội dung kiến thức |
Đơn vị kiến thức |
Mức độ nhận thức |
Tổng |
% tổng điểm |
|
|||||||||
|
Nhận biết |
Thông hiểu |
Vận dụng |
Vận dụng cao |
|
|||||||||||
|
Số CH |
Thời gian (phút) |
|
|||||||||||||
|
Số CH |
Thời gian (phút) |
Số CH |
Thời gian (phút) |
Số CH |
Thời gian (phút) |
Số CH |
Thời gian (phút) |
TN |
TL |
|
|||||
|
1 |
Sự điện li
|
Sự điện li |
2 |
1,5 |
1 |
1 |
1 |
4,5 |
0 |
0 |
3 |
2 |
22,5 |
7,5% |
|
|
Axit, bazơ và muối |
3 |
2,25 |
1 |
1 |
1 |
6 |
4 |
20% |
|
||||||
|
Sự điện li của nước. pH. Chất chỉ thị axit-bazơ |
3 |
2,25 |
2 |
2 |
5 |
12,5% |
|
||||||||
|
Phản ứng trao đổi ion trong dung dịch các chất điện li |
2 |
2 |
2 |
10% |
|
||||||||||
|
2 |
Nitơ và hợp chất của nitơ |
Nitơ |
2 |
1,5 |
1 |
1 |
1 |
4,5 |
1 |
6 |
3 |
2 |
22,5 |
7,5% |
|
|
amonia và muối amoni |
3 |
2,25 |
3 |
3 |
6 |
25% |
|
||||||||
|
Nitric acid và muối nitrate |
3 |
2,25 |
2 |
2 |
5 |
17,5% |
|
||||||||
|
Tổng |
16 |
12 |
12 |
12 |
2 |
9 |
2 |
12 |
28 |
4 |
45 |
100% |
|
||
|
Tỉ lệ % |
40% |
30% |
20% |
10% |
|
|
|
100% |
|
||||||
|
Tỉ lệ chung |
70% |
30% |
|
|
100% |
|
|||||||||
Lưu ý:
- Các câu hỏi ở cấp độ nhận biết và thông hiểu là các câu hỏi trắc nghiệm khách quan 4 lựa chọn, trong đó có duy nhất 1 lựa chọn đúng.
- Các câu hỏi ở cấp độ vận dụng và vận dụng cao là các câu hỏi tự luận.
- Số điểm tính cho 1 câu trắc nghiệm là 0,25 điểm/câu; số điểm của câu tự luận được quy định trong hướng dẫn chấm nhưng phải tương ứng với tỉ lệ điểm được quy định trong ma trận.
- Trong nội dung kiến thức Sự điện li chỉ được chọn một câu mức độ vận dụng và một câu mức độ vận dụng cao ở nội dung đó.
- Trong nội dung kiến thức Nitơ và hợp chất của nitơ chỉ được chọn một câu mức độ vận dụng và một câu mức độ vận dụng cao ở nội dung đó.
Đề thi Giữa học kì 1 năm học 2021
Môn thi Hóa học - Lớp 11
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
PHẦN TRẮC NGHIỆM (7,0 điểm)
Câu 1: Dung dịch chất nào sau đây dẫn được điện?
A. NaCl.
B. C6H12O6 (glucose).
C. C12H22O11 (saccharose).
D. C2H5OH.
Câu 2: Chất nào sau đây là chất điện li yếu?
A. KNO3.
B. NaOH.
C. HCl.
D. CH3COOH.
Câu 3: Theo thuyết A-rê-ni-ut, chất nào sau đây là axit?
A. HCl.
B. C6H12O6 (glucose).
C. K2SO4.
D. NaOH.
Câu 4: Chất nào sau đây là hiđroxit lưỡng tính?
A. Ba(OH)2.
B. Al(OH)3.
C. NaOH.
D. Ca(OH)2.
Câu 5: Chất nào sau đây là muối trung hòa?
A. NaHCO3.
B. NaH2PO4.
C. NaHSO4.
D. Na2SO4.
Câu 6: Môi trường axit có nồng độ ion H+ thỏa mãn điều kiện nào sau đây?
A. [H+] < [OH-].
B. [H+] = 10-7.
C. [H+] > 10-7.
D. [H+] < 10-7.
Câu 7: Dung dịch chất nào sau đây làm quỳ tím chuyển màu xanh?
A. KOH.
B. KNO3.
C. H2SO4.
D. NaCl.
Câu 8: Dung dịch chất nào sau đây có pH < 7?
A. KNO3.
B. CH3COOH.
C. Ba(OH)2.
D. Na2SO4.
Câu 9: Trong bảng tuần hoàn, nitơ thuộc nhóm nào sau đây?
A. Nhóm VA.
B. Nhóm IIIA.
C. Nhóm IA.
D. Nhóm VIIIA.
Câu 10: Trong công nghiệp nitơ, được sản xuất bằng phương pháp nào sau đây?
A. Chưng cất phân đoạn không khí lỏng.
B. Dẫn không khí qua bình chứa Cu dư, đun nóng.
C. Dẫn không khí qua dung dịch HNO3.
D. Dẫn không khí qua bình chứa photpho dư.
Câu 11: Chất nào sau đây có tính bazơ?
A. N2.
B. NH3.
C. HNO3.
D. NaNO3.
Câu 12: Muối NH4Cl tác dụng được với dung dịch chất nào sau đây?
A. Ca(OH)2.
B. NaNO3.
C. (NH4)2SO4.
D. KCl.
Câu 13: Amoniac có tính chất vật lí nào sau đây?
A. Tan tốt trong nước.
B. Có màu nâu đỏ.
C. Không tan trong nước.
D. Có màu xanh tím.
Câu 14: Số oxi hóa của nitơ trong HNO3 là
A. +2.
B. +3.
C. +4.
D. +5.
Câu 15: Chất nào sau đây là axit mạnh?
A. NH3.
B. HNO3.
C. NH4Cl.
D. NaNO3.
Câu 16: Công thức của muối natri nitrate là
A. NaNO3.
B. Na2CO3.
C. NaCl.
D. KNO3.
Câu 17: Phương trình điện li nào sau đây đúng?
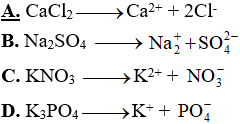
Câu 18: Cho các chất: Ca(OH)2, NH4Cl, NaHSO4 và KOH. Có bao nhiêu chất là bazơ theo thuyết A-rê-ni-ut trong các chất trên?
A. 1.
B. 2.
C. 3.
D. 4.
Câu 19: Giá trị pH của dung dịch HCl 0,01M là
A. 2.
B. 1.
C. 3.
D. 4.
Câu 20: Dung dịch chất nào sau đây có pH nhỏ nhất?
A. HCl.
B. NaCl.
C. K2SO4.
D. Ba(OH)2.
Câu 21: Phương trình nào sau đây là phương trình ion rút gọn của phản ứng giữa NaOH với HCl trong dung dịch?
A. Na+ + Cl- →NaCl
B. NaOH + H+ →Na+ + H2O
C. OH- + H+ →H2O
D. NaOH + Cl- →NaCl + OH-
Câu 22: Để trung hòa 0,1 mol H2SO4 cần dùng vừa đủ a mol NaOH. Giá trị của a là
A. 0,10.
B. 0,05.
C. 0,20.
D. 0,15.
Câu 23: Nitơ khá trơ ở nhiệt độ thường do nguyên nhân nào sau đây?
A. Trong phân tử N2, liên kết giữa hai nguyên tử N là liên kết ba bền vững.
B. Trong phân tử N2, liên kết giữa hai nguyên tử N là liên kết đơn.
C. Trong các phản ứng hóa học, nitơ chỉ thể hiện tính oxi hóa.
D. Trong các phản ứng hóa học, nitơ chỉ thể hiện tính khử.
Câu 24: Nhỏ 1 hoặc 2 giọt phenolphtalein vào dung dịch NH3, hiện tượng quan sát được là
A. dung dịch từ không màu chuyển sang màu hồng.
B. dung dịch từ màu hồng chuyển sang màu xanh.
C. xuất hiện kết tủa làm vẩn đục dung dịch.
D. sủi bọt, tạo chất khí không mùi bay ra.
Câu 25: Cho muối X vào dung dịch NaOH, đun nóng, thu được một chất khí làm xanh giấy quỳ ẩm. Chất nào sau đây thỏa mãn tính chất của X?
A. K2SO4.
B. NH4NO3.
C. CaCO3.
D. FeCl2.
Câu 26: Cho 0,1 mol NH4Cl tác dụng với lượng dư dung dịch Ba(OH)2 đun nóng, thu được a mol NH3. Giá trị của a là
A. 0,05.
B. 0,10.
C. 0,15.
D. 0,20.
Câu 27: Cho kim loại Fe tác dụng với dung dịch HNO3 đặc, nóng, dư, thu được muối sắt nào sau đây?
A. Fe(NO3)2.
B. Fe(NO3)3.
C. Fe(NO3)2 và Fe(NO3)3.
D. Fe2(NO3)3.
Câu 28: Phương trình nào sau đây đúng?
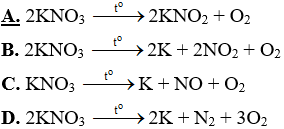
PHẦN TỰ LUẬN (3,0 điểm)
Câu 29 (1,0 điểm).
Dung dịch X chứa BaCl2 0,05M và HCl 0,10M. Bỏ qua sự điện li của nước.
a. Viết phương trình điện li của các chất trong X.
b. Tính nồng độ mol/l của các ion trong X.
Câu 30 (1,0 điểm).
Viết phương trình hóa học của phản ứng xảy ra trong các thí nghiệm sau:
a. Cho dung dịch NH3 vào dung dịch FeCl3.
b. Đốt khí NH3 trong O2 có xúc tác Pt.
c. Cho dung dịch (NH4)2SO4 vào dung dịch Ba(OH)2.
d. Nhiệt phân muối NH4NO3.
Câu 31 (0,5 điểm).
Có bốn dung dịch: NaCl, Na2SO4, NaNO3 và HNO3 đựng trong bốn bình riêng biệt. Trình bày phương pháp hóa học để phân biệt từng dung dịch. Viết các phương trình phản ứng xảy ra (nếu có).
Câu 32 (0,5 điểm).
Hỗn hợp X gồm NaNO3 và Mg(NO3)2. Nhiệt phân hoàn toàn một lượng X, thu được hỗn hợp khí Y gồm NO2 và O2, tỉ khối của Y so với H2 là 19,5. Tính phần trăm theo khối lượng mỗi muối trong X.
Xem thêm tài liệu ma trận đề thi môn Hóa học lớp 11 chọn lọc, có đáp án hay khác:
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

