155 bài tập trắc nghiệm Đại cương về kim loại (có đáp án)
Tổng hợp bài tập trắc nghiệm Đại cương về kim loại lớp 12 có đáp án và lời giải chi tiết đầy đủ các mức độ nhận biết, thông hiểu, vận dụng sẽ giúp học sinh ôn tập trắc nghiệm Hóa học 12.
155 bài tập trắc nghiệm Đại cương về kim loại (có đáp án)
Thi online Hóa 12 KNTTThi online Hóa 12 CDThi online Hóa 12 CTST
- 15 bài tập trắc nghiệm Vị trí của kim loại trong bảng tuần hoàn và cấu tạo của kim loại (có đáp án)
- 15 bài tập trắc nghiệm Tính chất của kim loại, Dãy điện hóa của kim loại (có đáp án)
- 7 bài tập trắc nghiệm Hợp kim (có đáp án)
- 15 bài tập trắc nghiệm Sự ăn mòn kim loại (có đáp án)
- 15 bài tập trắc nghiệm Điều chế kim loại (có đáp án)
- 15 bài tập trắc nghiệm Tính chất của kim loại (có đáp án)
- 15 bài tập trắc nghiệm Điều chế kim loại và sự ăn mòn kim loại (có đáp án)
- 5 bài tập trắc nghiệm Tính chất, điều chế kim loại, sự ăn mòn kim loại
- 16 bài tập trắc nghiệm Ôn tập Hóa học 12 Học kì 1 (có đáp án)
- Đề thi Học kì 1 Hóa học 12 (có đáp án)
Trắc nghiệm tổng hợp Đại cương về kim loại
- Trắc nghiệm Vị trí của kim loại trong bảng tuần hoàn và cấu tạo của kim loại (có đáp án)
- Trắc nghiệm Tính chất của kim loại, Dãy điện hóa của kim loại (có đáp án)
- Trắc nghiệm Hợp kim (có đáp án)
- Trắc nghiệm Sự ăn mòn kim loại (có đáp án)
- Trắc nghiệm Điều chế kim loại (có đáp án)
- Trắc nghiệm tổng hợp Tính chất của kim loại (có đáp án)
- Trắc nghiệm tổng hợp Điều chế kim loại và sự ăn mòn kim loại (có đáp án)
- Trắc nghiệm Tính chất, điều chế kim loại, sự ăn mòn kim loại
- Trắc nghiệm Ôn tập Học kì 1 (có đáp án)
Trắc nghiệm Vị trí của kim loại trong bảng tuần hoàn và cấu tạo của kim loại (có đáp án)
Câu 1: Phát biểu nào sau đây là sai ?
A. Trong một chu kì, khi điện tích hạt nhân tăng thì tính kim loại tăng dần.
B. Trong một nhóm theo chiều tăng dần của điện tích hạt nhân, tính kim loại tăng,
C. Kim loại có độ âm điện bé hơn phi kim trong cùng chu kì.
D. Đa số các kim loại đều có cấu tạo tinh thể.
Đáp án: A
Trong một chu kì, khi điện tích hạt nhân tăng thì tính kim loại giảm dần
Câu 2: Nguyên tố X ở ô số 24 của bảng tuần hoàn. Một học sinh đã đưa ra các nhận xét về nguyên tố X như sau :
(1) X có 6 e hoá trị yà là nguyên tố kim loại.
(2) X là một nguyên tố nhóm d.
(3) X nằm ở chu kì 4 của bảng tuần hoàn.
(4) Ở trạng thái cơ bản, X có 6 e ở phân lớp s;
Trong các nhận xét trên, số nhận xét đúng là
A. 1. B. 2. C. 3. D. 4.
Đáp án: C
Cấu hình e của nguyên tố này là: 1s22s22p63s23p63d54s1
Các phát biểu 1,2,3 đúng
Câu 3: Xét 2 nguyên tố ở vị trí 19 và 29 trong bảng tuần hoàn. Kết luận nào sau đây là sai ?
A. Hai nguyên tố này cùng là kim loại.
B. Hai nguyên tố này thuộc cùng một chu’kì.
C. Hai nguyên tố này có cùng số e lớp ngoài cùng ở trạng thái cơ bản.
D. Hai nguyên tố này cùng là nguyên tố s.
Đáp án: D
Nguyên tố ở vị trí 19 có cấu hình e: 1s22s22p63s23p64s1 : là nguyên tố thuộc nhóm s
Nguyên tố ở vị trí 29 có cấu hình e: 1s22s22p63s23p63d104s1 : là nguyên tố thuộc nhóm d
Câu 4: Cấu hình electron nguyên tử của ba nguyên tố X, Y, Z lần lượt là ls22s22p63s2, ls22s22p63s23p64s1, ls22s22p63s1. Nếu xếp theo chiều tăng dần tính kim loại thì cách sắp xếp nào sau đây đúng ?
A. Y < Z < X. B. X < Z < Y.
C. X ≤ Y ≤ Z. D. Z < X < Y.
Đáp án: B
X và Z cùng chu kì, ZX > ZZ nên tính kim loại của X < Z
Y và Z cùng nhóm IA; ZY > ZZ nên tính kim loại của Y > Z
Suy ra tính kim loại: X < Z < Y
Câu 5: Kết luận nào sau đây sai?
A. Các nguyên tố nhóm A có cấu hình e lớp ngoài cùng ns2 đều là các kim loại.
B. Nguyên tố có Z = 19 có bán kính lớn hơn nguyên tố có Z = 11
C. Li là kim loại có độ âm điện lớn nhất trong số các kim loại kiềm
D. Các nguyên tố nhóm B đều là kim loại
Đáp án: A
he có cấu hình e lớp ngoài cùng là 1s2 và là khí hiếm
Câu 6: R là một kim loại thuộc nhóm IA của bảng tuần hoàn. Lấy 17,55 gam R tác dụng với 25 gam dung dịch HCl 29,2%. Sau khi phản ứng xảy ra hoàn toàn cho bốc hơi cẩn thận dung dịch tạo thành trong điều kiện không có không khí thì thu được 28,9 gam hỗn hợp rắn gồm hai chất. Kim loại R là:
A. Na B. K C. Rb D. Cs
Đáp án: D
ta có nHCl = 0,2 mol
Xét các phản ứng:
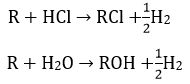
Trong 28,9 gam chất rắn bao gồm ROH và RCl ⇒ 28,9 = mR+ + mCl- + mOH-
nCl- = nHCl = 0,2 mol; mR = 17,55 gam
nOH- = 0,25 mol
nR = 0,45 mol và MR = 39 ⇒ R là kim loại K
Câu 7: Kim loại M phản ứng với oxi để tạo thành oxit. Khối lượng oxi đã phản ứng bằng 40% khối lượng kim loại đã dùng. Kim loại M là:
A. Na B. Ca C.Fe D.Al
Đáp án: B
Đặt công thức của oxit kim loại là MOx
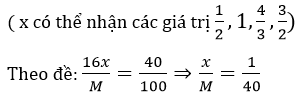
Lập bảng
| X | 1/2 | 1 | 4/3 | 3/2 |
| M | 20 | 40 | 53,33 | 60 |
Vậy kim loại M là Ca, oxit tạo thành là CaO
Câu 8: Một viên bi sắt có đường kính 2cm ngập trong một cốc chứa 100ml axit có pH = 0, phản ứng xảy ra hoàn toàn. Bán kính viên bi sắt sau phản ứng (coi rằng viên bi bị mòn đều từ mọi phí, khối lượng riêng của sắt là 7,8 g/cm3)là:
A. 0,56cm B. 0,84cm C.0,78cm D.0,97cm
Đáp án: D
Số mol H+ là 0,1 mol
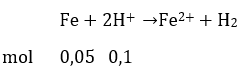
Khối lượng sắt bị tan là: 2,8 gam
Vậy thể tích sắt bị mất đi:
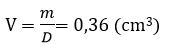
Thể tích ban đầu của viên bi:
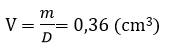
Vậy thể tích của viên bi sắt còn lại sau phản ứng là: V2 = V1 – V = 3,83 cm3
Bán kính viên bi còn lại:
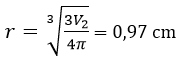
Câu 9: Nhóm A bao gồm các nguyên tố:
A. Nguyên tố s
B. Nguyên tố p
C. Nguyên tố d và nguyên tố f.
D. Nguyên tố s và nguyên tố p
Đáp án: D
Câu 10: Cho nguyên tố có kí hiệu là 12X. Vị trí của X trong bảng tuần hoàn:
A. Nhóm IIA, chu kì 3
B. Nhóm IA, chu kì 3
C. Nhóm IIIA, chu kì 2
D. Nhóm IA, chu kì 2
Đáp án: A
Trắc nghiệm Tính chất của kim loại, Dãy điện hóa của kim loại (có đáp án)
Câu 1: Kết luận nào sau đây là sai ?
A Kim loại có nhiệt độ nóng chảy thấp nhất là Hg.
B Kim loại dẻo nhất là natri.
C. Kim loại dẫn điện tốt nhất là bạc
D Kim loại nhẹ nhất là liti.
Đáp án: B
Kim loại dẻo nhất là vàng
Câu 2: Phát biểu nào sau đây không đúng ?
A. Kim loại cesi được dùng để làm tế bào quang điện
B. Kim loại crom được dùng để làm dao cát kính.
C. Kim loai bạc dược dùng để làm dây dẫn điện trong gia đình
D. Kim loại chì được dùng để chế tạo điện cực trong acquy.
Đáp án: C
Mặc dù bạc dẫn điện tốt nhưng do đắt nên không dùng làm dây dẫn điện
Câu 3: Cho các kim loại sau : Li, Mg, Al, Zn, Fe, Ni. Có bao nhiêu kim loại tác dụng với HCl và Cl2 thu được cùng một muối ?
A. 6 B. 3 C. 4 D. 5
Đáp án: D
Câu 4: Một học sinh tiến hành thí nghiệm : Nhúng một thanh đồng vào dung dịch AgNO3, sau một lúc nhúng tiếp một thanh sắt vào dung dịch này đến phản ứng hoàn toàn. Sau khi thí nghiệm kết thúc, học sinh đó rút ra các kết luận sau :
(I) Dung dịch thu được sau phản ứng có màu xanh nhạt.
(II) Khối lượng thanh đồng bị giảm sau phản ứng.
(III) Khối lượng thanh sắt tăng lên sau phản ứng.
Kết luận không đúng là
A. (I). B. (II). C. (III). D. (I) (II) và (III)
Đáp án: A
Sau phản ứng, dung dịch có màu xanh nhạt của ion Fe2+; khối lượng thanh đồng và sắt tăng lên
Câu 5: Hoà tan hoàn toàn a gam hỗn hờp gồm FeO và Fe2O3 (tỉ lệ mol 1:1) vào dung dịch HCl. Thêm tiếp b gam Cu vào dung dịch thu được ở trên thấy Cu tan hoàn toàn. Mối quan hệ giữa a và b là
A. 64a >232b. B. 64a < 232b. C. 64a > 116b. D. 64a < 116b.
Đáp án: A
phản ứng hoà tan hoàn toàn FeO và Fe2O3 ( tỉ lệ mol 1:1) vào dung dịch HCl
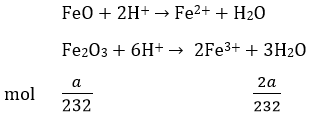
Hoà tan Cu vào dung dịch trên:
Cu + 2Fe3+ → Cu2+ + 2Fe2+
Khi Cu tan hoàn toàn tức là
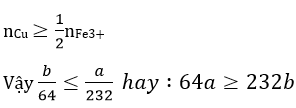
Câu 6: Thêm từ từ dung dịch H2SO4 đến dư vào cốc đựng hỗn hợp bột Zn và Fe, phản ứng là hoàn toàn. Mối quan hệ giữa số mol CuSO4 thêm vào và khối lượng chất rắn sau phản ứng có thể biểu diễn bằng đồ thị nào dưới đây ?
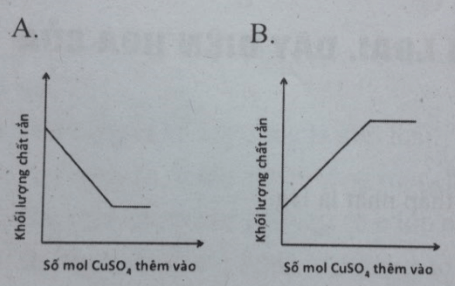
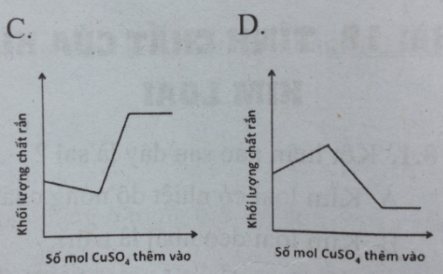
Đáp án: C
Ban đầu có phản ứng: Zn + Cu2+ → Zn2+ + Cu
Sau khi hết Zn, sẽ có phản ứng: Fe + Cu2+ → Fe2+ + Cu
Các chất tham gia và tạo thành trong phản ứng đều có tỉ lệ mol là 1:1
Vậy: ban đầu Cu(M = 64) thay thế Zn ( M=65) trong chất rắn, nên khối lượng chất rắn giảm
Sau khi Zn phản ứng hết, Fe bắt đầu phản ứng. Lúc này Cu (M = 64) thay hế Fe ( M = 56) trong chất rắn, nên khối lượng chất rắn tăng lên
Khi toàn bộ Fe đã phản ứng hết thì khối lượng chất rắn không thay đổi nữa
Câu 7: Cho m gam hỗn hợp bột Fe và Cu vào dung dịch AgNO3 dư. Khuấy kĩ cho đến khi phản ứng hoàn toàn thu được 35,64 gam kim loại. Mặt khác cũng cho m gam hỗn hợp trộn vào dung dịch CuSO4 dư, khuấy kĩ cho đến khi phản ứng kết thúc, thu được m + 0,72 gam kim loại. Giá trị của m là
A. 9,84. B. 8,34. C. 5,79. D. 6,96
Đáp án: D
Gọi số mol của Fe và Cu lần lượt là x và y
Xét phản ứng của Fe và Cu với AgNO3 dư, thu được 35,64 gam kim loại là Ag.

Bảo toàn e: 3x + 2y = 0,33 (1)
Xét phản ứng của Fe và Cu với CuSO4 dư:
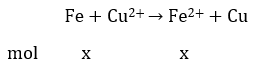
Khối lượng hỗn hợp tăng: 64x – 56x = 0,72 (2)
Kết hợp (1) và (2) giải ra x = 0,09 và y = 0,03
Khối lượng lim loại là 6,96 gam
Câu 8: Cho 2,8 gam bột sắt và 0,81 gam bột nhôm vào 100 ml dung dịch A chứa Cu(NO3)2 và AgNO3. Khuấy kĩ đến khi phản ứng hoàn toàn, thu được chất rắn B gồm 3 kim loại có khối lượng 8,12 gam. Cho B tác dụng với dung dịch HCl dư thu được 0,672 lít H2 (đktc). Nồng độ mol của Cu(NO3)2 là
A.0.3M. B.0,5M. C. 0,6M. D, 1M.
Đáp án: B
Chất rắn B gồm Ag, Cu, Fe với số mol lần lượt là x, y, z
Ta có: 108x + 64y + 56z = 8,12 (1)
Fe + 2HCl → FeCl2 + H2
nFe = nH2 = 0,03 mol => z= 0,03 mol (2)
từ (1) và (2) suy ra : 108x + 64 y = 6,44 (3)
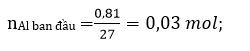
nFe ban đầu = 0,05 mol
nFe phản ứng = 0,05 – 0,03 = 0,02 mol
nAl phản ứng = 0,03 mol
theo bảo toàn e: x+ 2y = 0,03.3 + 0,02.2 = 0,13 (4)
từ (3) và (4) suy ra: x= 0,03, y= 0,05
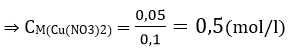
Câu 9: Có các phản ứng như sau :
1. Fe + 2H+ → Fe2+ + H2
2. Fe + Cl2 → FeCl2
3. AgNO3 + Fe(NO3)2 → Fe(NO3)3 + Ag
4. Ca + FeCl2 dung dịch → CaCl2 + Fe
5. Zn + 2FeCl3 → ZnCl2 + 2FeCl2
6. 3Fe dư + 8HNO3 loãng →3Fe(NO3)2 + 2NO + 4H2O
Trong các phản ứng trên, số phản ứng viết không đúng là
A. 1 B. 2. C. 3. D. 4.
Đáp án: B
phản ứng 2,4 không đúng
Câu 10: Cho các phát biểu sau :
1. Có thể dùng lưu huỳnh để khử độc thủy ngân.
2. Có thể dùng thùng bằng kẽm để vận chuyển HNO3 dặc, nguội.
3. Ngay cả ở nhiệt độ cao, magie không tác dụng với nước.
4. Bạc để lâu trong không khí có thể bị hoá đen do chuyển thành Ag2S.
Trong các phát biểu trên, số phát biếu đứng là
A. 1. B. 2. C. 3. D. 4.
Đáp án: B
phát biểu 1,4 đúng
Thi online Hóa 12 KNTTThi online Hóa 12 CDThi online Hóa 12 CTST
Xem thêm Bài tập & Câu hỏi trắc nghiệm Hóa học 12 có đáp án hay khác:
- 100 Bài tập trắc nghiệm Este; Lipit
- 100 Bài tập trắc nghiệm Cacbohidrat
- 100 Bài tập trắc nghiệm Amin, amino axit và protein
- 100 Bài tập trắc nghiệm Polime và vật liệu polime
- 100 Bài tập trắc nghiệm Kim loại kiềm, kim loại kiềm thổ, nhôm
- 100 Bài tập trắc nghiệm Sắt và một số kim loại quan trọng
- 100 Bài tập trắc nghiệm Phân biệt một số chất vô cơ
- 100 Bài tập trắc nghiệm Hóa học và vấn đề phát triển kinh tế, xã hội, môi trường
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Lớp 12 Kết nối tri thức
- Soạn văn 12 (hay nhất) - KNTT
- Soạn văn 12 (ngắn nhất) - KNTT
- Giải sgk Toán 12 - KNTT
- Giải sgk Vật Lí 12 - KNTT
- Giải sgk Hóa học 12 - KNTT
- Giải sgk Sinh học 12 - KNTT
- Giải sgk Lịch Sử 12 - KNTT
- Giải sgk Địa Lí 12 - KNTT
- Giải sgk Giáo dục KTPL 12 - KNTT
- Giải sgk Tin học 12 - KNTT
- Giải sgk Công nghệ 12 - KNTT
- Giải sgk Hoạt động trải nghiệm 12 - KNTT
- Giải sgk Giáo dục quốc phòng 12 - KNTT
- Giải sgk Âm nhạc 12 - KNTT
- Giải sgk Mĩ thuật 12 - KNTT
- Lớp 12 Chân trời sáng tạo
- Soạn văn 12 (hay nhất) - CTST
- Soạn văn 12 (ngắn nhất) - CTST
- Giải sgk Toán 12 - CTST
- Giải sgk Vật Lí 12 - CTST
- Giải sgk Hóa học 12 - CTST
- Giải sgk Sinh học 12 - CTST
- Giải sgk Lịch Sử 12 - CTST
- Giải sgk Địa Lí 12 - CTST
- Giải sgk Giáo dục KTPL 12 - CTST
- Giải sgk Tin học 12 - CTST
- Giải sgk Hoạt động trải nghiệm 12 - CTST
- Giải sgk Âm nhạc 12 - CTST
- Lớp 12 Cánh diều
- Soạn văn 12 Cánh diều (hay nhất)
- Soạn văn 12 Cánh diều (ngắn nhất)
- Giải sgk Toán 12 Cánh diều
- Giải sgk Vật Lí 12 - Cánh diều
- Giải sgk Hóa học 12 - Cánh diều
- Giải sgk Sinh học 12 - Cánh diều
- Giải sgk Lịch Sử 12 - Cánh diều
- Giải sgk Địa Lí 12 - Cánh diều
- Giải sgk Giáo dục KTPL 12 - Cánh diều
- Giải sgk Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 - Cánh diều
- Giải sgk Giáo dục quốc phòng 12 - Cánh diều
- Giải sgk Âm nhạc 12 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

