Công thức tính số khối lớp 10 (hay, chi tiết)
Bài viết Công thức tính số khối lớp 10 trình bày đầy đủ công thức, ví dụ minh họa có lời giải chi tiết và các bài tập tự luyện giúp học sinh nắm vững kiến thức trọng tâm về Công thức tính số khối từ đó học tốt môn Hóa học.
Công thức tính số khối lớp 10 (hay, chi tiết)
(199k) Xem Khóa học Hóa 10 KNTTXem Khóa học Hóa 10 CDXem Khóa học Hóa 10 CTST
I. Công thức tính số khối
Tổng số proton (P = Z) và tổng số neutron (N) trong hạt nhân của một nguyên tử được gọi là số khối (hay số nucleon), kí hiệu là A.
A = Z + N
Mở rộng:
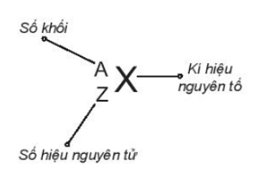
Để kí hiệu nguyên tử, người ta thường ghi các chỉ số đặc trưng ở bên trái kí hiệu nguyên tố với số khối A ở phía trên, số hiệu nguyên tử Z ở phía dưới.
II. Ví dụ minh họa tính số khối
Ví dụ 1: X là nguyên tố hóa học có trong thành phần của muối ăn. Nguyên tử X có tổng số các loại hạt bằng 52, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 16 hạt. X có số khối là?
Hướng dẫn giải
Gọi P, N và E lần lượt là số proton, neutron và electron của X. Trong đó P = E = Z.
Nguyên tử X có tổng số các loại hạt bằng 52 nên:
P + N + E = 52 hay 2P + N = 52 (1)
Trong nguyên tử X, số hạt mang điện nhiều hơn số hạt không mang điện là 16 hạt nên:
(P + E) – N = 16 hay 2P – N = 16 (2)
Từ (1) và (2) ta có hệ phương trình:
Vậy số khối của X là Z + N = 17 + 18 = 35.
Ví dụ 2: Tổng số hạt proton, neutron và electron trong nguyên tử X là 10. Nguyên tử X có số khối là?
A. 3.
B. 4.
C. 6.
D. 7.
Hướng dẫn giải
Đáp án đúng là: D
Trong X: số proton = số electron = số hiệu nguyên tử (Z)
Đặt số neutron trong X là N.
Với các nguyên tử bền ta có: (1)
Theo bài ra có:
Tổng số hạt proton, neutron và electron trong nguyên tử của nguyên tố X là 10 nên:
2Z + N = 10 ⇒ N = 10 – 2Z, thay vào (1) ta có:
⇔ Z ≤ 10 – 2Z ≤ 1,52Z ⇔ 2,84 ≤ Z ≤ 3,33
Vậy Z = 3 thỏa mãn ⇒ N = 4.
Số khối của X là Z + N = 7.
III. Bài tập minh họa tính số khối
Câu 1: Các hợp chất của nguyên tố Y được sử dụng như là vật liệu chịu lửa trong các lò sản xuất sắt, thép, kim loại màu, thủy tinh và xi măng. Oxide của Y và các hợp chất khác cũng được sử dụng trong nông nghiệp, công nghiệp hóa chất và xây dựng. Nguyên tử Y có tổng số các hạt là 36. Số hạt không mang điện bằng một nửa hiệu số giữa tổng số hạt với số hạt mang điện tích âm. Số khối của Y là
A. 12.
B. 24.
C. 36.
D. 40.
Hướng dẫn giải
Đáp án đúng là: B
Gọi P, N và E lần lượt là số proton, neutron và electron của Y. Trong đó P = E.
Theo bài ra ta có hệ phương trình:
Số khối của Y là A = P + N = 12 + 12 = 24.
Câu 2: Tổng số hạt cơ bản của 1 nguyên tử X là 82, trong đó tổng số hạt mang điện nhiều hơn số hạt không mang điện là 22. X có số khối là
A. 104.
B. 60.
C. 56.
D. 62.
Hướng dẫn giải
Đáp án đúng là: C
Gọi P, N và E lần lượt là số proton, neutron và electron của X. Trong đó P = E = Z.
Theo bài ra ta có hệ phương trình:
Số khối của X là: Z + N = 26 + 30 = 56.
Câu 3: Nguyên tử sắt (iron) có điện tích hạt nhân là +26. Trong nguyên tử, số hạt mang điện nhiều hơn số hạt không mang điện là 22. Số khối của nguyên tử sắt là
A. 26.
B. 30.
C. 56.
D. 22.
Hướng dẫn giải
Đáp án đúng là: C
Số hạt mang điện nhiều hơn số hạt không mang điện là 22 nên:
2Z – N = 22 (1)
Nguyên tử sắt có điện tích hạt nhân là +26 nên Z = 26
Thay Z = 26 vào (1) ta có N = 2.26 – 22 = 30
Số khối của nguyên tử sắt là:
A = Z + N = 26 + 30 = 56.
Câu 4: Trong nguyên tử một nguyên tố M có tổng số các loại hạt là 58. Biết trong ion M+ thì số hạt mang điện tích dương ít hơn số hạt không mang điện là 1 hạt. Số khối của M là
A. 38.
B. 39.
C. 19.
D. 40.
Hướng dẫn giải
Đáp án đúng là: B
Gọi P, N và E lần lượt là số proton, neutron và electron của M. Trong đó P = E = Z.
Trong nguyên tử một nguyên tố M có tổng số các loại hạt là 58 nên:
P + N + E = 58 hay 2P + N = 58 (1)
Trong ion M+ thì số hạt mang điện tích dương ít hơn số hạt không mang điện là 1 hạt nên: P + 1 = N (2)
Từ (1) và (2) giải hệ phương trình được P = 19 và N = 20.
Số khối của M là Z + N = 19 + 20 = 39.
Câu 5: Nguyên tử của một nguyên tố X có tổng số các loại bằng 115. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 25 hạt. Số khối của nguyên tử X là
A. 35.
B. 80.
C. 115.
D. 90.
Hướng dẫn giải
Đáp án đúng là: B
Gọi P, N và E lần lượt là số proton, neutron và electron của X. Trong đó P = E.
Theo bài ra ta có hệ phương trình:
Số hiệu nguyên tử: Z = số proton = 35
Số khối: A = Z + N = P + N = 80
Câu 6: Nitrogen giúp bảo quản tinh trùng, phôi, máu và tế bào gốc. Biết nguyên tử nitrogen có tổng số hạt là 21, trong đó số hạt không mang điện chiếm 33,33%. Nitrogen có số khối là
A. 21.
B. 14.
C. 7.
D. 28.
Hướng dẫn giải
Đáp án đúng là: B
Gọi P, N và E lần lượt là số proton, neutron và electron của nitrogen.
Trong đó P = E = Z.
Số hạt không mang điện chiếm 33,33%
⇒ Số neutron = N =
Lại có: P + E + N = 21 ⇒ 2P + N = 21 (2)
Thế N = 7 vào (2) được P = 7.
Số khối của nitrogen là: Z + N = 7 + 7 = 14.
Câu 7: Nguyên tử X có khối lượng là 3,173.10-23g. Trong X, số neutron nhiều hơn số proton 1 hạt. Số khối của X là
(cho mp ≈ mn ≈ 1,67.10-27kg, me ≈ 9,1.10-31kg)
A. 19.
B. 10.
C. 8.
D. 9.
Hướng dẫn giải
Đáp án đúng là: A
Gọi số proton, số neutron trong nguyên tử X lần lượt là P, N.
Ta có: mnguyên tử ≈ mhạt nhân = mcác proton + mcác neutron
⇔ 3,173.10-23 = (P + N).1,67.10-27.103 ⇔ P + N = 19 (1)
Lại có N – P = 1 (2)
Từ (1) và (2) giải hệ phương trình ta được: P = 9; N = 10.
Số khối của X là: Z + N = P + N = 9 + 10 = 19.
Câu 8: Nguyên tử của nguyên tố A có 56 electron, trong hạt nhân có 81 neutron. Kí hiệu của nguyên tử nguyên tố A là
A.
B.
C.
D.
Hướng dẫn giải:
Đáp án đúng là: A
Số khối (A) = 56 + 81 = 137.
Số hiệu nguyên tử (Z) = số electron = 56.
Vậy kí hiệu nguyên tử:
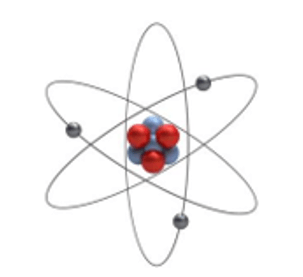
Câu 9: Cho hình vẽ nguyên tử:
Kí hiệu nguyên tử nào sau đây là đúng?
A.
B.
C.
D.
Hướng dẫn giải
Đáp án đúng là: A
Quan sát hình vẽ xác định được nguyên tử Li có:
+ Số proton = số electron = 3 → Số hiệu nguyên tử (Z) = 3.
+ Số neutron = 4.
+ Số khối (A) = số proton + số neutron = 3 + 4 = 7.
Vậy kí hiệu nguyên tử là:
Câu 10: Tổng số hạt proton, neutron và electron trong là
A. 19.
B. 28.
C. 30.
D. 32.
Hướng dẫn giải
Đáp án đúng là: B
Dựa vào kí hiệu nguyên tử xác định được:
+ Số proton = số electron = số hiệu nguyên tử = 9.
+ Số neutron = số khối – số proton = 19 – 9 = 10.
Vậy tổng số hạt proton, neutron và electron trong là: 9 + 10 + 9 = 28.
(199k) Xem Khóa học Hóa 10 KNTTXem Khóa học Hóa 10 CDXem Khóa học Hóa 10 CTST
Xem thêm các bài viết về công thức Hóa học 10 hay, chi tiết khác:
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài 500 Công thức, Định Lí, Định nghĩa Toán, Vật Lí, Hóa học, Sinh học được biên soạn bám sát nội dung chương trình học các cấp.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)









 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

