Chuyên đề Hợp chất carbonyl - carboxylic acid lớp 11
Tài liệu chuyên đề Hợp chất carbonyl - carboxylic acid Hóa học lớp 11 gồm các dạng bài tập từ cơ bản đến nâng cao với phương pháp giải chi tiết và bài tập tự luyện đa dạng giúp Giáo viên có thêm tài liệu giảng dạy Hóa học 11.
Chuyên đề Hợp chất carbonyl - carboxylic acid lớp 11
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Xem thử chuyên đề Hóa học 11 KNTT
Chỉ từ 450k mua trọn bộ Chuyên đề dạy thêm Hóa học 11 (cả 3 sách) bản word có lời giải chi tiết:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận giáo án
Hợp chất carbonyl
I. Khái niệm, phân loại và danh pháp
- Hợp chất cabonyl là những hợp chất hữu cơ trong phân tử có chứa nhóm carbonyl (>C=O).
Aldehyde |
Ketone |
|
Khái niệm |
- Aldehyde là hợp chất hữu cơ có nhóm -CHO liên kết trực tiếp với nguyên tử C (của gốc hydrocarbon hoặc nhóm -CHO) hoặc nguyên tử H. - CT aldehyde đơn chức: R – CHO (R là H, gốc HC, nhóm -CHO) |
- Ketone là hợp chất hữu cơ có nhóm carbonyl (>C=O) liên kết với hai gốc hydrocarbon. - CT ketone đơn chức: R – CO – R’ (R, R’ là gốc HC) |
Phân loại |
♦ Aldehyde no, đơn chức, mạch hở: CnH2nO (n≥ 0) hay CmH2m+1CHO (m ≥ 0) ♦ Aldehyde không no: CH2=CH-CHO, … ♦ Aldehyde thơm: C6H5CHO, … ♦ Aldehyde đa chức: (CHO)2, … |
♦ Ketone no: CH3 – CO – CH3, … ♦ Ketone không no: CH2=CH-CO-CH3 ♦ Ketone thơm: CH3 – CO – C6H5 ♦ Ketone đa chức: CH3 – CO – CH2 – CO – CH3 |
Danh pháp |
Tên thay thế aldehyde đơn chức, mạch hở = Tên hydrocarbon (bỏ e cuối) + al Tên thay thế ketone đơn chức, mạch hở = Tên hydrocarbon (bỏ e cuối) + VT >C=O + one Chú ý: + Mạch chính là mạch dài nhất chứa nhóm >C=O. + Đánh số carbon trên mạch chính từ phía gần nhóm >C=O nhất. + Nếu mạch carbon có nhánh thì cần thêm vị trí nhánh và tên nhánh ở phía trước |
|
MỘT SỐ ALDEHYDE, KETONE THƯỜNG GẶP
ALDEHYDE | ||
Công thức |
Tên thay thế |
Tên thông thường |
HCHO |
methanal |
formic aldehyde (formaldehyde) |
CH3CHO |
ethanal |
acetic aldehyde (acetaldehyde) |
CH3CH2CHO |
propanal |
propionic aldehyde (propionaldehyde) |
CH2=CHCHO |
propenal |
acrylic aldehyde (acrylaldehyde) |
C6H5CHO |
phenylmethanal |
benzoic aldehyde (benzaldehyde) |
C6H5CH=CHCHO |
phenylpropenal |
cinnamic aldehyde (cinnamaldehyde) |
KETONE | ||
Công thức |
Tên thay thế |
Tên thông thường |
CH3COCH3 |
propanone |
acetone |
C6H5COCH3 |
1-phenylethan-1-one |
acetophenone |
C6H5COC6H5 |
diphenylmethanone |
benzophenone |
II. Đặc điểm cấu tạo
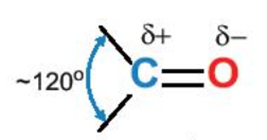
- Aldehyde, ketone chứa liên kết đôi C=O phân cực về phía O.
Cấu trúc nhóm >CO |
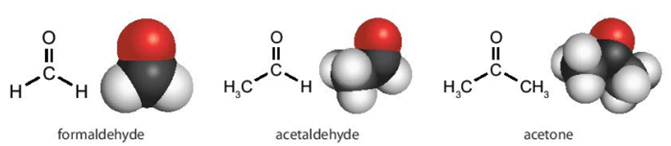
Mô hình phân tử |
III. Tính chất vật lí
- Ở điều kiện thường, HCHO, CH3CHO ở trạng thái khí, các aldehyde, ketone khác là những chất lỏng hoặc rắn.
- HCHO, CH3CHO, CH3COCH3 tan vô hạn trong nước do tạo được liên kết hydrogen với nước, các aldehyde, ketone mạch C lớn hơn thì độ tan giảm dần.
- Nhiệt độ nóng chảy, nhiệt độ sôi cao hơn hydrocarbon có phân tử khối tương đương do aldehyde, ketone phân cực.
IV. Tính chất hóa học
1. Phản ứng khử aldehyde, ketone
- Aldehyde bị khử bởi NaBH4 hoặc NaAlH4 thành ancol bậc I: R – CHO R – CH2OH
- Ketone bị khử bởi NaBH4 hoặc NaAlH4 thành ancol bậc II: RCOR’ R – CHOH – R’
2. Phản ứng oxi hóa aldehyde
- Aldehyde dễ bị oxi hóa bởi Br2/H2O, [Ag(NH3)2]OH, Cu(OH)2/OH-, …. Ketone không có phản ứng này.
(a) Phản ứng với nước bromine (Br2/H2O)
TQ: RCHO + Br2 + H2O → RCOOH + 2HBr
Aldehyde làm mất màu nước bromine.
(b) Phản ứng với AgNO3/NH3 (thuốc thử Tollens)
TQ: RCHO + 2[Ag(NH3)2]OH RCOONH4 + 2Ag↓ + 3NH3 + H2O
Phản ứng tạo thành Ag sáng bóng bám vào ống nghiệm nên còn gọi là phản ứng tráng bạc.
Chú ý: Các aldehyde đơn chức tráng bạc cho 2Ag, riêng HCHO cho 4Ag.
(c) Phản ứng với copper (II) hydroxide
TQ: RCHO + 2Cu(OH)2 + NaOH RCOONa + Cu2O↓ đỏ gạch + 3H2O
Nước bromine, thuốc thử Tollens, Cu(OH)2 đều là các thuốc thử nhận biết aldehyde và ketone.
3. Phản ứng cộng hydrogen cyanide (HCN)
- Hợp chất carbonyl có thể tham gia phản ứng cộng HCN vào liên kết đôi C=O.
4. Phản ứng tạo iodoform
- Hợp chất chứa nhóm methyl ketone (CH3CO -) có phản ứng với I2 trong môi trường kiềm tạo ra kết tủa iodoform (CHI3) màu vàng <![if !vml]><![endif]> PƯ dùng để nhận biết các hợp chất chứa nhóm CH3CO-.
TQ: CH3CO – R + 3I2 + 4NaOH → RCOONa + 3NaI + CHI3↓ vàng + 3H2O
- Phản ứng trên còn gọi là phản ứng iodoform.
V. Ứng dụng và điều chế
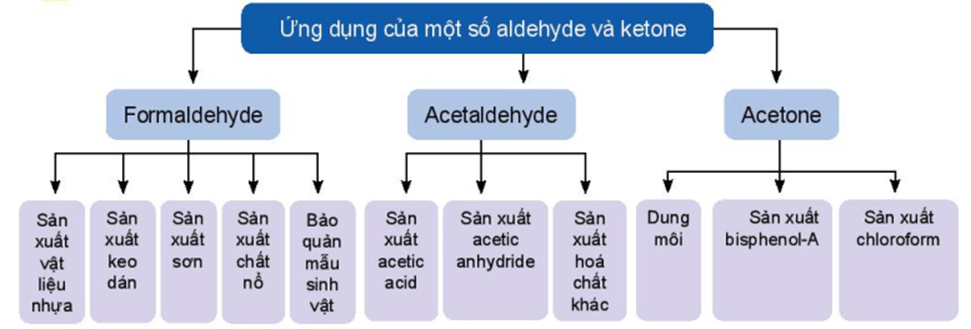
1. Ứng dụng
2. Điều chế
- Acetaldehyde: 2CH2=CH2 + O2 2CH3-CHO
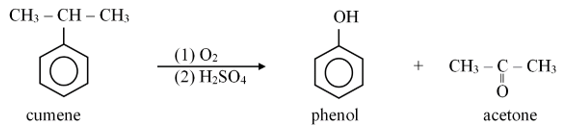
- Acetone:
Carboxylic acid
I. Khái niệm, phân loại, danh pháp
1. Khái niệm
- Carboxylic acid là những hợp chất hữu cơ trong phân tử chứa nhóm carboxyl (-COOH) liên kết trực tiếp với nguyên tử carbon (của gốc hydrocarbon hoặc -COOH) hoặc nguyên tử hydrogen.
- CT carboxylic acid đơn chức: 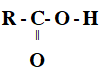
2. Phân loại
♦ Carboxylic acid no, đơn chức, mạch hở: CnH2nO2 (n ≥ 1) hay CmH2m+1COOH (m ≥ 0)
♦ Carboxylic acid không no: CH2=CH-COOH, …
♦ Carboxylic acid thơm: C6H5COOH, …
♦ Carboxylic acid đa chức: (COOH)2, …
3. Danh pháp
(a) Tên thay thế carboxylic acid đơn chức = Tên hydrocarbon (bỏ e ở cuối) + oic + acid
- Mạch chính là mạch dài nhất có chứa nhóm -COOH và đánh số carbon bắt đầu từ nhóm -COOH
- Nếu mạch carbon có nhánh thì thêm vị trí nhánh và tên nhánh ở phía trước.
(b) Tên thông thường
- Một số carboxylic acid có tên thông thường xuất phát từ nguồn gốc tìm ra chúng trong tự nhiên.
MỘT SỐ CARBOXYLIC ACID THƯỜNG GẶP
Công thức |
Tên thay thế |
Tên thông thường |
Nguồn gốc |
HCOOH |
methanoic acid |
formic acid |
formica: con kiến |
CH3COOH |
ethanoic acid |
acetic acid |
acetum: giấm ăn |
C2H5COOH |
propanoic acid |
propionic acid |
propion: chất béo đầu tiên |
CH2=CH-COOH |
Propenoic acid |
acrylic acid |
|
CH2=C(CH3)-COOH |
methylpropenoic acid |
methacrylic acid |
|
CH3[CH2]14COOH |
hexadecanoic acid |
palmitic acid |
palma: cây cọ |
CH3[CH2]16COOH |
octadecanoic acid |
stearic acid |
stear: chất béo dạng rắn |
C6H5COOH |
phenylmethanoic acid |
benzoic acid |
benzoin: tên nhựa cây |
HOOC – COOH |
ethanedioic acid |
oxalic acid |
oxalis: tên chi thực vật |
II. Đặc điểm cấu tạo
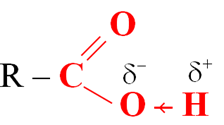
- Nhóm carboxyl gồm nhóm hydroxy (-OH) liên kết với nhóm carbonyl (>C=O). Nhóm >C=O hút electron mạnh làm tăng sự phân cực của liên kết O – H về phía O hơn so với trong ancol, phenol.
Nhóm -COOH dễ phân li ra H+ trong nước nên thể hiện tính acid đặc trưng.
Cấu tạo nhóm -COOH |
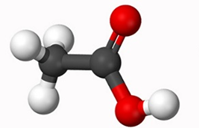
Mô hình phân tử acetic acid |
III. Tính chất vật lí
- Ở điều kiện thường, carboxylic acid là những chất lỏng hoặc rắn.
- Giữa các phân tử carboxylic acid có liên kết hydrogen bền vững hơn alcohol nên carboxylic acid có nhiệt độ nóng chảy, nhiệt độ sôi cao hơn alcohol, phenol, aldehyde, ketone có khối lượng phân tử tương đương.
Nếu cùng số C thì nhiệt độ sôi: carboxylic acid > alcohol > aldehyde > hydrocarbon.
- Do tạo được liên kết hydrogen với nước nên carboxylic tan tốt trong nước, độ tan trong nước giảm khi số C tăng.
- Mỗi carboxylic có một vị chua riêng biệt: acetic acid (giấm), oxalic acid (me), citric acid (chanh), …
IV. Tính chất hóa học
1. Tính acid
Carboxylic acid tan trong nước phân li ra H+ thể hiện tính acid: RCOOH RCOO- + H+
♦ Carboxylic acid làm đổi màu quỳ tím → đỏ.
♦ Tác dụng với kim loại trước H → Muối + H2.
♦ Tác dụng với basic oxide/ base → Muối + H2O.
♦ Tác dụng với muối → Muối mới + acid mới
2. Phản ứng ester hóa
- Phản ứng giữa carboxylic acid và alcohol tạo thành ester gọi là phản ứng ester hóa.
- Phản ứng ester hóa xảy ra thuận nghịch và có H2SO4 đặc làm xúc tác.
RCOOH + R’OH RCOOR’ + H2O
carboxylic acid alcohol ester
V. Ứng dụng và điều chế
1. Ứng dụng
2. Điều chế
- Lên men giấm: C2H5OH + O2 CH3COOH + H2O
- Oxi hóa alkane: RCH2 – CH2R’ + 2,5O2 RCOOH + R’COOH + H2O
A. CÁC BÀI TẬP TỰ LUẬN
Câu 1. Hãy chỉ ra hợp chất carboxylic acid trong số các chất sau: (1) CH3CHO, (2) C6H5OH, (3) CH2=CHCOOH, (4) HOOC-COOH, (5) HCOOH, (6) HO – CH2 – CH2 – OH.
Câu 2. [CTST - SGK] Viết công thức cấu tạo của các đồng phân acid có công thức phân tử C5H10O2. Gọi tên theo danh pháp thay thế của các đồng phân đó
Câu 3.Hoàn thành thông tin còn thiếu trong bảng sau:
Công thức cấu tạo thu gọn |
Tên thay thế |
(CH3)2CH – COOH |
|
(CH3)3C – COOH |
|
CH3CH=CH – COOH |
|
CH3CH=C(CH3) – COOH |
|
pentanoic acid |
|
but-3-enoic acid |
|
2-methylbutanoic acid |
|
2,2-dimethylpropanoic acid |
Câu 4. [CTST - SGK]
(a)So sánh nhiệt độ sôi của butanoic acid với nhiệt độ sôi của các chất trong bảng sau. Giải thích.
Chất |
Công thức |
Nhiệt độ sôi (oC) |
Butane |
CH3CH2CH2CH3 |
-0,5 |
Butanal |
CH3CH2CH2CHO |
76 |
Butan – 1 – ol |
CH3CH2CH2CH2OH |
117,7 |
Butanoic acid |
CH3CH2CH2COOH |
163,0 |
(b) Vì sao acetic acid tan vô hạn trong nước?
(c) Hãy sắp xếp theo chiều tăng dần nhiệt độ sôi của các chất sau, giải thích: (1) C3H8, (2) C2H5COOH, (3) C2H5CHO, (4) C3H7OH.
Câu 5. [CTST - SGK]
(1) Từ đặc điểm cấu tạo nhóm carboxyl, dự đoán tính chất hóa học đặc trưng của hợp chất carboxylic acid.
(2) Biết Ka (hằng số phân li acid) của R-COOH theo biểu thức sau: . Dựa vào bảng sau nhận xét về tính acid của các carboxylic acid. Nêu tính chất hóa học đặc trưng của chúng.
Carboxylic acid |
Ka |
HCOOH |
1,6.10-4 |
CH3COOH |
1,3.10-5 |
CH3CH2COOH |
1,34.10-5 |
CH3CH2CH2COOH |
1,55.10-5 |
C6H5COOH |
6,6.10-5 |
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Xem thêm Chuyên đề dạy thêm Hóa học lớp 11 các chương hay khác:
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 11 Global Success
- Giải sgk Tiếng Anh 11 Smart World
- Giải sgk Tiếng Anh 11 Friends Global
- Lớp 11 - Kết nối tri thức
- Soạn văn 11 (hay nhất) - KNTT
- Soạn văn 11 (ngắn nhất) - KNTT
- Giải sgk Toán 11 - KNTT
- Giải sgk Vật Lí 11 - KNTT
- Giải sgk Hóa học 11 - KNTT
- Giải sgk Sinh học 11 - KNTT
- Giải sgk Lịch Sử 11 - KNTT
- Giải sgk Địa Lí 11 - KNTT
- Giải sgk Giáo dục KTPL 11 - KNTT
- Giải sgk Tin học 11 - KNTT
- Giải sgk Công nghệ 11 - KNTT
- Giải sgk Hoạt động trải nghiệm 11 - KNTT
- Giải sgk Giáo dục quốc phòng 11 - KNTT
- Giải sgk Âm nhạc 11 - KNTT
- Lớp 11 - Chân trời sáng tạo
- Soạn văn 11 (hay nhất) - CTST
- Soạn văn 11 (ngắn nhất) - CTST
- Giải sgk Toán 11 - CTST
- Giải sgk Vật Lí 11 - CTST
- Giải sgk Hóa học 11 - CTST
- Giải sgk Sinh học 11 - CTST
- Giải sgk Lịch Sử 11 - CTST
- Giải sgk Địa Lí 11 - CTST
- Giải sgk Giáo dục KTPL 11 - CTST
- Giải sgk Hoạt động trải nghiệm 11 - CTST
- Giải sgk Âm nhạc 11 - CTST
- Lớp 11 - Cánh diều
- Soạn văn 11 Cánh diều (hay nhất)
- Soạn văn 11 Cánh diều (ngắn nhất)
- Giải sgk Toán 11 - Cánh diều
- Giải sgk Vật Lí 11 - Cánh diều
- Giải sgk Hóa học 11 - Cánh diều
- Giải sgk Sinh học 11 - Cánh diều
- Giải sgk Lịch Sử 11 - Cánh diều
- Giải sgk Địa Lí 11 - Cánh diều
- Giải sgk Giáo dục KTPL 11 - Cánh diều
- Giải sgk Tin học 11 - Cánh diều
- Giải sgk Công nghệ 11 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 11 - Cánh diều
- Giải sgk Giáo dục quốc phòng 11 - Cánh diều
- Giải sgk Âm nhạc 11 - Cánh diều

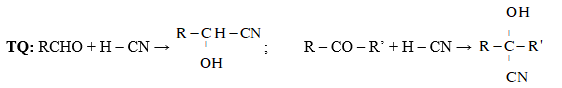





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

