Phương pháp đường chéo trong hóa học cực (chi tiết, có lời giải)
Bài viết Phương pháp đường chéo trong hóa học cực với phương pháp giải chi tiết giúp học sinh ôn tập, biết cách làm bài tập Phương pháp đường chéo trong hóa học cực.
Phương pháp đường chéo trong hóa học cực (chi tiết, có lời giải)
Thi online Hóa 12 KNTTThi online Hóa 12 CDThi online Hóa 12 CTST
Phương pháp giải
1. Nội dung
+ Phương pháp này áp dụng cho các bài toán hỗn hợp chứa 2 thành phần mà yêu cầu của bài là xác định tỉ lệ giữa 2 thành phần đó.
+ Ta có thể sử dụng đặt ẩn – giải hệ để thay thế cho phương pháp đường chéo, tuy nhiên áp dụng đường chéo hợp lí, đúng cách trong nhiều bài toán sẽ giúp tốc độ làm bài nhanh hơn.
2. Phạm vi sử dụng
+ Bài toán về đồng vị: Ta áp dụng sơ đồ đường chéo cho đại lượng khối lượng phân tử và số khối
+ Bài toán hỗn hợp khí: Ta áp dụng sơ đồ đường chéo cho tỉ lệ mol tương ứng với tỉ lệ chênh lệch phân tử khối các chất so với giá trị trung bình
+ Bài toán pha chế: Ta áp dụng sơ đồ đường chéo cho các đại lượng C%, CM, d,…
+ Bài toán xác định công thức, tính tỉ lệ các chất: Ta áp dụng cho các đại lượng, phân tử khối trung bình, số nguyên tử trung bình,…
Ví dụ minh họa
Ví dụ 1: Để pha được 500 ml dung dịch nước muối sinh lí (C = 0,9%) cần lấy V ml dung dịch NaCl 3%. Giá trị của V là:
A. 150
B. 214,3
C. 285,7
D. 350
Giải:
Ta có sơ đồ:
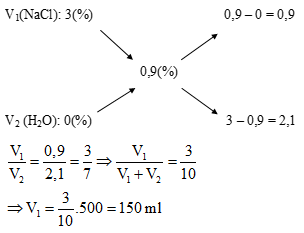
⇒ Đáp án A
Ví dụ 2: Nguyên tử khối trung bình của brom là 79,319. Brom có hai đồng vị bền: 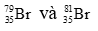
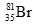
A. 84,05
B. 81,02
C. 18,98
D. 15,95
Giải
Ta có sơ đồ đường chéo:
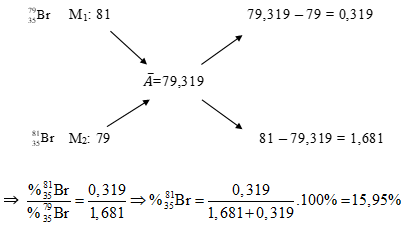
⇒ Đáp án D
Ví dụ 3: Đốt cháy 0,1 mol hỗn hợp X gồm CH4, C2H4 và C2H6, sản phẩm thu được dẫn qua bình I đựng dung dịch H2SO4 đặc bình II đựng dung dịch Ca(OH)2 dư. Sau thí nghiệm, thấy bình 2 có 15g kết tủa và khối lượng bình 2 nặng hơn khối lượng bình 1 là 2,55g. Thành phần % về thể tích của mỗi khí trong hỗn hợp là:
A. 50%, 30%, 20%
B. 30%, 40%, 30%
C. 50%, 25%, 25%
D. 50%, 15%, 35%
Giải:
Bình 1 khối lượng tăng là do hấp thụ H2O, bình 2 khối lượng tăng là do hấp thụ CO2
n CO2 = 15 : 100 = 0,15 mol
⇒ m H2O = 0,15.44 – 2,55 = 4,05 ⇒ n H2O = 0,225 mol
Gọi công thức trung bình của hỗn hợp X là: 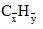
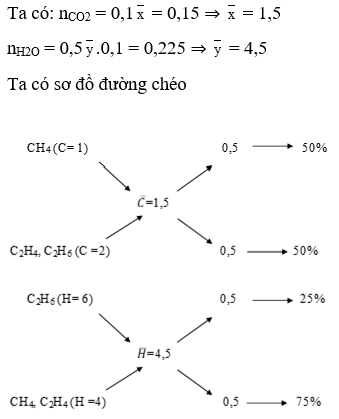
⇒ Đáp án C
Ví dụ 4: Cho hỗn hợp gồm H2, N2 và NH3 có tỉ khối hơi so với H2 bằng 8 đi qua bình đựng dung dịch H2SO4 đặc, dư thì thể tích khí còn lại một nửa. Thành phần % thể tích của mỗi khí trong hỗn hợp lần lượt là:
A. 25%, 25%, 50%
B. 20%, 30%, 50%
C. 50%, 25%, 25%
D. 15%, 35%, 50%
Giải:
Khi cho hỗn hợp qua bình đựng H2SO4 đặc thì NH3 bị giữ lại phản ứng, thể tích giảm đi một nửa
⇒ VNH3 = ½ Vhỗn hợp ⇒ %VNH3 = 50%
Gọi khối lượng phân tử trung bình của H2 và N2 là 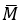
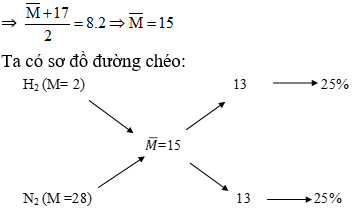
⇒ Đáp án A
Ví dụ 5: Đốt cháy hoàn toàn hỗn hợp 2 hydrocarbon đồng đẳng liên tiếp, thu được 0,9 mol CO2 và 1,4 mol H2O. Thành phần % về thể tích của mỗi chất trong hỗn hợp ban đầu lần lượt là:
A. 25% và 75%
B. 20% và 80%
C. 40% và 60%
D. 15% và 85%
Giải:
Vì n CO2 < n H2O ⇒ 2 hydrocarbon là alkane.
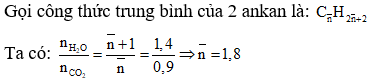
⇒ 2 alkane là: CH4 và C2H6
Ta có sơ đồ đường chéo:
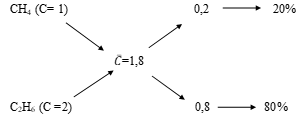
⇒ Đáp án B
Bài tập tự luyện
Bài 1: Hoà tan 28,4g 1 hỗn hợp 2 muối carbonate của 2 kim loại hoá trị II bằng dung dịch HCl dư, thu được 6,72 lít khí ở đktc và dung dịch A. % khối lượng muối có phân tử khối nhỏ hơn trong hỗn hợp ban đầu là:
A. 74,2%
B. 33,3%
C. 70,4%
D. 29,6%
Lời giải:
Hướng dẫn giải:
Gọi công thức chung 2 muối carbonate: MCO3
n CO2 = 0,3 mol
⇒ n MCO3 = 0,3 mol
⇒ MCO3 = 94,67
⇒ M = 34,67
⇒ 2 kim loại là Mg và Ca
Ta có sơ đồ đường chéo:
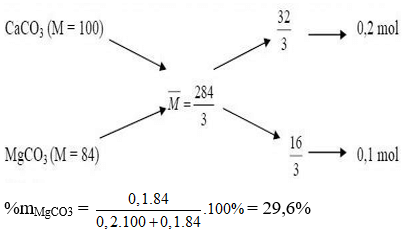
⇒ Đáp án D
Bài 2: Cần trộn 2 thể tích methane với một thể tích đồng đẳng X của methane để thu được hỗn hợp khí có tỉ khối hơi so với hiđro bằng 15. X là:
A. C3H8
B. C4H10
C. C5H12
D. C6H14
Lời giải:
Hướng dẫn giải:
Ta có sơ đồ đường chéo:
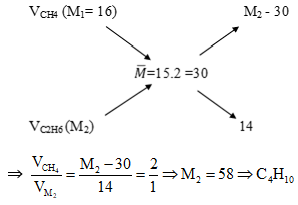
⇒ Đáp án B
Bài 3: Thêm 250 ml dung dịch NaOH 2M vào 200 ml dung dịch H3PO4 1,5M. Muối tạo thành và khối lượng tương ứng là:
A. 14,2 gam Na2HPO4; 32,8 gam Na3PO4
B. 28,4 gam Na2HPO4; 16,4 gam Na3PO4
C. 12,0 gam NaH2PO4; 28,4 gam Na2HPO4
D. 24,0 gam NaH2PO4; 14,2 gam Na2HPO4
Lời giải:
Hướng dẫn giải:
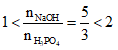
⇒ Tạo ra hỗn hợp 2 muối: NaH2PO4, Na2HPO4
Sơ đồ đường chéo:
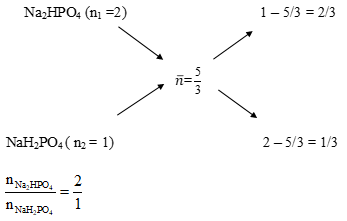
Mà: n Na2HPO4 + n NaH2PO4 = n H3PO4 = 0,3 mol
⇒ n Na2HPO4 =0,2 mol; n NaH2PO4 = 0,1 mol
⇒ m Na2HPO4 =0,2.142 = 28,4g;
m NaH2PO4 = 0,1.120 = 12g
⇒ Đáp án C
Bài 4: Cho 12,20g hỗn hợp X gồm ethanol và propane – 1- ol tác dụng với Na thu được 2,8 lít khí (đktc). Thành phần % khối lượng của mỗi chất trong X lần lượt là:
A. 75,4% và 24,6%
B. 25% và 75%
C. 24,6% và 75,4%
D. 75% và 25%
Lời giải:
Hướng dẫn giải:
n H2 = 0,125 mol ⇒ n X = 0,25
⇒ M− = 12,20 : 0,25 = 48,8
Ta có sơ đồ đường chéo:
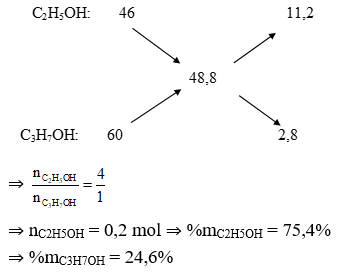
⇒ Đáp án A
Bài 5: Cần bao nhiêu lít axit H2SO4 (d = 1,84) và bao nhiêu lít nước cất (d = 1) để pha thành 9 lít dung dịch H2SO4 có d = 1,28?
A. 2 lít và 7 lít
B. 3 lít và 6 lít
B. 4 lít và 5 lít
D. 6 lít và 3 lít
Lời giải:
Hướng dẫn giải:
Ta có sơ đồ đường chéo:
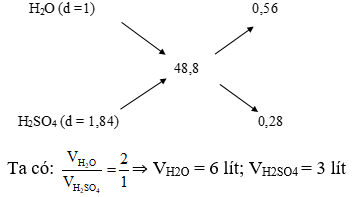
⇒ Đáp án B
Bài 6: Một loại rượu có tỉ khối d = 0,95 thì độ rượu của nó là bao nhiêu? Biết tỉ khối của nước và rượu nguyên chất lần lượt là 1 và 0,8
A. 25,5
B. 12,5
C. 50
D. 25
Lời giải:
Hướng dẫn giải:
Ta có sơ đồ đượng chéo
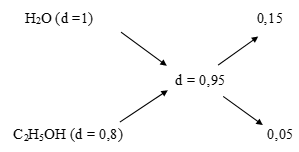
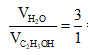
⇒ Độ rượu = 25 ⇒ Đáp án D
Bài 7: Khối lượng nguyên tử trung bình của Bo là 10,812. Hỏi khi có 94 nguyên tử 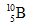
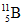
A. 188
B. 406
C. 812
D. 94
Lời giải:
Hướng dẫn giải:
Ta có sơ đồ đường chéo:
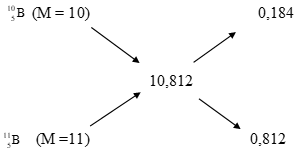
⇒ Số nguyên tử 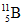
⇒ Đáp án B
Bài 8: Hỗn hợp khí X gồm alkene M và alkyne N có cùng số nguyên tử C trong phân tử. Hỗn hợp X có khối lượng 12,4g và thể tích 6,72 lít (đktc). Số mol, công thức phân tử M và N lần lượt là:
A. 0,1 mol C2H4 và 0,2 mol C2H2
B. 0,2 mol C2H4 và 0,1 mol C2H2
B. 0,1 mol C3H6 và 0,2 mol C3H4
C. 0,2 mol C3H6 và 0,1 mol C3H4
Lời giải:
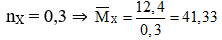
Hướng dẫn giải:
Vậy alkene là C3H6 (42) và alkyne là C3H4 (40)
Ta có sơ đồ đường chéo:
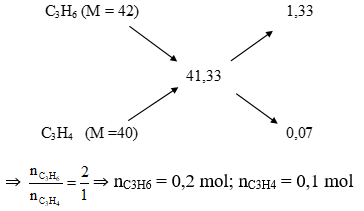
⇒ ⇒ n C3H6 = 0,2 mol; n C3H4 = 0,1 mol
⇒ Đáp án C
Bài 9: Điện phân nóng chảy Al2O3 với anot bằng than chì (H = 100%) thu được m kg Al và 67,2m3 (đktc) hỗn hợp khí X có tỉ khối so với H2 bằng 16. Lấy 2,24 lít (đktc) hỗn hợp khí X sục vào dung dịch nước vôi trong dư thu được 2g kết tủa. Gía trị của m là:
A. 67,5
B. 54
C. 75,6
D. 108
Lời giải:
Hướng dẫn giải:
M(tb)=32 ⇒ Hỗn hợp phải có CO (M =28) và n CO2 = 0,02
⇒ n CO + n O2 = 0,1 – 0,02 = 0,08
Gọi phân tử khối trung bình của CO và O2 là: M'(tb)
Ta có sơ đồ đường chéo:
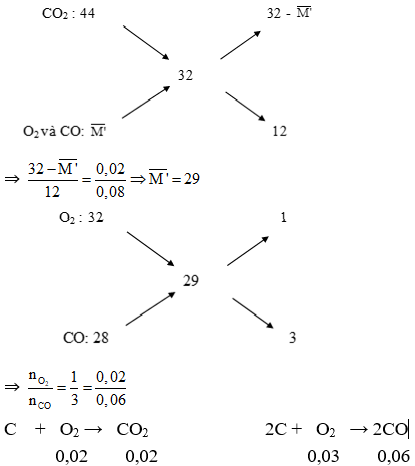
n O2 = 0,02 + 0,03 + 0,02 = 0,07
2Al2O3 → 4Al + 3O2
⇒ n Al = 2,8Kmol ⇒ m Al = 75,6Kg
⇒ Đáp án C
Bài 10: Nung 56,25g CaCO3 ở 1000°C và cho toàn bộ lượng khí thoát ra hấp thụ hết vào 500ml dung dịch NaOH 1,8M. Khối lượng muối thu được là:
A. 8,4g
B. 42,4g
C. 50,8
D. 59,625g
Lời giải:
Hướng dẫn giải:
n CO2 = 0,5 mol; n NaOH = 0,9 mol
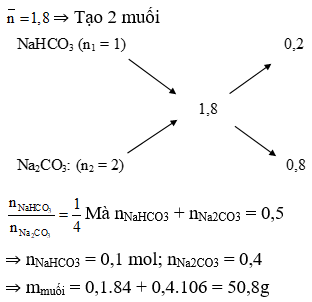
⇒ Đáp án C
Thi online Hóa 12 KNTTThi online Hóa 12 CDThi online Hóa 12 CTST
Xem thêm các phương pháp giải nhanh bài tập Hóa học hay khác:
- Phương pháp bảo toàn điện tích trong hóa học hay, chi tiết, có lời giải
- Phương pháp bảo toàn electron trong hóa học hay, chi tiết, có lời giải
- Phương pháp bảo toàn khối lượng trong hóa học cực hay, có lời giải
- Phương pháp bảo toàn nguyên tố trong hóa học cực hay, có lời giải
- Phương pháp chọn đại lượng thích hợp trong hóa học cực hay, có lời giải
- Phương pháp đồ thị trong hóa học hay, chi tiết, có lời giải
- Phương pháp trung bình trong hóa học cực hay, chi tiết, có lời giải
- Phương pháp quy đổi trong hóa học cực hay, chi tiết, có lời giải
- Phương pháp sử dụng phương trình ion thu gọn trong hóa học cực hay, có lời giải
- Phương pháp tăng giảm khối lượng trong hóa học cực hay, có lời giải
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Lớp 12 Kết nối tri thức
- Soạn văn 12 (hay nhất) - KNTT
- Soạn văn 12 (ngắn nhất) - KNTT
- Giải sgk Toán 12 - KNTT
- Giải sgk Vật Lí 12 - KNTT
- Giải sgk Hóa học 12 - KNTT
- Giải sgk Sinh học 12 - KNTT
- Giải sgk Lịch Sử 12 - KNTT
- Giải sgk Địa Lí 12 - KNTT
- Giải sgk Giáo dục KTPL 12 - KNTT
- Giải sgk Tin học 12 - KNTT
- Giải sgk Công nghệ 12 - KNTT
- Giải sgk Hoạt động trải nghiệm 12 - KNTT
- Giải sgk Giáo dục quốc phòng 12 - KNTT
- Giải sgk Âm nhạc 12 - KNTT
- Giải sgk Mĩ thuật 12 - KNTT
- Lớp 12 Chân trời sáng tạo
- Soạn văn 12 (hay nhất) - CTST
- Soạn văn 12 (ngắn nhất) - CTST
- Giải sgk Toán 12 - CTST
- Giải sgk Vật Lí 12 - CTST
- Giải sgk Hóa học 12 - CTST
- Giải sgk Sinh học 12 - CTST
- Giải sgk Lịch Sử 12 - CTST
- Giải sgk Địa Lí 12 - CTST
- Giải sgk Giáo dục KTPL 12 - CTST
- Giải sgk Tin học 12 - CTST
- Giải sgk Hoạt động trải nghiệm 12 - CTST
- Giải sgk Âm nhạc 12 - CTST
- Lớp 12 Cánh diều
- Soạn văn 12 Cánh diều (hay nhất)
- Soạn văn 12 Cánh diều (ngắn nhất)
- Giải sgk Toán 12 Cánh diều
- Giải sgk Vật Lí 12 - Cánh diều
- Giải sgk Hóa học 12 - Cánh diều
- Giải sgk Sinh học 12 - Cánh diều
- Giải sgk Lịch Sử 12 - Cánh diều
- Giải sgk Địa Lí 12 - Cánh diều
- Giải sgk Giáo dục KTPL 12 - Cánh diều
- Giải sgk Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 - Cánh diều
- Giải sgk Giáo dục quốc phòng 12 - Cánh diều
- Giải sgk Âm nhạc 12 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

