Chuyên đề bồi dưỡng HSG Hóa học 9 Alcohol (có lời giải)
Bài viết Chuyên đề bồi dưỡng HSG Hóa học 9 Alcohol gồm các dạng bài tập từ cơ bản đến nâng cao với phương pháp giải chi tiết và bài tập tự luyện đa dạng giúp Giáo viên có thêm tài liệu ôn thi Học sinh giỏi Hóa 9.
Chuyên đề bồi dưỡng HSG Hóa học 9 Alcohol (có lời giải)
Chỉ từ 300k mua trọn Chuyên đề bồi dưỡng HSG Hóa học 9 sách mới bản word có lời giải chi tiết:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận giáo án
A. LÝ THUYẾT TRỌNG TÂM
I. ĐỊNH NGHĨA - PHÂN LOẠI
1. Định nghĩa
- Alcohol là những hợp chất hữu cơ trong phân tử có nhóm hydroxyl (-OH) liên kết trực tiếp với nguyên tử C no.
+ Ví dụ: CH3-OH, CH3-CH2-CH2-CH2OH…
- Bậc alcohol là bậc của nguyên tử C liên kết trực tiếp với nhóm (-OH).
+ Ví dụ:
CH3-CH2-CH2-CH2OH: alcohol bậc I
CH3-CH2-CH(CH3)-OH: alcohol bậc II
CH3-C(CH3)2-OH: alcohol bậc III
2. Phân loại
- Alcohol no, đơn chức, mạch hở (CnH2n+1OH):
+ Ví dụ: CH3OH, C2H5OH, C4H9OH...
- Alcohol không no, đơn chức mạch hở:
+ Ví dụ: CH2=CH-CH2OH
- Alcohol thơm đơn chức:
+ Ví dụ: C6H5CH2OH
- Alcohol đa chức:
+ Ví dụ: CH2OH-CH2OH (ethylene glycol), CH2OH-CHOH-CH2OH (glycerol)
(Chương trình THCS chỉ nói về Ethylic alcohol nên trong chuyên đề này chỉ dừng lại nội dung các alcohol no, đơn chức, mạch hở)
3. Đồng phân - Danh pháp
a. Đồng phân:
- Alcohol no, đơn chức, mạch hở có đồng phân cấu tạo (gồm đồng phân mạch C và đồng phân vị trí nhóm -OH).
+ Ví dụ: C4H10O có 4 đồng phân alcohol
CH3-CH2-CH2-CH2OH; CH3-CH(CH3)-CH2OH
CH3-CH2-CH(CH3)-OH; CH3-C(CH3)2-OH
- Ngoài ra alcohol còn có đồng phân ether (ete): R -O-R’ (R, R’ là gốc hydrocarbon)
+ Ví dụ: từ công thức phân tử C2H6O có đồng phân ether: CH3 – O – CH3 (dimethyl ether)
b. Danh pháp:
- Danh pháp thường: Tên gốc alkyl + ic + alcohol
+ Ví dụ: C2H5OH (alcohol ethylic)
Tên của một số alcohol no, đơn chức, mạch hở
Số nguyên tử C |
Công thức cấu tạo mạch thẳng |
Tên thông thường |
Tên thay thế |
1 |
CH3 – OH |
Methylic alcohol |
Methanol |
2 |
CH3 – CH2 – OH |
Ethylic alcohol |
Ethanol |
3 |
CH3 – CH2 – CH2 – OH |
Propylic alcohol |
Propane-1-ol |
4 |
CH3 – CH2 – CH2 – CH2 – OH |
Butylic alcohol |
Butane – 1 – ol |
5 |
CH3 – CH2 – CH2 – CH2 – CH2 – OH |
Pentylic alcohol |
Pentane – 1 – ol |
4. Đặc điểm cấu tạo
- Trong phân tử alcohol các liên kết C−O và O−H kém bền dễ bị phân cắt trong các phản ứng hóa học.
II. ETHYLIC ALCOHOL (ETHANOL)
- Công thức phân tử: C2H6O
- Công thức cấu tạo: CH3 – CH2 – OH → viết gọn: C2H5OH
- Phân tử khối: 46 (g/mol)
1. Tính chất vật lý
- Ethylic alcohol là chất lỏng, không màu, có mùi đặc trưng, vị cay, sôi ở 78,3 °C, có khối lượng riêng là 0,789 g/mL (ở 20 °C), tan vô hạn trong nước, hoà tan được nhiều chất như iodine, benzene,....
- Độ cồn là số mL ethylic alcohol nguyên chất có trong 100 mL dung dịch ở 20°C.
+ Độ cồn thường được kí hiệu là Xº hoặc X% vol.
- Ví dụ: cồn y tế 70° có nghĩa là trong 100 mL cồn 70° có chứa 70 mL ethylic alcohol nguyên chất.
Công thức tính độ rượu: (Đr)
2. Tính chất hóa học
a. Phản ứng thế H của nhóm -OH
- Tác dụng với kim loại kiềm:
+ Các alcohol khác cũng tác dụng được với kim loại kiềm giải phóng khí H2 tương tự như ethylic alcohol.
b. Phản ứng thế nhóm -OH
c. Phản ứng tách nước
- Phản ứng tách nước tạo thành alkene.
+ PTTQ:
- Phản ứng tách nước tạo thành ether.
+ PTTQ:
d. Phản ứng oxi hóa:
- Oxi hóa không hoàn toàn:
+ Để lâu ethylic alcohol trong không khí thì có vị chua do tạo thành acetic acid (CH3COOH)
e. Phản ứng cháy
3. Điều chế:
a. Phương pháp tổng hợp:
- Điều chế từ alkene tương ứng:
b. Phương pháp sinh hóa: Điều chế C2H5OH từ tinh bột.
4. Ứng dụng
- Dùng làm dung môi trong mĩ phẩm, dược phẩm, vecni, sơn, …
- Sản xuất dung dịch sát khuẩn
- Sản xuất đồ uống có cồn: Rượu, bia.
- Điều chế acetic acid, ester.
- Sản xuất nhiên liệu sinh học.
5. Tác hại của việc lạm dụng rượu, bia, đồ uống có cồn.
- Hiện nay, có nhiều loại đồ uống chứa cồn như rượu, bia, nước quả lên men,... Sử dụng quá nhiều đồ uống này sẽ tăng nguy cơ bị viêm gan, viêm loét dạ dày, tăng huyết áp, xơ vữa động mạch, gây tổn thương hệ thần kinh, rối loạn tâm thần.
- Việc lạm dụng rượu, bia là một trong các nguyên nhân gây tai nạn giao thông, tai nạn lao động, bạo lực trong các mối quan hệ gia đình và xã hội.
................................
................................
................................
Xem thêm các Chuyên đề bài tập bồi dưỡng Học sinh giỏi Hóa học lớp 9 có đáp án hay khác:
Xem thêm các loạt bài Để học tốt Hóa học 9 hay khác:
- Giải bài tập Hóa học 9
- Giải sách bài tập Hóa 9
- Đề thi Hóa học 9
- Wiki 200 Tính chất hóa học
- Wiki 3000 Phản ứng hóa học quan trọng
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Chuyên đề: Lý thuyết - Bài tập Hóa học lớp 9 có đáp án được biên soạn bám sát nội dung chương trình sgk Hóa học 9.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 9 Global Success
- Giải sgk Tiếng Anh 9 Smart World
- Giải sgk Tiếng Anh 9 Friends plus
- Lớp 9 Kết nối tri thức
- Soạn văn 9 (hay nhất) - KNTT
- Soạn văn 9 (ngắn nhất) - KNTT
- Giải sgk Toán 9 - KNTT
- Giải sgk Khoa học tự nhiên 9 - KNTT
- Giải sgk Lịch Sử 9 - KNTT
- Giải sgk Địa Lí 9 - KNTT
- Giải sgk Giáo dục công dân 9 - KNTT
- Giải sgk Tin học 9 - KNTT
- Giải sgk Công nghệ 9 - KNTT
- Giải sgk Hoạt động trải nghiệm 9 - KNTT
- Giải sgk Âm nhạc 9 - KNTT
- Giải sgk Mĩ thuật 9 - KNTT
- Lớp 9 Chân trời sáng tạo
- Soạn văn 9 (hay nhất) - CTST
- Soạn văn 9 (ngắn nhất) - CTST
- Giải sgk Toán 9 - CTST
- Giải sgk Khoa học tự nhiên 9 - CTST
- Giải sgk Lịch Sử 9 - CTST
- Giải sgk Địa Lí 9 - CTST
- Giải sgk Giáo dục công dân 9 - CTST
- Giải sgk Tin học 9 - CTST
- Giải sgk Công nghệ 9 - CTST
- Giải sgk Hoạt động trải nghiệm 9 - CTST
- Giải sgk Âm nhạc 9 - CTST
- Giải sgk Mĩ thuật 9 - CTST
- Lớp 9 Cánh diều
- Soạn văn 9 Cánh diều (hay nhất)
- Soạn văn 9 Cánh diều (ngắn nhất)
- Giải sgk Toán 9 - Cánh diều
- Giải sgk Khoa học tự nhiên 9 - Cánh diều
- Giải sgk Lịch Sử 9 - Cánh diều
- Giải sgk Địa Lí 9 - Cánh diều
- Giải sgk Giáo dục công dân 9 - Cánh diều
- Giải sgk Tin học 9 - Cánh diều
- Giải sgk Công nghệ 9 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 9 - Cánh diều
- Giải sgk Âm nhạc 9 - Cánh diều
- Giải sgk Mĩ thuật 9 - Cánh diều

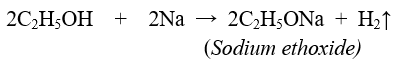










 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

