Chuyên đề bồi dưỡng HSG Hóa học 9 Alkene (có lời giải)
Bài viết Chuyên đề bồi dưỡng HSG Hóa học 9 Alkene gồm các dạng bài tập từ cơ bản đến nâng cao với phương pháp giải chi tiết và bài tập tự luyện đa dạng giúp Giáo viên có thêm tài liệu ôn thi Học sinh giỏi Hóa 9.
Chuyên đề bồi dưỡng HSG Hóa học 9 Alkene (có lời giải)
Chỉ từ 300k mua trọn Chuyên đề bồi dưỡng HSG Hóa học 9 sách mới bản word có lời giải chi tiết:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận giáo án
A. LÝ THUYẾT TRỌNG TÂM
1. Khái niệm - Đồng phân - Danh pháp
a. Khái niệm:
- Alkene là hydrocarbon không no mạch hở có một nối đôi (C = C) trong phân tử.
- Công thức chung: CnH2n (n≥2)
- Các chất C2H4, C3H6, C4H8 . . . CnH2n (n≥2) hợp thành dãy đồng đẵng của alkene.
b. Đồng phân: Có hai loại đồng phân
- Đồng phân cấu tạo: (Đồng phân mạch C và đồng phân vị trí liên kết đôi)
Ví dụ: C4H8 có ba đồng phân cấu tạo.
CH2=CH-CH2-CH3;
CH3-CH=CH-CH3;
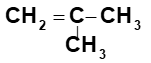
- Đồng phân hình học (cis - trans): Cho alkene có CTCT: abC=Ccd. Điều kiện để xuất hiện đồng phân hình học là: a ≠ b và c ≠ d.
+ Đồng phân cis- : Đồng phân có mạch C chính ở cùng một phía của liên kết đôi.
+ Đồng phân trans- : Đồng phân có mạch C chính ở về hai phía của liên kết đôi.
Ví dụ: CH3-CH=CH-CH3 có hai đồng phân hình học
c. Danh pháp:
- Danh pháp thường: Tên alkane nhưng thay đuôi ane = ylene.
+ Ví dụ: C2H4 (Ethylene), C3H6 (propylene).
- Danh pháp quốc tế (tên thay thế):
* Chú ý:
- Chọn mạch carbon dài nhất, có nhiều nhánh nhất và chứa liên kết bội làm mạch chính.
- Đánh số sao cho nguyên tử carbon có liên kết đôi có chỉ số nhỏ nhất (đánh số mạch chính từ đầu gần liên kết đôi.
- Dùng chữ số (1, 2, 3,...) và gạch nối (-) để chỉ vị trí liên kết bội (nếu chỉ có một vị trị duy nhất của liên kết bội thì không cần).
- Nếu alkene có nhánh thì cần thêm vị trí nhánh và tên nhánh trước tên của alkene tương ứng với mạch chính.
⇒ Đối với mạch C không phân nhánh:
Phần nền + số chỉ vị trí liên kết đôi + ene
⇒ Đối với mạch C có phân nhánh
Số chỉ vị trí nhánh + tên nhánh + phần nền + số chỉ vị trí liên kết đôi + ene
+ Ví dụ: (C4H8) But-2-ene
(C4H8) 2 - Methylprop-1-ene (methylpropene)
Bảng tên gọi của một số alken thường gặp
Số C |
Công thức alkane |
Tiền tố (phần nền) |
Tên alkene |
2 |
CH2 = CH2 |
eth- |
Ethene (Ethylene) |
3 |
CH2 = CH – CH3 |
prop- |
Propene (Propylene) |
4 |
CH2 = CH – CH2 – CH3 |
but-1- |
But-1-ene Methylpropene |
5 |
CH2 = CH – CH2 – CH2 – CH3 |
pent-1- |
Pent-1-ene |
2. Đặc điểm cấu tạo của Ethylene.
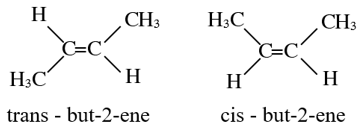
- Công thức phân của của ethylene là C2H4.
- Công thức cấu tạo:
- Phân tử ethylene có liên kết đôi C = C, trong đó có một liên kết (𝛑) kém bền dễ bị phá vỡ trong các phản ứng hóa học. Liên kết còn lại là liên kết bền.
- Các đồng đẳng của ethylene cũng có cấu tạo liên kết tương tự.
3. Tính chất vật lý
- Ở điều kiện thường các alkene
+ Từ C2H4 → C4H8 là chất khí.
+ Từ C5H10 trở đi là chất lỏng hoặc chất rắn.
4. Tính chất hóa học
a. Phản ứng cộng (đặc trưng)
- Cộng H2:
Viết gọn:
- Cộng Br2:
Viết gọn:
→ Phản ứng alkene tác dụng với Br2 dùng để nhận biết alkene (dd Br2 mất màu)
* Cộng HX (X: Cl, Br, OH . . .)
Ví dụ:
b. Phản ứng trùng hợp:
Phản ứng trùng hợp alkene là quá trình cộng hợp liên tiếp nhiều phân tử alkene giống nhau hoặc tương tự nhau (gọi là monomer) tạo thành phân tử có phân tử khối lớn (gọi là polymer).
Ví dụ: Phản ứng trùng hợp ethylene và propylene tạo thành polyethylene (PE) và polypropylene (PP).
c. Phản ứng cháy: Alkene dễ cháy khi có mặt oxygen, phản ứng tỏa nhiều nhiệt.
4. Điều chế
a. Phòng thí nghiệm:
b. Điều chế từ alkane:
5. Ứng dụng
- Sản xuất chất dẻo PE, PVC,...
- Sản xuất keo dán
- Nguyên liệu cho công nghiệp hóa học: Tổng hợp ethylic alcolhol, tổng hợp acetic acid...
- Sản xuất dung môi.
B. BÀI TẬP CHUYÊN ĐỀ
1. BÀI TẬP LÝ THUYẾT
Bài 1. Viết CTCT các đồng phân (cấu tạo) alkene ứng với CTPT là C4H8 và C5H10.
Bài 2. Hoàn thành các PTHH của các phản ứng sau:
a.
b.
c.
d.
e.
f.
g.
h.
Bài 3. Viết phương trình hóa học của các phản ứng:
(a) Propene tác dụng với hydrogen, xúc tác nickel.
(b) Propene tác dụng với nước, xúc tác acid H3PO4.
(c) 2-methylpropene tác dụng với nước, xúc tác acid H3PO4.
................................
................................
................................
Xem thêm các Chuyên đề bài tập bồi dưỡng Học sinh giỏi Hóa học lớp 9 có đáp án hay khác:
Xem thêm các loạt bài Để học tốt Hóa học 9 hay khác:
- Giải bài tập Hóa học 9
- Giải sách bài tập Hóa 9
- Đề thi Hóa học 9
- Wiki 200 Tính chất hóa học
- Wiki 3000 Phản ứng hóa học quan trọng
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Chuyên đề: Lý thuyết - Bài tập Hóa học lớp 9 có đáp án được biên soạn bám sát nội dung chương trình sgk Hóa học 9.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 9 Global Success
- Giải sgk Tiếng Anh 9 Smart World
- Giải sgk Tiếng Anh 9 Friends plus
- Lớp 9 Kết nối tri thức
- Soạn văn 9 (hay nhất) - KNTT
- Soạn văn 9 (ngắn nhất) - KNTT
- Giải sgk Toán 9 - KNTT
- Giải sgk Khoa học tự nhiên 9 - KNTT
- Giải sgk Lịch Sử 9 - KNTT
- Giải sgk Địa Lí 9 - KNTT
- Giải sgk Giáo dục công dân 9 - KNTT
- Giải sgk Tin học 9 - KNTT
- Giải sgk Công nghệ 9 - KNTT
- Giải sgk Hoạt động trải nghiệm 9 - KNTT
- Giải sgk Âm nhạc 9 - KNTT
- Giải sgk Mĩ thuật 9 - KNTT
- Lớp 9 Chân trời sáng tạo
- Soạn văn 9 (hay nhất) - CTST
- Soạn văn 9 (ngắn nhất) - CTST
- Giải sgk Toán 9 - CTST
- Giải sgk Khoa học tự nhiên 9 - CTST
- Giải sgk Lịch Sử 9 - CTST
- Giải sgk Địa Lí 9 - CTST
- Giải sgk Giáo dục công dân 9 - CTST
- Giải sgk Tin học 9 - CTST
- Giải sgk Công nghệ 9 - CTST
- Giải sgk Hoạt động trải nghiệm 9 - CTST
- Giải sgk Âm nhạc 9 - CTST
- Giải sgk Mĩ thuật 9 - CTST
- Lớp 9 Cánh diều
- Soạn văn 9 Cánh diều (hay nhất)
- Soạn văn 9 Cánh diều (ngắn nhất)
- Giải sgk Toán 9 - Cánh diều
- Giải sgk Khoa học tự nhiên 9 - Cánh diều
- Giải sgk Lịch Sử 9 - Cánh diều
- Giải sgk Địa Lí 9 - Cánh diều
- Giải sgk Giáo dục công dân 9 - Cánh diều
- Giải sgk Tin học 9 - Cánh diều
- Giải sgk Công nghệ 9 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 9 - Cánh diều
- Giải sgk Âm nhạc 9 - Cánh diều
- Giải sgk Mĩ thuật 9 - Cánh diều

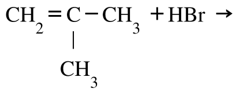










 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

