Na2SO3 + HCl → NaCl + SO2 + H2O | Na2SO3 ra SO2
Phản ứng Na2SO3 + HCl tạo ra khí SO2 thuộc loại phản ứng trao đổi đã được cân bằng chính xác và chi tiết nhất. Bên cạnh đó là một số bài tập có liên quan về Na2SO3 có lời giải, mời các bạn đón xem:
Na2SO3 + 2HCl → 2NaCl + SO2 ↑ + H2O
1. Phương trình phản ứng Na2SO3 tác dụng với HCl
Na2SO3 + 2HCl → 2NaCl + H2O + SO2↑
Phản ứng này thuộc loại phản ứng trao đổi.
2. Hiện tượng của phản ứng Na2SO3 tác dụng với HCl
- Có khí thoát ra; khí là SO2.
3. Cách tiến hành phản ứng Na2SO3 tác dụng với HCl
- Nhỏ từ từ dung dịch HCl vào ống nghiệm có chứa dung dịch Na2SO3
4. Cách viết phương trình ion thu gọn của phản ứng Na2SO3 tác dụng với HCl Bước 1: Viết phương trình phân tử:
Na2SO3 + 2HCl → 2NaCl + H2O + SO2↑
Bước 2: Viết phương trình ion đầy đủ bằng cách: chuyển các chất vừa dễ tan, vừa điện li mạnh thành ion; các chất điện li yếu, chất kết tủa, chất khí để nguyên dưới dạng phân tử:
Bước 3: Viết phương trình ion thu gọn từ phương trình ion đầy đủ bằng cách lược bỏ đi các ion giống nhau ở cả hai vế:
5. Mở rộng về phản ứng trao đổi trong dung dịch chất điện li
Xét phản ứng:
Dung dịch A + dung dịch B → Sản phẩm.
- Phản ứng xảy ra trong dung dịch các chất điện li là phản ứng giữa các ion.
- Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi các ion kết hợp được với nhau tạo thành ít nhất 1 trong số các chất sau:
+ Chất kết tủa.
+ Chất điện li yếu.
+ Chất khí.
Thí dụ:
+ Phản ứng tạo thành chất kết tủa:
Na2SO4 + BaCl2 → 2NaCl + BaSO4↓
+ Phản ứng tạo thành chất điện li yếu:
HCl + NaOH → NaCl + H2O
+ Phản ứng tạo thành chất khí:
Fe + H2SO4 loãng → FeSO4 + H2↑
6. Mở rộng về hydrochloric acid (HCl)
6.1. Tính chất vật lí
- Hiđro clorua tan vào nước tạo thành dung dịch hydrochloric acid.
- hydrochloric acid là chất lỏng, không màu, mùi xốc.
- Dung dịch HCl đặc nhất (ở 20oC) đạt tới nồng độ 37% và có khối lượng riêng D = 1,19 g/cm3.
- Dung dịch HCl đặc “bốc khói” trong không khí ẩm. Đó là do hiđro clorua thoát ra tạo với hơi nước trong không khí thành những hạt dung dịch nhỏ như sương mù.
6.2. Tính chất hóa học
Hydrochloric acid là một axit mạnh, mang đầy đủ tính chất hóa học của một axit như:
- Làm quỳ tím chuyển sang màu đỏ.
- Tác dụng với kim loại đứng trước (H) trong dãy hoạt động hóa học của kim loại. Ví dụ:
Mg + 2HCl → MgCl2 + H2
2Al + 6HCl → 2AlCl3 + 3H2
Chú ý: Kim loại có nhiều hóa trị tác dụng với dung dịch HCl thu được muối trong đó kim loại ở mức hóa trị thấp. Ví dụ:
Fe + 2HCl → FeCl2 + H2
- Tác dụng với basic oxide và bazơ tạo thành muối và nước. Ví dụ:
CuO + 2HCl CuCl2 + H2O
Fe2O3 + 6HCl 2FeCl3 + 3H2O
NaOH + HCl → NaCl + H2O
Cu(OH)2 + 2HCl → CuCl2 + 2H2O
- Tác dụng với muối của axit yếu hơn tạo thành muối mới và axit mới. Ví dụ:
CaCO3 + 2HCl → CaCl2 + H2O + CO2 ↑
AgNO3 + HCl → AgCl↓ + HNO3
Ngoài tính chất đặc trưng là tính axit, dung dịch axit HCl đặc còn thể hiện tính khử khi tác dụng chất oxi hoá mạnh như KMnO4, MnO2, K2Cr2O7, MnO2, KClO3…
6.3. Điều chế
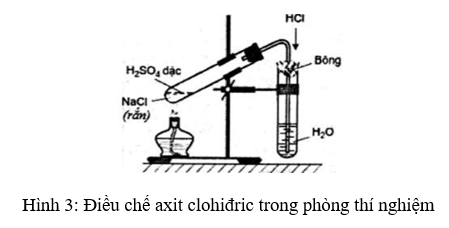
a) Trong phòng thí nghiệm
- Điều chế hiđro clorua bằng cách cho tinh thể NaCl vào dung dịch H2SO4 đậm đặc và đun nóng (phương pháp sunfat) rồi hấp thụ vào nước để được hydrochloric acid.
- Phương trình hóa học minh họa:
2NaCltt + H2SO4 đặc Na2SO4 + 2HCl ↑
NaCltt + H2SO4 đặc NaHSO4 + HCl ↑
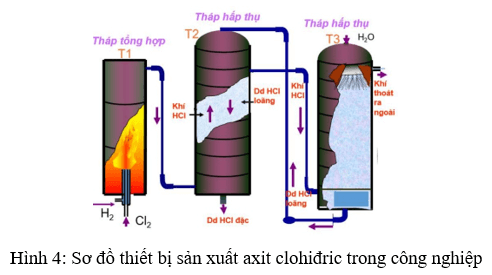
b) Trong công nghiệp
- Phương pháp tổng hợp: Đốt H2 trong khí quyển Cl2
H2 + Cl2 2HCl
- Phương pháp sunfat: Công nghệ sản xuất từ NaCl rắn và H2SO4 đặc:
2NaCltt + H2SO4 đặc Na2SO4 + 2HCl ↑
- Ngoài ra một lượng lớn HCl thu được trong công nghiệp từ quá trình clo hóa các hợp chất hữu cơ.
7. Bài tập vận dụng liên quan
Câu 1:Kim loại nào sau đây khi tác dụng với HCl và Clo cho cùng một muối clorua kim loại:
A. Cu
B. Ag
C. Fe
D. Zn
Hướng dẫn giải:
Đáp án D
Cu, Ag không tác dụng được với HCl → loại A và B.
Fe có hóa trị II và III, khi tác dụng với HCl cho FeCl2 còn tác dụng với Cl2 cho FeCl3 → loại C
Zn tác dụng với Cl2 và HCl đều cho ZnCl2.
Câu 2:Axit HCl có thể tác dụng được với bao nhiêu chất trong dãy sau: Al, Mg(OH)2, Na2SO4, FeS, Fe2O3, K2O, CaCO3, Mg(NO3)2?
A. 6
B. 7
C. 8
D. 9
Hướng dẫn giải:
Đáp án A
6 HCl +2 Al → 2AlCl3 + 3H2
2 HCl + Mg(OH)2 → MgCl2 + 2 H2O
2 HCl + FeS → FeCl2 + H2S
6 HCl + Fe2O3 → 2 FeCl3 + 3 H2O
2 HCl + K2O → 2 KCl + H2O
2 HCl + CaCO3 → CaCl2 + H2O + CO2
Câu 3: Cho 8,7 gam MnO2 tác dụng với dung dịch HCl đậm đặc sinh ra V lít khí Cl2 (ở đktc). Hiệu suất phản ứng là 85%. V có giá trị là
A. 2 lít
B. 1,904 lít
C. 1,82 lít
D. 2,905 lít
Hướng dẫn giải:
Đáp án B
Phương trình hóa học:
MnO2 + 4HCl MCl2 + Cl2 + 2H2O
Theo PTHH: (số mol lý thuyết tính theo PTHH)
→ → n clo thực tế = 0,085 mol
lít
Câu 4: Điều chế Cl2 từ HCl và MnO2. Cho toàn bộ khí Cl2 điều chế được qua dung dịch NaI, sau phản ứng thấy có 12,7 gam I2 sinh ra. Khối lượng HCl có trong dung dịch đã dùng là:
A. 9,1 gam
B. 8,3 gam
C. 7,3 gam
D. 12,5 gam
Hướng dẫn giải:
Đáp án C
Theo PTHH: Cl2 + 2 NaI → 2 NaCl + I2
Theo PTHH: MnO2 + 4HCl MnCl2 + 2H2O +Cl2
= 0,05.4 = 0,2 mol
→ m HCl = 0,2. 36,5 = 7,3 g
Câu 5: Nồng độ cao nhất của dung dịch HCl ở 200C là
A. 25%
B. 37%
C. 20%
D. 50%
Hướng dẫn giải:
Đáp án B
Nồng độ cao nhất của dung dịch HCl ở 200C là 37%
Câu 6. Để trung hòa 20 ml dung dịch HCl 0,1M cần 10 ml dung dịch NaOH nồng độ x mol/l. Giá trị của x là
A. 0,3. B. 0,4. C. 0,2. D. 0,1.
Hướng dẫn giải
Đáp án C
nHCl = 0,1.0,02 = 0,002 mol
HCl + NaOH → NaCl + H2O
0,002 → 0,002 mol
Câu 7: Cho 36 gam FeO phản ứng vừa đủ với dung dịch chứa a mol HCl. Giá trị của a là
A. 1,00. B. 0,50. C. 0,75. D. 1,25.
Hướng dẫn giải
Đáp án A
2HCl + FeO → FeCl2 + H2O
Theo PTHH: nHCl = 2nFeO = 1 mol
Câu 8. Cần dùng 300 gam dung dịch HCl 3,65% để hòa tan vừa hết x gam Al2O3. Giá trị của x là
A. 51. B. 5,1. C. 153. D. 15,3.
Hướng dẫn giải
Đáp án B
6HCl + Al2O3 → 2AlCl3 + 3H2O
0,3 → 0,05 mol
= 0,05.102 = 5,1 gam
Câu 9. Cho 5,6 gam một oxit kim loại tác dụng vừa đủ với HCl cho 11,1 gam muối clorua của kim loại đó. Cho biết công thức oxit kim loại?
A. Al2O3. B. CaO. C. CuO. D. FeO.
Hướng dẫn giải
Đáp án B
Gọi công thức oxit là M2Oa
2aHCl + M2Oa → 2MCla + aH2O
Gọi số mol H2O là x (mol) ⇒ nHCl = 2x (mol)
Bảo toàn khối lượng: 36,5.2x + 5,6 = 11,1 + 18.x
⇒ x = 0,1 mol
a |
1 |
2 |
3 |
M |
20 |
40 |
60 |
Kết luận |
Loại |
Ca |
Loại |
Câu 10. Cho 30,00 gam hỗn hợp X gồm Fe và FeO phản ứng với dung dịch HCl dư, đến khi phản ứng xảy ra hoàn toàn thu được 6,72 lít khí H2 (đktc). Khối lượng của FeO trong 30,00 gam hỗn hợp X là
A. 13,2 gam. B. 46,8 gam. C. 16,8 gam. D. 5,6 gam.
Hướng dẫn giải
Đáp án A
2HCl + FeO → FeCl2 + H2O
2HCl + Fe → FeCl2 + H2
Theo PTHH:
nFe = nkhí = 0,3 mol ⇒ mFeO = 30 – 0,3.56 = 13,2 gam.
Câu 11. Để hoà tan hết hỗn hợp Zn và ZnO phải dùng 100,8 ml dung dịch HCl 36,5% (D = 1,19g/ml) thu được 0,4 mol khí. Phần trăm về khối lượng hỗn hợp Zn và ZnO ban đầu lần lượt là
A. 40% và 60%.. B. 45% và 55%.
C. 50% và 50% D. 61,6% và 38,4%.
Hướng dẫn giải
Đáp án D
2HCl + ZnO → ZnCl2 + H2O (1)
2HCl + Zn → ZnCl2 + H2 (2)
Theo PTHH (2):
nHCl (2) = 2.nZn = 0,8 mol ⇒ nHCl (1) = 1,2 – 0,8 = 0,4 mol
mhỗn hợp = 0,4.65 + 0,2.81 = 42,2 gam
Câu 12. Cho 36,5 gam dung dịch HCl 10% vào một cốc đựng NaHCO3 dư thì thu được V lit khí ở đktc. Giá trị của x là
A. 44,8. B. 4,48. C. 22,4. D. 2,24.
Hướng dẫn giải
Đáp án D
NaHCO3 + HCl → NaCl + H2O + CO2
0,1 0,1 mol
⇒ V = 0,1.22,4 = 2,24 lít.
Câu 13. Cho 50 gam CaCO3 tác dụng vừa đủ với dung dịch HCl 20% (D =1,2g/ml). Khối lượng dung dịch HCl đã dùng là
A. 152,08 gam. B. 55,0 gam.
C. 180,0 gam. D. 182,5 gam.
Hướng dẫn giải
Đáp án D
CaCO3 + 2HCl → CaCl2 + H2O + CO2
0,5 → 1 mol
Câu 14. Cho một lượng hỗn hợp CuO và Fe2O3 tác dụng hết với dung dịch HCl thu được 2 muối có tỉ lệ mol 1: 1. Phần trăm khối lượng của CuO và Fe2O3 trong hỗn hợp lần lượt là:
A. 30% và 70% B. 50% và 50%.
C. 20% và 80% D. 40% và 60%
Hướng dẫn giải
Đáp án B
CuO + 2HCl → CuCl2 + H2O (1)
Fe2O3 + 6HCl → 2FeCl3 + 3H2O (2)
Do 2 muối thu được có tỉ lệ mol 1 : 1, giả sử CuCl2 1 mol ⇒ FeCl3 1 mol.
Từ (1); (2) ta có:
Câu 15. Hòa tan hoàn toàn 12,4 gam hỗn hợp X gồm FeO, Fe3O4, ZnO và Al2O3 cần 400 ml dung dịch HCl 1,5M. Tính khối lượng muối thu được trong dung dịch sau phản ứng?
A. 26,8 gam B. 24,8 gam C. 28,9 gam D. 29,5 gam
Hướng dẫn giải
Đáp án C
Sơ đồ phản ứng:
BTNT H:
BTKL: moxit + mHCl = mmuối + mnước
⇒ mmuối = 12,4 + 0,6.36,5 - 0,3.18 = 28,9 gam.
Xem thêm các phương trình hóa học hay khác:
- Na2SO3 + 2HBr → 2NaBr + SO2 ↑ + H2O
- Na2SO3 + H2SO4 → Na2SO4 + SO2 ↑ + H2O
- Na2SO3 + Ba(OH)2 → 2NaOH + BaSO3( ↓)
- Na2SO3 + Ca(OH)2 → 2NaOH + CaSO3( ↓)
- Na2SO3 + CaCl2 → 2NaCl + CaSO3( ↓)
- Na2SO3 + BaCl2 → 2NaCl + BaSO3( ↓)
- Na2SO3 + Ba(NO3)2 → 2NaNO3 + BaSO3( ↓)
- Na2SO3 + Ca(NO3)2 → 2NaNO3 + CaSO3( ↓)
- Na2SO3 + SO2 + H2O → 2NaHSO3
- 5Na2SO3 + 2KMnO4 + 6NaHSO4 → 8Na2SO4 +2MnSO4 + K2SO4 + 3H2O
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)









 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



