(Ôn thi ĐGNL, ĐGTD) Chuyên đề: Phản ứng oxi hóa - khử
Chuyên đề Phản ứng oxi hóa - khử trong tài liệu ôn thi Đánh giá năng lực, Đánh giá tư duy theo cấu trúc mới nhất đầy đủ lý thuyết trọng tâm, các dạng bài & bài tập đa dạng từ cơ bản đến nâng cao giúp Giáo viên & học sinh có thêm tài liệu ôn thi ĐGNL HSA, VACT và ĐGTD TSA đạt kết quả cao.
(Ôn thi ĐGNL, ĐGTD) Chuyên đề: Phản ứng oxi hóa - khử
Xem thử Tài liệu & Đề thi HSA Xem thử Tài liệu & Đề thi VACT Xem thử Tài liệu & Đề thi TSA Xem thử Tài liệu & Đề thi SPT
Chỉ từ 500k mua trọn bộ Đề thi & Tài liệu ôn thi ĐGNL - ĐGTD năm 2026 của các trường theo cấu trúc mới bản word có lời giải chi tiết:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận đề thi
I. LÝ THUYẾT TRỌNG TÂM
1. Số oxi hóa
- Số oxi hoá là điện tích quy ước của nguyên tử và được tính theo các quy tắc.
- Quy tắc xác định số oxi hóa:
+ Quy tắc 1. Trong đơn chất, số oxi hóa của nguyên tử bằng 0.
+ Quy tắc 2. Trong phân tử các hợp chất, thông thường số oxi hóa của hydrogen là +1, của oxygen là -2, các kim loại điển hình có số oxi hóa dương và có giá trị bằng số electron hóa trị.
+ Quy tắc 3. Trong hợp chất, tổng số oxi hóa của các nguyên tử trong phân tử bằng 0.
Số oxi hóa thường gặp của một số nguyên tử trong hợp chất
Nguyên tử |
Hydrogen |
Oxygen |
Kim loại kiềm (nhóm IA) |
Kim loại kiềm thổ (nhóm IIA) |
Aluminium |
Số oxi hóa |
+1 |
-2 |
+1 |
+2 |
+3 |
+ Quy tắc 4. Trong ion đơn nguyên tử, số oxi hóa của nguyên tử bằng điện tích ion; trong ion đa nguyên tử, tổng số oxi hóa của các nguyên tử bằng điện tích ion.
2. Phản ứng oxi hóa – khử
- Phản ứng oxi hóa – khử là phản ứng hóa học xảy ra đồng thời quá trình nhường electron và quá trình nhận electron.
+ Chất khử là chất nhường electron, có số oxi hóa tăng sau phản ứng.
+ Chất oxi hóa là chất nhận electron, có số oxi hóa giảm sau phản ứng.
+ Quá trình oxi hóa (sự oxi hóa) là quá trình chất khử nhường electron.
+ Quá trình khử (sự khử) là quá trình chất oxi hóa nhận electron.
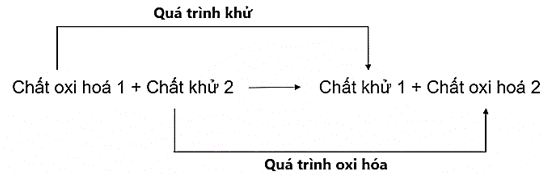
- Bản chất của phản ứng oxi hoá - khử:
- Nguyên tắc lập phương trình hoá học của phản ứng oxi hoá - khử theo phương pháp thăng bằng electron: ∑ số electron chất khử nhường = ∑ số electron chất oxi hoá nhận.
- Các phản ứng oxi hoá - khử xảy ra phổ biến trong thực tiễn: sự cháy, sự han gỉ của kim loại, sản xuất hoá chất, chuyển hoá nitrogen trong tự nhiên,...
II. CÂU HỎI ÔN LUYỆN
Phần 1. Trắc nghiệm nhiều phương án lựa chọn
Câu 1. Số oxi hóa của nguyên tử Cl trong hợp chất là
A. +7.
B. + 5.
C. −3.
D. +3.
Câu 2. Phản ứng hoá học nào dưới đây là phản ứng oxi hoá - khử?
A. (s) → CaO(s) + (g).
B. FeCl3(aq) + 3AgNO3(aq) → Fe(NO3)3(aq) + 3AgCl(s).
C. CuSO4(aq) + 2NaOH(aq) → Cu(OH)2(s) + Na2SO4(aq).
D. SO2(g) + 2H2S(g) → 3S(s) + 2H2O(l).
Câu 3. Hỗn hợp tecmit dùng hàn gắn đường ray có thành phần chính là aluminium (Al) và iron(III) oxide (Fe2O3). Phản ứng xảy ra khi đung nóng hỗn hợp tecmit như sau:
Phát biểu nào dưới đây là đúng?
A. là chất bị oxi hóa.
B. là chất nhường electron.
C. Al là chất bị oxi hoá.
D. là chất nhận electron.
Câu 4. Iron có số oxi hoá +2 trong hợp chất nào sau đây?
A.
B.
C.
D.
Câu 5. Số oxi hoá của nguyên tử hydrogen trong phân tử H2 là bao nhiêu?
A. –2.
B. +2.
C. +1.
D. 0.
Câu 6. Phản ứng oxi hóa – khử là phản ứng có sự nhường và nhận
A. electron.
B. neutron.
C. proton.
D. cation.
Câu 7. Chất khử là chất
A. nhường electron, chứa nguyên tố có số oxi hóa giảm sau phản ứng.
B. nhường electron, chứa nguyên tố có số oxi hóa tăng sau phản ứng.
C. nhận electron, chứa nguyên tố có số oxi hóa tăng sau phản ứng.
D. nhận electron, chứa nguyên tố có số oxi hóa giảm sau phản ứng.
Câu 8. Phản ứng nào sau đây có sự thay đổi số oxi hóa của nguyên tố calcium?
A.
B.
C.
D.
Câu 9. Cho quá trình Al → + 3e, đây là quá trình
A. khử.
B. oxi hóa.
C. tự oxi hóa – khử.
D. nhận proton.
Câu 10. Thực hiện các phản ứng hóa học sau:
(a)
(b)
(c)
(d)
Số phản ứng sulfur đóng vai trò chất oxi hóa là
A. 4.
B. 2.
C. 3.
D. 1.
................................
................................
................................
Xem thử Tài liệu & Đề thi HSA Xem thử Tài liệu & Đề thi VACT Xem thử Tài liệu & Đề thi TSA Xem thử Tài liệu & Đề thi SPT
Xem thêm tài liệu ôn thi đánh giá năng lực HSA, VACT, đánh giá tư duy TSA hay khác:
- (Ôn thi ĐGNL HSA) Chuyên đề: Cấu tạo nguyên tử
- (Ôn thi ĐGNL HSA) Chuyên đề: Bảng tuần hoàn các nguyên tố hóa học
- (Ôn thi ĐGNL HSA) Chuyên đề: Liên kết hóa học
- (Ôn thi ĐGNL HSA) Chuyên đề: Năng lượng hóa học
- (Ôn thi ĐGNL HSA) Chuyên đề: Tốc độ phản ứng hóa học
- (Ôn thi ĐGNL HSA) Chuyên đề: Nguyên tố nhóm VIIA (Nhóm Halogen)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Lớp 12 Kết nối tri thức
- Soạn văn 12 (hay nhất) - KNTT
- Soạn văn 12 (ngắn nhất) - KNTT
- Giải sgk Toán 12 - KNTT
- Giải sgk Vật Lí 12 - KNTT
- Giải sgk Hóa học 12 - KNTT
- Giải sgk Sinh học 12 - KNTT
- Giải sgk Lịch Sử 12 - KNTT
- Giải sgk Địa Lí 12 - KNTT
- Giải sgk Giáo dục KTPL 12 - KNTT
- Giải sgk Tin học 12 - KNTT
- Giải sgk Công nghệ 12 - KNTT
- Giải sgk Hoạt động trải nghiệm 12 - KNTT
- Giải sgk Giáo dục quốc phòng 12 - KNTT
- Giải sgk Âm nhạc 12 - KNTT
- Giải sgk Mĩ thuật 12 - KNTT
- Lớp 12 Chân trời sáng tạo
- Soạn văn 12 (hay nhất) - CTST
- Soạn văn 12 (ngắn nhất) - CTST
- Giải sgk Toán 12 - CTST
- Giải sgk Vật Lí 12 - CTST
- Giải sgk Hóa học 12 - CTST
- Giải sgk Sinh học 12 - CTST
- Giải sgk Lịch Sử 12 - CTST
- Giải sgk Địa Lí 12 - CTST
- Giải sgk Giáo dục KTPL 12 - CTST
- Giải sgk Tin học 12 - CTST
- Giải sgk Hoạt động trải nghiệm 12 - CTST
- Giải sgk Âm nhạc 12 - CTST
- Lớp 12 Cánh diều
- Soạn văn 12 Cánh diều (hay nhất)
- Soạn văn 12 Cánh diều (ngắn nhất)
- Giải sgk Toán 12 Cánh diều
- Giải sgk Vật Lí 12 - Cánh diều
- Giải sgk Hóa học 12 - Cánh diều
- Giải sgk Sinh học 12 - Cánh diều
- Giải sgk Lịch Sử 12 - Cánh diều
- Giải sgk Địa Lí 12 - Cánh diều
- Giải sgk Giáo dục KTPL 12 - Cánh diều
- Giải sgk Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 - Cánh diều
- Giải sgk Giáo dục quốc phòng 12 - Cánh diều
- Giải sgk Âm nhạc 12 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

