Tài liệu Vật Lí ôn thi ĐGNL HSA, VACT, TSA
Tài liệu tổng hợp các chuyên đề môn Vật Lí ôn thi Đánh giá năng lực Đại học Quốc gia Hà Nội, Đại học Quốc gia Tp.HCM, Đánh giá tư duy Đại học Bách khoa Hà Nội theo cấu trúc mới nhất giúp Giáo viên & học sinh có thêm tài liệu ôn thi HSA, VACT, TSA đạt kết quả cao. Mời các bạn đón đọc:
Tài liệu Vật Lí ôn thi ĐGNL HSA, VACT, TSA
Xem thử Tài liệu & Đề thi HSA Xem thử Tài liệu & Đề thi VACT Xem thử Tài liệu & Đề thi TSA Xem thử Tài liệu & Đề thi SPT
Chỉ từ 450k mua trọn bộ Đề thi & Tài liệu ôn thi ĐGNL - ĐGTD năm 2025 của các trường theo cấu trúc mới bản word có lời giải chi tiết:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận đề thi
- (Ôn thi ĐGNL HSA, VACT, TSA) Chuyên đề: Vật lí nhiệt
- (Ôn thi ĐGNL HSA, VACT, TSA) Chuyên đề: Khí lí tưởng
- (Ôn thi ĐGNL HSA, VACT, TSA) Chuyên đề: Từ trường
- (Ôn thi ĐGNL HSA, VACT, TSA) Chuyên đề: Vật lí hạt nhân
- (Ôn thi ĐGNL HSA, VACT, TSA) Chuyên đề: Dao động
- (Ôn thi ĐGNL HSA, VACT, TSA) Chuyên đề: Sóng
- (Ôn thi ĐGNL HSA, VACT, TSA) Chuyên đề: Điện trường
- (Ôn thi ĐGNL HSA, VACT, TSA) Chuyên đề: Dòng điện. Mạch điện
- (Ôn thi ĐGNL HSA, VACT, TSA) Chuyên đề: Động lực học
- (Ôn thi ĐGNL HSA, VACT, TSA) Chuyên đề: Bảo toàn động lượng - bảo toàn năng lượng
Xem thử Tài liệu & Đề thi HSA Xem thử Tài liệu & Đề thi VACT Xem thử Tài liệu & Đề thi TSA Xem thử Tài liệu & Đề thi SPT
(Ôn thi ĐGNL HSA, VACT, TSA) Chuyên đề: Khí lí tưởng
A. KIẾN THỨC TRỌNG TÂM
I. MÔ HÌNH ĐỘNG HỌC PHÂN TỬ CHẤT KHÍ
1. Chuyển động Brown
Chuyển động Brown chứng tỏ các phân tử chất khí chuyển động hỗn loạn, không ngừng. Nhiệt độ càng cao, các phân tử khí chuyển động càng nhanh.
2. Chất khí
Khoảng cách giữa các phân tử khí rất lớn so với kích thước của chúng nên lực tương tác giữa các phân tử khí không đáng kể trừ khi chúng tiếp xúc với nhau trong quá trình va chạm.
Các phân tử khí chuyển động hỗn loạn, do đó khối chất khí không có hình dạng và thể tích riêng mà nó có hình dạng và thể tích của bình chứa nó và có thể nén được dễ dàng.
Khi chuyển động hỗn loạn, các phân tử khí va chạm vào nhau và va chạm thành bình nên gây ra áp suất lên thành bình chứa. Khi nhiệt độ tăng, áp suất khí tác dụng lên thành bình tăng. Khi đó tốc độ trung bình của các phân tử được xác định:
3. Số mol và số Avogadro
• Số lượng phân tử trong một mol chất được gọi là số Avogadro
• Số phân tử hay nguyên tử chứa trong n mol của một chất: N = n.NA
• Nếu một chất có khối lượng m, chứa N phân tử thì số mol n của chất đó:
Trong đó M (g/mol) là khối lượng mol (khối lượng của 1 mol) chất đó.
4. Mô hình động học phân tử chất khí
Thuyết động học phân tử chất khí hay còn gọi là mô hình động học phân tử chất khí gồm những nội dung chính sau:
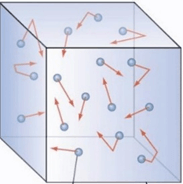
• Chất khí gồm tập hợp rất nhiều các phân tử có kích thước rất nhỏ so với khoảng cách giữa chúng.
• Các phân tử khí luôn chuyển động hỗn loạn, không ngừng. Nhiệt độ càng cao, các phân tử khí chuyển động càng nhanh.
• Khi chuyển động hỗn loạn, các phân tử khí va chạm vào nhau và va chạm thành bình nên gây ra áp suất lên thành bình chứa.
5. Mô hình khí lí tưởng
Khí lí tưởng là chất khí gồm các phân tử có kích thước rất nhỏ, có thể bỏ qua. Các phân tử chỉ tương tác khi va chạm; giữa hai va chạm liên tiếp, chúng chuyển động thẳng đều. Va chạm của các phân tử khí lí tưởng với nhau và với thành bình là va chạm hoàn toàn đàn hồi.
II. ĐỊNH LUẬT BOYLE
1. Trạng thái và quá trình biến đổi trạng thái
Trạng thái của một khối lượng khí nhất định được xác định bằng ba thông số trạng thái của khối khí: thể tích V, áp suất p và nhiệt độ tuyệt đối T.
Quá trình khối khí biến đổi từ trạng thái này sang trạng thái khác gọi là quá trình biến đổi trạng thái.
2. Định luật Boyle
a. Quá trình đẳng nhiệt
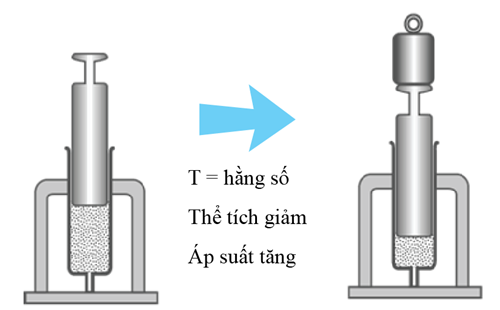
Quá trình biến đổi trạng thái của một khối lượng khí xác định khi nhiệt độ giữ không đổi được gọi là quá trình đẳng nhiệt.
Quá trình đẳng nhiệt (nhiệt độ được giữ không đổi), khi thể tích giảm thì áp suất tăng và ngược lại.
b. Định luật Boyle
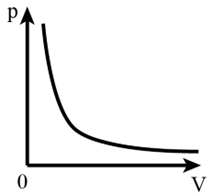
Ở nhiệt độ không đổi, áp suất của một lượng khí xác định tỉ lệ nghịch với thể tích của nó hay pV = const => p1V1 = p2V2.
Đồ thị của định luật Boyle
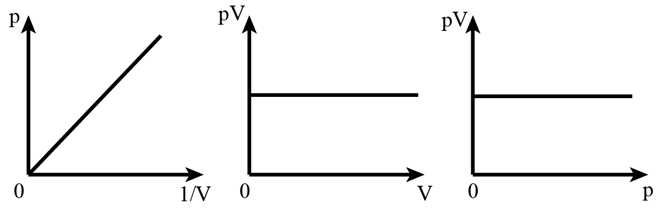
Ngoài ra còn có thể biểu diễn định luật dưới các dạng đồ thị khác như sau:
c. Ứng dụng
Định luật Boyle được ứng dụng trong nhiều lĩnh vực như:
• Chế tạo các dụng cụ như bơm xe đạp, bình cứu hỏa, phao cứu sinh, ...
• Hóa lỏng khí để bảo quản và vận chuyển.
III. ĐỊNH LUẬT CHARLES
1. Quá trình đẳng áp
a. Quá trình biến đổi đẳng áp
Quá trình biến đổi trạng thái của một khối lượng khí xác định khi giữ áp suất không đổi được gọi là quá trình đẳng áp.
b. Định luật Charles
Ở áp suất không đổi, thể tích của một khối lượng khí xác định tỉ lệ thuận với nhiệt độ tuyệt đối của nó:
V ∼ T hay = k = const.
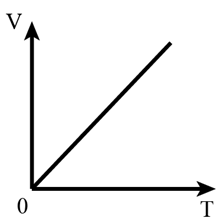
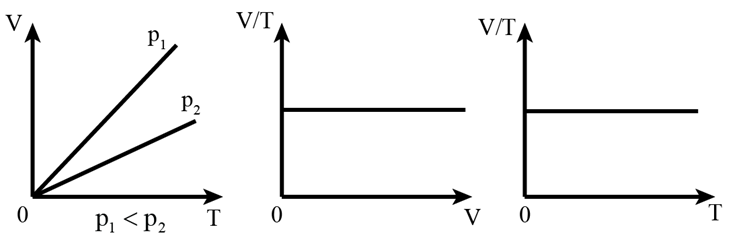
Đồ thị của định luật Charles
Ngoài ra có thể biểu diễn định luật Charles dưới dạng các đồ thị khác sau:
d. Ứng dụng:
Định luật Charles được ứng dụng trong nhiều lĩnh vực như:
• Nhiệt kế khí: Đo nhiệt độ môi trường, đo nhiệt độ cơ thể,...
• Cảm biến áp suất: Cảm biến áp suất trong lốp xe, cảm biến áp suất khí quyển,...
• Hệ thống điều hòa: Sử dụng sự thay đổi thể tích khí để điều chỉnh nhiệt độ.
• Y học: Chẩn đoán và điều trị các bệnh về phổi.
• Vật lý: Nghiên cứu về các tính chất của khí.
IV. PHƯƠNG TRÌNH TRẠNG THÁI KHÍ LÍ TƯỞNG
1. Khí lý tưởng
Khí lý tưởng là một mô hình được sử dụng để mô tả tính chất của chất khí ở áp suất và nhiệt độ thấp. Mô hình này giả định rằng các phân tử khí:
• Có kích thước vô cùng nhỏ so với thể tích của khối khí.
• Chuyển động không ngừng, va chạm với nhau và với thành của bình chứa.
• Chỉ tương tác với nhau qua các va chạm đàn hồi, không có lực tương tác giữa các phân tử.
• Tuân theo định luật Boyle, định luật Charles và định luật Avogadro.
2. Phương trình trạng thái khí lý tưởng
Phương trình trạng thái khí lý tưởng mô tả mối quan hệ giữa áp suất, thể tích, nhiệt độ và số mol của chất khí:
pV = nRT => = nR = const.
Trong đó R = 8,31 J/(mol.K) gọi là hằng số lí tưởng.
Hay phương trình trạng thái khí lý tưởng có dạng:
Mở rộng: Quá trình biến đổi đẳng tích
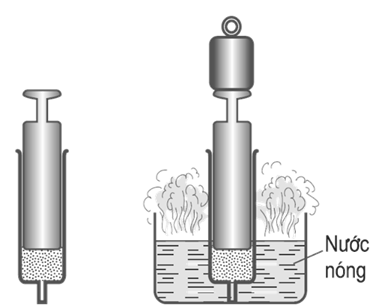
Quá trình biến đổi trạng thái của một khối lượng khí xác định khi giữ thể tích không đổi được gọi là quá trình đẳng tích.
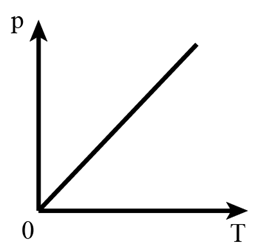
Ở thể tích không đổi, áp suất của một khối lượng khí xác định tỉ lệ thuận với nhiệt độ tuyệt đối của nó: p ~ T hay p = kT => = k = const.
Mô tả quá trình đẳng tích, nhiệt độ tăng thì áp suất tăng
Đồ thị quá trình đẳng tích
3. Phương trình Claperon – Mendeleev:
Phương trình: còn được gọi là phương trình Claperon - Mendeleev.
Trong đó:
• n là số mol: với (m là khối lượng, M là khối lượng mol);
• R hằng số khí, hệ SI: R = 8,31 (J/mol.K);
hệ hỗn hợp ;
4. Ứng dụng của mô hình khí lý tưởng:
Mô hình khí lý tưởng được sử dụng rộng rãi trong nhiều lĩnh vực khác nhau, bao gồm:
• Kỹ thuật: Mô hình này được sử dụng để thiết kế động cơ, máy nén khí, hệ thống lạnh,...
• Hóa học: Tính toán các phản ứng hóa học, xác định thành phần của hỗn hợp khí,...
• Vật lý: Được sử dụng để nghiên cứu các hiện tượng vật lý như sự khuếch tán, dẫn nhiệt,...
• Dự báo thời tiết: Mô hình khí lý tưởng được sử dụng trong dự báo thời tiết
• Hàng không: Tính toán hiệu suất của máy bay và thiết kế các bộ phận khí động học.
V. ÁP SUẤT VÀ ĐỘNG NĂNG PHÂN TỬ CHẤT KHÍ
Áp suất khí tác dụng lên thành bình càng tăng khi các phân tử khi chuyển động nhiệt càng nhanh, khối lượng và mật độ phân tử khí càng lớn.
• Áp suất của chất khí lên thành bình:
• Động năng trung bình của phân tử khí lí tưởng tỉ lệ thuận với nhiệt độ tuyệt đối: với m là khối lượng phân tử, M là khối lượng 1 mol phân tử, k = 1,38.10-23 J / K là hằng số Boltzmann; NA = 6,02.1023 mol-1 là số Avogadro.
B. CÂU HỎI VẬN DỤNG
Câu 1. Nén khí đẳng nhiệt từ thể tích 9 lít đến thể tích 6 lít thì thấy áp suất tăng lên một lượng 40 kPa. Áp suất ban đầu của khí là
A. 20 kPa.
B. 40 kPa.
C. 80 kPa.
D. 60 kPa.
Câu 2. Một khối khí lí tưởng có nhiệt độ ở trạng thái ban đầu là 27 °C. Xác định nhiệt độ của khối khí sau khi đun nóng đẳng áp để thể tích của khối khí tăng lên gấp 3 lần?
A. 627 °C.
B. 2700 °C.
C. 705 °C.
D. 900 °C.
Câu 3. Một khối khí xác định giãn nở đẳng áp từ nhiệt độ t1 = 32 °C đến nhiệt độ t2 = 117 °C, thể tích khối khí tăng thêm 1,7 lít. Tìm thể tích khối khí trước khi giãn nở.
A. 2,6 lít.
B. 4,3 lít.
C. 2,1 lít.
D. 6,1 lít.
Câu 4. Một bình có thể tích 4.10-3 m3 chứa khí lý tưởng ở nhiệt độ 300 K và áp suất 500 kPa. Khí bị rò rỉ cho đến khi áp suất giảm xuống 325 kPa. Tính số mol khí thoát ra ngoài? Coi nhiệt độ không đổi?
A. 0,10.
B. 0,28.
C. 0,42.
D. 0,16.
Câu 5. Hệ thức nào sau đây cho biết mối liên hệ giữa khối lượng riêng r và áp suất p của một khối lượng khí lí tưởng xác định trong quá trình biến đổi đẳng nhiệt?
A. .
B. .
C. .
D. .
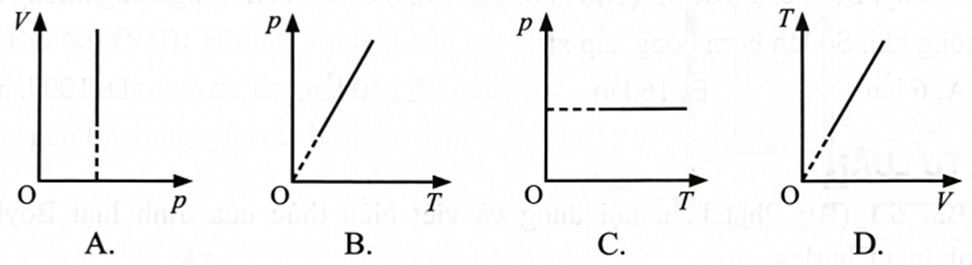
Câu 6. Xét một khối khí lí tưởng xác định thực hiện quá trình biến đổi đẳng áp. Hình nào sau đây diễn tả không đúng dạng đường đẳng áp trong hệ toạ độ tương ứng?
Câu 7. Trong quá trình biến đổi đẳng nhiệt của một khối khí lí tưởng, khi thể tích của khối khí giảm đi 2 lít thì áp suất của nó tăng lên 1,2 lần. Thể tích ban đầu của khối khí là
A. 10 lít.
B. 4 lít.
C. 12 lít.
D. 2,4 lít.
Câu 8. Một bình kín có thể tích 12 lít, chứa nitrogen ở áp suất 80 atm có nhiệt độ 17 °C, xem nitrogen là khí lí tưởng. Khối lượng nitrogen trong bình xấp xỉ giá trị nào sau đây? Biết khối lượng mol của nitrogen là 28 g/mol.
A. 1,13 kg.
B. 1,13 g.
C. 0,113 g.
D. 0,113 kg.
Câu 9. Một hộp hình lập phương có cạnh 10 cm chứa khí lí tưởng đơn nguyên tử ở nhiệt độ 20 °C và áp suất 1,2.106 Pa. Cho số Avogadro NA = 6,02.1023 mol-1. Số phân tử khí chuyển động đập vào một mặt hộp là
A. 9,89.1022.
B. 1,23.1023.
C. 4,95.1022.
D. 4,34.1024.
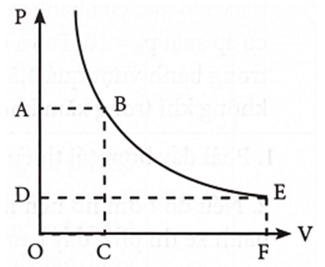
Câu 10. Hình dưới là đồ thị biểu diễn đường đẳng nhiệt của một lượng khí lí tưởng. Sự so sánh nào sau đây giữa diện tích S1 của hình chữ nhật OABC với diện tích S2 của hình chữ nhật ODEF là đúng?
A. S1 > S2.
B. S1 < S2.
C. S1 ≈ S2.
D. S1 = S2.
................................
................................
................................
Xem thử Tài liệu & Đề thi HSA Xem thử Tài liệu & Đề thi VACT Xem thử Tài liệu & Đề thi TSA Xem thử Tài liệu & Đề thi SPT
Xem thêm tài liệu ôn thi đánh giá năng lực HSA, VACT, đánh giá tư duy TSA hay khác:
Xem thêm đề thi lớp 12 các môn học có đáp án hay khác:
Đề ôn thi Tốt nghiệp (các môn học), ĐGNL, ĐGTD các trường có đáp án hay khác:
Tài liệu giáo án lớp 12 các môn học chuẩn khác:
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Lớp 12 Kết nối tri thức
- Soạn văn 12 (hay nhất) - KNTT
- Soạn văn 12 (ngắn nhất) - KNTT
- Giải sgk Toán 12 - KNTT
- Giải sgk Vật Lí 12 - KNTT
- Giải sgk Hóa học 12 - KNTT
- Giải sgk Sinh học 12 - KNTT
- Giải sgk Lịch Sử 12 - KNTT
- Giải sgk Địa Lí 12 - KNTT
- Giải sgk Giáo dục KTPL 12 - KNTT
- Giải sgk Tin học 12 - KNTT
- Giải sgk Công nghệ 12 - KNTT
- Giải sgk Hoạt động trải nghiệm 12 - KNTT
- Giải sgk Giáo dục quốc phòng 12 - KNTT
- Giải sgk Âm nhạc 12 - KNTT
- Giải sgk Mĩ thuật 12 - KNTT
- Lớp 12 Chân trời sáng tạo
- Soạn văn 12 (hay nhất) - CTST
- Soạn văn 12 (ngắn nhất) - CTST
- Giải sgk Toán 12 - CTST
- Giải sgk Vật Lí 12 - CTST
- Giải sgk Hóa học 12 - CTST
- Giải sgk Sinh học 12 - CTST
- Giải sgk Lịch Sử 12 - CTST
- Giải sgk Địa Lí 12 - CTST
- Giải sgk Giáo dục KTPL 12 - CTST
- Giải sgk Tin học 12 - CTST
- Giải sgk Hoạt động trải nghiệm 12 - CTST
- Giải sgk Âm nhạc 12 - CTST
- Lớp 12 Cánh diều
- Soạn văn 12 Cánh diều (hay nhất)
- Soạn văn 12 Cánh diều (ngắn nhất)
- Giải sgk Toán 12 Cánh diều
- Giải sgk Vật Lí 12 - Cánh diều
- Giải sgk Hóa học 12 - Cánh diều
- Giải sgk Sinh học 12 - Cánh diều
- Giải sgk Lịch Sử 12 - Cánh diều
- Giải sgk Địa Lí 12 - Cánh diều
- Giải sgk Giáo dục KTPL 12 - Cánh diều
- Giải sgk Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 - Cánh diều
- Giải sgk Giáo dục quốc phòng 12 - Cánh diều
- Giải sgk Âm nhạc 12 - Cánh diều







 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

