(Ôn thi ĐGNL, ĐGTD) Chuyên đề: Vật lí nhiệt
Chuyên đề Vật lí nhiệt trong tài liệu ôn thi Đánh giá năng lực, Đánh giá tư duy theo cấu trúc mới nhất đầy đủ lý thuyết trọng tâm, các dạng bài & bài tập đa dạng từ cơ bản đến nâng cao giúp Giáo viên & học sinh có thêm tài liệu ôn thi ĐGNL HSA, VACT và ĐGTD TSA đạt kết quả cao.
(Ôn thi ĐGNL, ĐGTD) Chuyên đề: Vật lí nhiệt
Xem thử Tài liệu & Đề thi HSA Xem thử Tài liệu & Đề thi VACT Xem thử Tài liệu & Đề thi TSA Xem thử Tài liệu & Đề thi SPT
Chỉ từ 500k mua trọn bộ Đề thi & Tài liệu ôn thi ĐGNL - ĐGTD năm 2026 của các trường theo cấu trúc mới bản word có lời giải chi tiết:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận đề thi
A. KIẾN THỨC TRỌNG TÂM
I. MÔ HÌNH ĐỘNG HỌC PHÂN TỬ VÀ CẤU TRÚC CỦA CHẤT
1. Mô hình động học phân tử
Mô hình động học phân tử gồm các nội dung cơ bản:
• Các chất được cấu tạo từ các hạt riêng biệt là phân tử.
• Các phân tử chuyển động không ngừng. Nhiệt độ của vật càng cao thì tốc độ chuyển động của các phân tử cấu tạo nên vật càng lớn.
• Giữa các phân tử có lực hút và đẩy gọi chung là lực liên kết phân tử.
2. Cấu trúc của vật chất
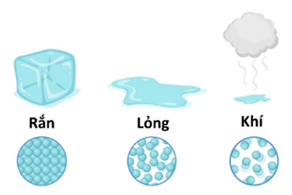
Vật chất thường tồn tại ở ba trạng thái cơ bản là: thể rắn, thể lỏng và thể khí.
- Khoảng cách giữa các phân tử càng lớn thì lực liên kết giữa chúng càng yếu.
- Các phân tử sắp xếp có trật tự thì lực liên kết giữa chúng mạnh.
Các trạng thái của vật chất
• Ở thể rắn các phân tử rất gần nhau và chúng được sắp xếp theo một trật tự hình học xác định. Lực tương tác giữa các phân tử rất mạnh, giữ cho chúng không di chuyển tự do mà chỉ có thể dao động quanh vị trí cân bằng xác định. Do đó, chất rắn kết tinh luôn có thể tích và hình dạng riêng xác định.
• Ở thể lỏng, các phân tử ở xa nhau hơn so với các phân tử trong chất rắn. Lực tương tác giữa các phân tử chất lỏng nhỏ hơn trong chất rắn nên giữ cho các phân tử không bị phân tán ra xa nhau, do đó chất lỏng có thể tích riêng xác định. Tuy nhiên lực tương tác này chưa đủ lớn nên các phân tử ở thể lỏng cũng dao động quanh vị trí cân bằng nhưng các vị trí cân bằng này không cố định mà luôn luôn thay đổi. Do đó, chất lỏng rất khó bị nén, nó có thể tích xác định nhưng không có hình dạng riêng mà có hình dạng của phần bình chứa nó.
• Ở thể khí, các phân tử ở xa nhau hơn so với các phân tử trong chất lỏng. Khoảng cách giữa các phân tử rất lớn so với kích thước của chúng nên lực tương tác giữa các phân tử rất yếu (trừ khi va chạm nhau), nên các phân tử chuyển động hoàn toàn hỗn loạn. Do đó, khối chất khí không có hình dạng và thể tích riêng mà nó có hình dạng và thể tích của bình chứa nó và có thể nén được dễ dàng.
|
Cấu trúc |
Thể rắn |
Thể lỏng |
Thể khí |
|
Khoảng cách giữa các phân tử |
Rất gần nhau (cỡ kích thước phân tử) |
Xa nhau |
Rất xa nhau (gấp hàng chục lần kích thước phân tử) |
|
Sự sắp xếp của các phân tử |
Trật tự |
Kém trật tự hơn so với thể rắn |
Không có trật tự |
|
Chuyển động của các phân tử |
Chỉ dao động quanh vị trí cân bằng cố định |
Dao động quanh vị trí cân bằng luôn luôn thay đổi |
Chuyển động hỗn loạn |
|
Hình dạng |
Xác định |
Phụ thuộc phần bình chứa nó |
Phụ thuộc bình chứa |
|
Thể tích |
Xác định |
Xác định |
Phụ thuộc bình chứa |
II. SỰ CHUYỂN THỂ CỦA CÁC CHẤT
1. Sự chuyển thể của các chất:
• Khi các điều kiện như nhiệt độ, áp suất thay đổi, chất có thể chuyển từ thể này sang thể khác.
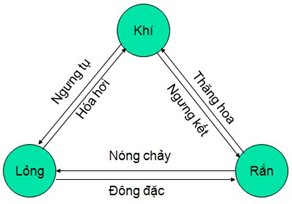
- Quá trình chuyển từ thể rắn sang thể lỏng của các chất được gọi là sự nóng chảy. Quá trình chuyển ngược lại từ thể lỏng sang thể rắn được gọi là đông đặc.
- Quá trình chuyển từ thể lỏng sang thể khí (hơi) của các chất được gọi là sự hóa hơi. Quá trình chuyển ngược lại, từ thể khí (hơi) sang thể lỏng được gọi là sự ngưng tụ.
|
• Sự thay đổi trạng thái của vật chất được thể hiện như hình vẽ bên cạnh. Chú ý: Một số chất như băng phiến, đá khô (ở thể rắn) có khả năng chuyển trực tiếp sang thể khí khi nó nhận nhiệt. Hiện tượng trên gọi là sự thăng hoa và ngược lại gọi là sự ngưng kết. |
|
2. Sự nóng chảy:
Quá trình chuyển từ thể rắn sang thể lỏng của các chất gọi là sự nóng chảy.
a. Đặc điểm:
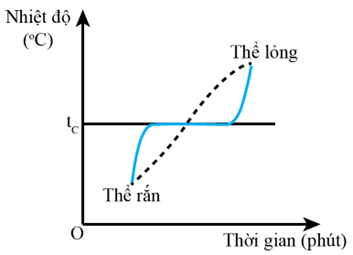
• Mỗi chất rắn kết tinh có một nhiệt độ nóng chảy xác định ở mỗi áp suất cho trước.
• Các chất rắn vô định hình không có nhiệt độ nóng chảy xác định.
Đồ thị thể hiện sự thay đổi nhiệt độ theo thời gian trong quá trình nóng chảy của chất rắn kết tinh (đường nét liền) và chất rắn vô định hình (đường nét đứt)
b. Giải thích sự nóng chảy của chất rắn kết tinh
Ở áp suất không đổi, các hạt ở thể rắn liên kết chặt chẽ với nhau, chúng dao động quanh các vị trí cân bằng xác định. Khi nung nóng chất rắn, các hạt được cung cấp nhiệt năng làm tốc độ chuyển động nhiệt của nó tăng lên, mức độ trật tự trong cấu trúc của các hạt giảm đi. Khi đạt đến nhiệt độ nóng chảy, chuyển động của các hạt giống như chuyển động của các phân tử chất lỏng, đó là quá trình nóng chảy.
c. Ứng dụng
Sự nóng chảy được ứng dụng trong công nghiệp luyện kim, hàn điện, thực phẩm.
3. Sự hoá hơi:
|
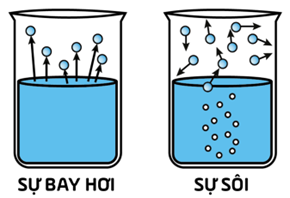
Sự hoá hơi là quá trình chuyển từ thể lỏng sang thể khí. Sự hoá hơi thể hiện qua hai hình thức đó là sự bay hơi và sự sôi. a. Sự bay hơi: Sự hoá hơi xảy ra trên bề mặt chất lỏng gọi là sự bay hơi. Sự bay hơi xảy ra ở nhiệt độ bất kì và luôn kèm theo sự ngưng tụ. |
|
Tốc độ bay hơi của chất lỏng càng nhanh nếu diện tích mặt thoáng càng lớn, tốc độ gió càng lớn, nhiệt độ càng cao và độ ẩm không khí càng thấp.
Giải thích sự bay hơi: Các phân tử chất lỏng tham gia chuyển động nhiệt, trong đó có những phân tử ở bề mặt chất lỏng chuyển động hướng ra ngoài chất lỏng. Một số phân tử chất lỏng này có động năng đủ lớn, thắng lực tương tác giữa các phân tử chất lỏng với nhau thì chúng có thể thoát ra khỏi mặt thoáng, trở thành các phân tử hơi.
b. Sự sôi:
Sự hoá hơi xảy ra ở bên trong và trên bề mặt chất lỏng gọi là sự sôi. Sự sôi xảy ra ở nhiệt độ sôi.
Nhiệt độ sôi của chất lỏng phụ thuộc áp suất khí trên mặt thoáng và bản chất của chất lỏng. Trong suốt thời gian sôi, nhiệt độ chất lỏng không thay đổi.
Giải thích sự sôi của chất lỏng: Khi đun chất lỏng đến nhiệt độ sôi, do tiếp tục được cung cấp nhiệt lượng nên các phân tử chất lỏng chuyển động nhiệt mạnh hơn, làm phá vỡ sự liên kết giữa các phân tử chất lỏng với nhau, phân tử chất lỏng chuyển sang phân tử hơi. Hiện tượng này xảy ra với tất cả các phân tử chất lỏng ở bên trong và trên bề mặt khối chất lỏng.
c. Tác dụng của sự bay hơi
Sự bay hơi nước từ biển, sông, hồ, ... tạo thành mây, sương mù, mưa, làm cho khí hậu điều hoà và cây cối phát triển. Sự bay hơi của nước biển được sử dụng trong ngành sản xuất muối. Sự bay hơi của khí ammonia, difluoromethane... được sử dụng trong kĩ thuật làm lạnh như máy điều hòa không khí, tủ lạnh.
III. ĐỊNH LUẬT 1 CỦA NHIỆT ĐỘNG LỰC HỌC
1. Nội năng
a) Khái niệm
Tổng động năng và thế năng của các phân tử cấu tạo nên vật được gọi là nội năng của vật. Nội năng của một vật phụ thuộc vào nhiệt độ và thể tích của vật. Nội năng được kí hiệu bằng chữ U, có đơn vị là jun (J).
Trong nhiệt động lực học người ta chủ yếu quan tâm đến độ biến thiên nội năng ΔU của vật, là phần nội năng tăng lên hoặc giảm đi trong một quá trình.
b) Các cách làm thay đổi nội năng
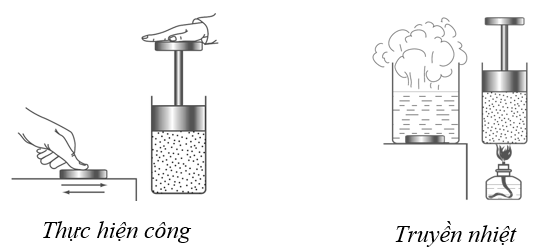
Có hai cách làm thay đổi nội năng của vật là thực hiện công và truyền nhiệt. Trong quá trình thực hiện công có sự chuyển hóa từ một dạng năng lượng khác (ví dụ như cơ năng) sang nội năng. Trong quá trình truyền nhiệt không có sự chuyển hóa năng lượng từ dạng này sang dạng khác mà chỉ có sự truyền nội năng từ vật này sang vật khác.
- Quá trình thực hiện công làm cho nội năng của vật thay đổi, vật nhận công thì nội năng tăng, vật thực hiện công cho vật khác thì nội năng giảm.
- Khi hai vật có nhiệt độ khác nhau tiếp xúc với nhau thì xảy ra quá trình truyền nhiệt. Quá trình này làm thay đổi nội năng của các vật.
2. Định luật 1 của nhiệt động lực học
Theo định luật bảo toàn và chuyển hoá năng lượng thì độ biến thiên nội năng của vật bằng tổng công và nhiệt lượng mà vật nhận được:
∆U = A + Q
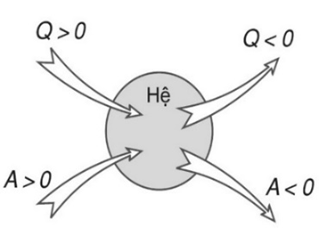
Quy ước dấu:
• ∆U > 0: Nội năng tăng; ∆U < 0: Nội năng giảm.
• A > 0: Hệ nhận công; A < 0: Hệ thực hiện công.
• Q > 0: Hệ nhận nhiệt lượng; Q < 0: Hệ truyền nhiệt lượng.
IV. THANG NHIỆT ĐỘ
1. Sự truyền năng lượng nhiệt
a) Năng lượng nhiệt
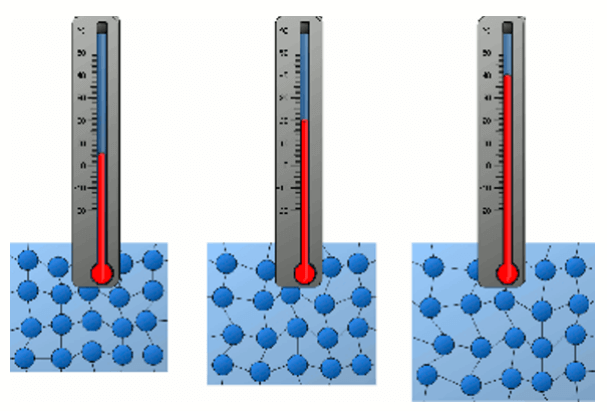
Năng lượng nhiệt là động năng gắn liền với chuyển động hỗn loạn của các nguyên tử và phân tử cấu tạo nên vật.
Ở mẫu nước có nhiệt độ cao hơn thì các phân tử chuyển động nhanh hơn
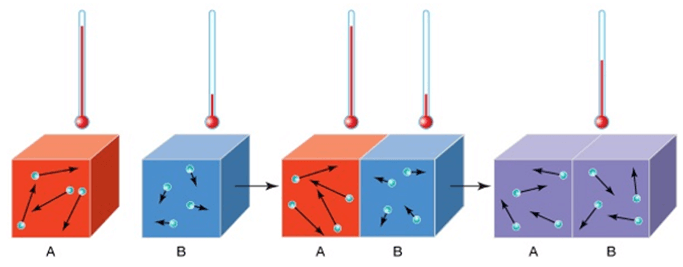
b) Sự truyền năng lượng nhiệt giữa hai vật ở các nhiệt độ khác nhau
Khi cho hai vật chênh lệch nhiệt độ tiếp xúc nhau, năng lượng nhiệt luôn truyền từ vật có nhiệt độ cao hơn sang vật có nhiệt độ thấp hơn. Quá trình truyền nhiệt kết thúc khi hai vật ở cùng nhiệt độ (lúc này hai vật ở trạng thái cân bằng nhiệt).
Phần năng lượng nhiệt truyền từ vật có nhiệt độ cao hơn sang vật có nhiệt độ thấp hơn được gọi là nhiệt lượng, để đo năng lượng nhiệt người ta dùng nhiệt lượng kế.
2. Thang nhiệt độ
a) Nhiệt kế
Nhiệt kế là thiết bị dùng để đo nhiệt độ. Nhiệt kế được chế tạo dựa trên một số tính chất vật lí phụ thuộc vào nhiệt độ của các chất, các vật liệu, các linh kiện điện và điện tử,...
Tính chất vật lí được sử dụng nhiều trong trong việc chế tạo nhiệt kế là sự nở vì nhiệt. Các nhiệt kế thường dùng là các nhiệt kế được chế tạo dựa trên sự nở dài của cột chất lỏng trong ống thuỷ tinh (nhiệt kế rượu, nhiệt kế thuỷ ngân, nhiệt kế dầu).
Sự nở dài của một thanh kim loại mỏng thẳng hoặc xoắn ốc được dùng trong việc chế tạo các loại nhiệt kế kim loại.
Sự nở khối của một lượng khí xác định ở áp suất không đổi được dùng để chế tạo các loại nhiệt kế khí.
b) Thang nhiệt độ
Các loại thang đo nhiệt độ
Có thể đo nhiệt độ của vật theo các thang đo khác nhau. Một số loại thang nhiệt độ (còn gọi là nhiệt giai) thông dụng như: thang nhiệt độ Celsius, thang nhiệt độ Kelvin, thang nhiệt độ Fahrenheit.
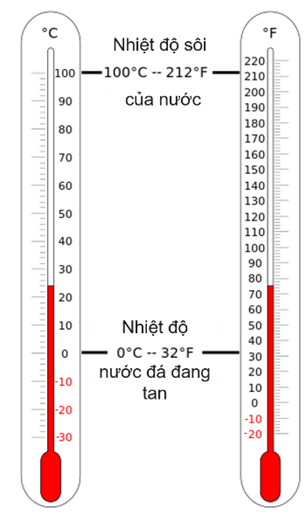
Trong thang nhiệt độ Celsius, chọn hai mốc nhiệt độ là nhiệt độ của nước đá (nước tinh khiết đóng băng) đang tan ở áp suất 1 atm là 0 °C và nhiệt độ sôi của nước tinh khiết ở áp suất 1 atm là 100 °C. Từ vạch 0°C đến vạch 100°C chia thành 100 khoảng bằng nhau, mỗi khoảng ứng với 1 °C. Nhiệt độ trong thang đo này được kí hiệu là t. Đơn vị là độ Celsius (kí hiệu: °C).
Thang nhiệt độ này được lấy theo tên của nhà vật lí thiên văn người Thụy Điển là Anders Celsius (An-đo Xen-xi-út) (1701 – 1744), người đề xuất thang đo năm 1742.
Thang nhiệt độ Kelvin (thang nhiệt độ tuyệt đối), chọn hai mốc nhiệt độ là nhiệt độ mà tại đó động năng chuyển động nhiệt của các phân tử, nguyên tử cấu tạo nên các chất bằng không là 0 K (gọi là độ không tuyệt đối) và chọn nhiệt độ nước tinh khiết tồn tại đồng thời ở thể rắn, lỏng và hơi là 273,16 K (nhiệt độ điểm ba của nước). Trong khoảng giữa hai giá trị nhiệt độ này, chia thành 273,16 khoảng bằng nhau, mỗi khoảng là 1 K.
Trong thang đo này, nhiệt độ được kí hiệu là T, đơn vị là Kelvin (kí hiệu: K). Một độ chia trên thang nhiệt độ Kelvin bằng một độ chia trên thang nhiệt độ Celsius và tại 0 °C trong thang nhiệt độ Celsius ứng với 273,15 K trong thang nhiệt độ Kelvin.
c) Nhiệt độ không tuyệt đối
Nhiệt độ không tuyệt đối (0 K) là nhiệt độ mà tại đó động năng chuyển động nhiệt của các phân tử cấu tạo nên vật chất bằng không và thế năng của chúng là tối thiểu.
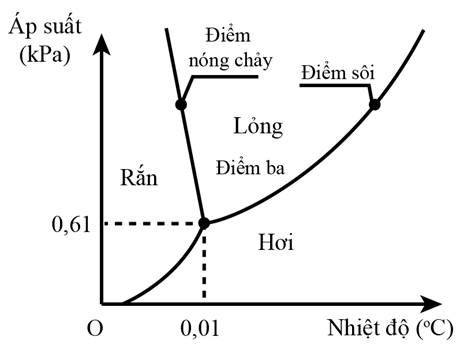
d) Điểm ba của nước
Nhiệt độ mà nước tinh khiết có thể tồn tại đồng thời ở cả ba thể rắn, lỏng và hơi, trong trạng thái cân bằng nhiệt ở áp suất tiêu chuẩn (nhiệt độ này có độ lớn là 0,01 °C), được gọi là nhiệt độ điểm ba của nước.
e) Chuyển đổi nhiệt độ giữa các thang đo
Gọi t là giá trị nhiệt độ của vật theo thang nhiệt độ Celcius và T là giá trị nhiệt độ của vật đó theo thang nhiệt độ Kelvin thì:
T(K) = t(°C) + 273 hoặc t(°C) = T(K) - 273
Gọi t là giá trị nhiệt độ của vật theo thang nhiệt độ Celcius và t’ là giá trị nhiệt độ của vật đó theo thang nhiệt độ Fahrenheit thì:
t'(°C) = 32 + 1,8t°C hoặc t(°C) =
V. NHIỆT DUNG RIÊNG, NHIỆT NÓNG CHẢY RIÊNG, NHIỆT HOÁ HƠI RIÊNG
1. Nhiệt dung riêng
Nhiệt lượng vật toả ra hoặc thu vào khi nhiệt độ thay đổi: Q = mc∆t = mc(t2 - t1)
Trong đó:
• m là khối lượng của vật (kg).
• c là nhiệt dung riêng của vật (J/kg.K).
• t1 là nhiệt độ ban đầu của vật.
• t2 là nhiệt độ lúc sau của vật.
2. Nhiệt nóng chảy riêng
Nhiệt nóng chảy riêng của một chất là nhiệt lượng cần thiết để biến đổi 1 kg chất đó từ pha rắn sang pha lỏng mà không thay đổi nhiệt độ.
• Công thức tính nhiệt nóng chảy riêng:
• Trong quá trình nóng chảy, nhiệt lượng hấp thụ được sử dụng để phá vỡ liên kết giữa các phân tử. Các phân tử được giải phóng khỏi vị trí cố định của chúng và có thể chuyển động nhiệt hỗn loạn.
• Khi chất lỏng đông đặc ở điểm đóng băng để thành pha rắn, thì nó sẽ tỏa ra nhiệt lượng Q.
3. Nhiệt hóa hơi riêng
Nhiệt hóa hơi riêng của một chất được là lượng nhiệt cần thiết để chuyển 1 kg chất đó từ pha lỏng sang pha khí mà không thay đổi nhiệt độ:
• Công thức tính nhiệt hóa hơi riêng:
• Khi một chất lỏng sôi, nhiệt lượng do nó hấp thụ được sử dụng để phá vỡ hoàn toàn liên kết giữa các phân tử đồng thời sinh công để chống lại áp suất khí quyển khi hơi giãn nở.
• Khi hơi ngưng tụ để chuyển thành pha lỏng, thì nó sẽ tỏa ra nhiệt lượng Q.
• Nhiệt hóa hơi riêng của một chất thường lớn hơn nhiệt nóng chảy riêng.
4. Phương trình cân bằng nhiệt
Trong một hệ cô lập về nhiệt – không trao đổi nhiệt độ với môi trường bên ngoài, thì tổng nhiệt lượng mà các vật trong hệ tỏa ra bằng tổng nhiệt lượng các vật trong hệ thu vào:
với t là nhiệt độ của hệ khi xảy ra cân bằng, ttỏa và tthu lần lượt là nhiệt độ ban đầu của vật tỏa nhiệt và vật thu nhiệt trong hệ.
Phương trình (1) được gọi là phương trình cân bằng nhiệt.
5. Cách xác định nhiệt nóng chảy riêng qua thí nghiệm
• Nhiệt lượng cung cấp: Q = mc∆t =>
• Ta có
6. Cách xác định nhiệt nóng chảy riêng qua thí nghiệm
• Nhiệt lượng cung cấp:
• Trong quá trình chuyển từ thể rắn sang thể lỏng không có sự thay đổi về nhiệt độ.
• Ta có
7. Cách xác định nhiệt hoá hơi riêng qua thí nghiệm
• Nhiệt lượng cung cấp: Q = Lm =>
• Trong quá trình chuyển từ thể lỏng sang thể khí không có sự thay đổi về nhiệt độ.
• Ta có .
B. CÂU HỎI VẬN DỤNG
Câu 1. Một học sinh nhìn qua kính hiển vi vào một hộp nhỏ chứa không khí và khói được chiếu sáng. Phát biểu nào sau đây đúng?
A. Trong hộp có các hạt khói.
B. Trong hộp có các chấm đen.
C. Các hạt khói chuyển động hỗn loạn.
D. Các phân tử khói bị các phân tử không khí bắn phá.
Câu 2. Cho hai vật có nhiệt độ khác nhau tiếp xúc với nhau. Năng lượng nhiệt được truyền từ
A. vật có nhiệt độ cao hơn sang vật có nhiệt độ thấp hơn.
B. vật có khối lượng lớn hơn sang vật có khối lượng nhỏ hơn.
C. vật ở trên cao sang vật ở dưới thấp.
D. vật ở dưới thấp sang vật ở trên cao.
Câu 3. Một vật có nhiệt độ theo thang Fahrenheit là 95 °F. Nhiệt độ của vật theo thang Kelvin (làm tròn) là
A. 35 K.
B. 308 K.
C. 368 K.
D. 178 K.
Câu 4. Biết nhiệt nóng chảy riêng của thiếc là 0,61.105 J/kg. Nhiệt lượng cần cung cấp cho một cuộn thiếc hàn có khối lượng 800 g nóng chảy hoàn toàn ở nhiệt độ nóng chảy là
A. 48 800 J.
B. 4 880 J.
C. 4,88.107 J.
D. 76 250 J.
Câu 5. Giả thiết rằng rượu ethylic có nhiệt hoá hơi riêng là 0,9.106 J/kg và khối lượng riêng là 0,8 kg/lít. Nhiệt lượng cần thiết để 10 lít rượu ethylic hoá hơi hoàn toàn ở nhiệt độ sôi là
A. 7,2.103 J.
B. 1,125.105 J.
C. 7,2.106 J.
D. 9.105 J.
Câu 6. Hệ thức nào sau đây phù hợp với quá trình khối khí được làm lạnh và giữ nguyên thể tích?
A. DU = A, A > 0.
B. DU = Q, Q > 0.
C. DU = A, A < 0.
D. DU = Q, Q < 0.
Câu 7: Biết nhiệt nóng chảy riêng của nhôm là 4,00.105 J/kg, của chì là 0,25.105 J/kg. Nhiệt lượng cần thiết để làm nóng chảy hoàn toàn 1 kg nhôm ở nhiệt độ nóng chảy có thể làm nóng chảy được bao nhiêu kilôgam chì?
A. 1,6 kg.
B. 1 kg.
C. 16 kg.
D. 160 kg.
Câu 8: Cho biết mối liên hệ giữa thang nhiệt độ Celsius và thang nhiệt độ Fahrenheit là T (°F) = 1,8t (°C) + 32. Một vật có nhiệt độ theo thang Celsius là 52 °C. Nhiệt độ của vật theo thang Fahrenheit là
A. 125,6 °F.
B. 152,6 °F.
C. 126,5 °F.
D. 162,5 °F.
Câu 9: Nhiệt lượng của một vật đồng chất thu vào là 6900 J làm nhiệt độ của vật tăng thêm 50 °C. Bỏ qua sự trao đổi nhiệt với môi trường. Biết khối lượng của vật là 300 g, nhiệt dung riêng của chất làm vật là
A. 460 J/kg.K.
B. 1 150 J/kg.K.
C. 71,2 J/kg.K.
D. 41,4 J/kg.K.
Câu 10. Phát biểu nào sau đây là đúng?
A. Nội năng là một dạng năng lượng.
B. Nội năng là một dạng nhiệt lượng.
C. Nội năng của vật A lớn hơn nội năng của vật B thì nhiệt độ của vật A cũng lớn hơn nhiệt độ của vật B.
D. Nội năng của vật chỉ thay đổi trong quá trình truyền nhiệt, không thay đổi trong quá trình thực hiện công.
................................
................................
................................
Xem thử Tài liệu & Đề thi HSA Xem thử Tài liệu & Đề thi VACT Xem thử Tài liệu & Đề thi TSA Xem thử Tài liệu & Đề thi SPT
Xem thêm tài liệu ôn thi đánh giá năng lực HSA, VACT, đánh giá tư duy TSA hay khác:
- (Ôn thi ĐGNL, ĐGTD) Chuyên đề: Khí lí tưởng
- (Ôn thi ĐGNL, ĐGTD) Chuyên đề: Từ trường
- (Ôn thi ĐGNL, ĐGTD) Chuyên đề: Vật lí hạt nhân
- (Ôn thi ĐGNL, ĐGTD) Chuyên đề: Dao động
- (Ôn thi ĐGNL, ĐGTD) Chuyên đề: Sóng
- (Ôn thi ĐGNL, ĐGTD) Chuyên đề: Điện trường
- (Ôn thi ĐGNL, ĐGTD) Chuyên đề: Dòng điện. Mạch điện
- (Ôn thi ĐGNL, ĐGTD) Chuyên đề: Động lực học
- (Ôn thi ĐGNL, ĐGTD) Chuyên đề: Bảo toàn động lượng - bảo toàn năng lượng
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Lớp 12 Kết nối tri thức
- Soạn văn 12 (hay nhất) - KNTT
- Soạn văn 12 (ngắn nhất) - KNTT
- Giải sgk Toán 12 - KNTT
- Giải sgk Vật Lí 12 - KNTT
- Giải sgk Hóa học 12 - KNTT
- Giải sgk Sinh học 12 - KNTT
- Giải sgk Lịch Sử 12 - KNTT
- Giải sgk Địa Lí 12 - KNTT
- Giải sgk Giáo dục KTPL 12 - KNTT
- Giải sgk Tin học 12 - KNTT
- Giải sgk Công nghệ 12 - KNTT
- Giải sgk Hoạt động trải nghiệm 12 - KNTT
- Giải sgk Giáo dục quốc phòng 12 - KNTT
- Giải sgk Âm nhạc 12 - KNTT
- Giải sgk Mĩ thuật 12 - KNTT
- Lớp 12 Chân trời sáng tạo
- Soạn văn 12 (hay nhất) - CTST
- Soạn văn 12 (ngắn nhất) - CTST
- Giải sgk Toán 12 - CTST
- Giải sgk Vật Lí 12 - CTST
- Giải sgk Hóa học 12 - CTST
- Giải sgk Sinh học 12 - CTST
- Giải sgk Lịch Sử 12 - CTST
- Giải sgk Địa Lí 12 - CTST
- Giải sgk Giáo dục KTPL 12 - CTST
- Giải sgk Tin học 12 - CTST
- Giải sgk Hoạt động trải nghiệm 12 - CTST
- Giải sgk Âm nhạc 12 - CTST
- Lớp 12 Cánh diều
- Soạn văn 12 Cánh diều (hay nhất)
- Soạn văn 12 Cánh diều (ngắn nhất)
- Giải sgk Toán 12 Cánh diều
- Giải sgk Vật Lí 12 - Cánh diều
- Giải sgk Hóa học 12 - Cánh diều
- Giải sgk Sinh học 12 - Cánh diều
- Giải sgk Lịch Sử 12 - Cánh diều
- Giải sgk Địa Lí 12 - Cánh diều
- Giải sgk Giáo dục KTPL 12 - Cánh diều
- Giải sgk Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 - Cánh diều
- Giải sgk Giáo dục quốc phòng 12 - Cánh diều
- Giải sgk Âm nhạc 12 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

