100+ Đề thi Tốt nghiệp THPT Hóa học năm 2026 (có đáp án)
Tuyển tập đề ôn thi tốt nghiệp THPT môn Hóa học năm 2026 được các Thầy/Cô biên soạn công phu, cực sát đề chính thức giúp bạn ôn luyện môn Hóa học thi tốt nghiệp THPT đạt kết quả cao.
100+ Đề thi Tốt nghiệp THPT Hóa học năm 2026 (có đáp án)
Xem thử Đề thi Tốt nghiệp THPT Hóa 2025 Xem thử Đề thi thử Tốt nghiệp THPT Hóa 2025 Xem thử Chuyên đề ôn thi Tốt nghiệp THPT Hóa Xem thử 1000 câu trắc nghiệm Hóa
Chỉ từ 500k mua trọn bộ đề thi thử Hóa năm 2026 của các Trường/Sở trên cả nước hoặc bộ đề thi Hóa biên soạn theo đề tham khảo theo cấu trúc mới bản word có lời giải chi tiết:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận đề thi
Đề thi Tốt nghiệp THPT Hóa học (các năm)
- Đề chính thức môn Hóa học thi Tốt nghiệp THPT năm 2025
- 1000 câu trắc nghiệm lý thuyết Hóa thi Tốt nghiệp 2026
- Đề tham khảo Tốt nghiệp THPT Hóa học năm 2025
- Đề Tốt nghiệp THPT Hóa học 2026 theo form mới
- Đề ôn thi Tốt nghiệp THPT Hóa học năm 2026
- Đề minh họa Tốt nghiệp THPT Hóa học năm 2025
- Đề tham khảo Hóa học năm 2025
Đề thi thử Tốt nghiệp THPT Hóa 2026 (cả nước)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Lê Quý Đôn (Tp HCM)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Hậu Lộc 1 (Thanh Hóa)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Hậu Lộc 4 (Thanh Hóa)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Bỉm Sơn (Thanh Hóa)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Nguyễn Thị Giang (Phú Thọ)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Hưng Nhân (Hưng Yên)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Chuyên Chu Văn An (Lạng Sơn)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Cửa Lò (Nghệ An)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Cẩm Phả (Quảng Ninh)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Chuyên Lê Thánh Tông (Đà Nẵng)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT An Dương (Hải Phòng)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Vũng Tàu (TP. HCM)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Cẩm Xuyên (Hà Tĩnh)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 Cụm trường THPT TT1-QV1-LVT (Bắc Ninh)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 Liên trường THPT (Bắc Ninh)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Chuyên Bắc Ninh (Bắc Ninh)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Đồng Đậu (Phú Thọ)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Hàn Thuyên (Bắc Ninh)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Thuận Thành Số 1 (Bắc Ninh)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Hàm Rồng (Thanh Hóa)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Bỉm Sơn (Thanh Hóa)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Chuyên Trần Phú (Hải Phòng)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Bạch Đằng (Hải Phòng)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Lương Tài Số 2 (Bắc Ninh)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 trường THPT Võ Thị Sáu (Phú Thọ)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 Cụm các trường THPT (Bắc Ninh)
Đề thi thử Hóa Tốt nghiệp THPT 2025-2026 Cụm 13 trường THPT (Hải Phòng)
21 Chuyên đề ôn thi Tốt nghiệp THPT Hóa 2026
- Tổng ôn kiến thức Hóa học 12
Chuyên đề: Hợp chất chứa nitrogen (Ôn thi Hóa học Tốt nghiệp 2026)
Chuyên đề: Pin điện và điện phân (Ôn thi Hóa học Tốt nghiệp 2026)
Chuyên đề: Đại cương kim loại (Ôn thi Hóa học Tốt nghiệp 2026)
Chuyên đề: Nguyên tố nhóm IA và nhóm IIA (Ôn thi Hóa học Tốt nghiệp 2026)
- Tổng ôn kiến thức Hóa học 11
Chuyên đề: Cân bằng hoá học (Ôn thi Hóa học Tốt nghiệp 2026)
Chuyên đề: Nitrogen – sulfur (Ôn thi Hóa học Tốt nghiệp 2026)
Chuyên đề: Đại cương về hoá học hữu cơ (Ôn thi Hóa học Tốt nghiệp 2026)
Chuyên đề: Dẫn xuất halogen - alcohol - phenol (Ôn thi Hóa học Tốt nghiệp 2026)
Chuyên đề: Hợp chất carbonyl - carboxylic acid (Ôn thi Hóa học Tốt nghiệp 2026)
- Tổng ôn kiến thức Hóa học 10
Chuyên đề: Cấu tạo nguyên nguyên tử (Ôn thi Hóa học Tốt nghiệp 2026)
Chuyên đề: Bảng tuần hoàn các nguyên tố hóa học (Ôn thi Hóa học Tốt nghiệp 2026)
Chuyên đề: Liên kết hóa học (Ôn thi Hóa học Tốt nghiệp 2026)
Chuyên đề: Phản ứng oxi hóa - khử (Ôn thi Hóa học Tốt nghiệp 2026)
Chuyên đề: Năng lượng hóa học (Ôn thi Hóa học Tốt nghiệp 2026)
Chuyên đề: Nguyên tố nhóm VIIA (Nhóm Halogen) (Ôn thi Hóa học Tốt nghiệp 2026)
Đề thi thử Tốt nghiệp THPT Hóa năm 2024-2025
Đề thi thử Tốt nghiệp THPT Hóa năm 2024-2025 Trường THPT Tiên Du
Đề thi thử Tốt nghiệp THPT Hóa năm 2024-2025 Trường THCS-THPT Nguyễn Khuyến
Đề thi thử Tốt nghiệp THPT Hóa năm 2024-2025 Trường THPT chuyên Bắc Ninh
Đề thi thử Tốt nghiệp THPT Hóa năm 2024-2025 Trường THPT Yên Phong
Đề thi thử Tốt nghiệp THPT Hóa năm 2024-2025 Trường THPT Lương Tài
Đề thi thử Tốt nghiệp THPT Hóa năm 2024-2025 Trường THPT Yên Dũng
Đề thi thử Tốt nghiệp THPT Hóa năm 2024-2025 Trường THPT Nguyễn Đăng Đạo
Đề thi thử Tốt nghiệp THPT Hóa năm 2024-2025 Trường THPT Sơn Tây
Đề thi thử Tốt nghiệp THPT Hóa năm 2024-2025 Sở GD&ĐT Tuyên Quang
Đề thi thử Tốt nghiệp THPT Hóa năm 2024-2025 Sở GD&ĐT Ninh Bình
Đề thi thử Tốt nghiệp THPT Hóa năm 2024-2025 trường THPT Chuyên Trần Phú (Hải Phòng)
Đề thi thử Tốt nghiệp THPT Hóa năm 2024-2025 Sở GD&ĐT Vĩnh Phúc
Đề thi thử Tốt nghiệp THPT Hóa năm 2024-2025 Sở GD&ĐT Hà Tĩnh
Đề thi thử Tốt nghiệp THPT Hóa năm 2024-2025 trường THPT Chuyên Phan Bội Châu (Nghệ An)
Đề thi thử Tốt nghiệp THPT Hóa năm 2024-2025 trường THPT Khoái Châu (Hưng Yên)
Đề thi thử Tốt nghiệp THPT Hóa năm 2024-2025 Sở GD&ĐT Thanh Hóa
Đề thi thử Tốt nghiệp THPT Hóa năm 2024-2025 Sở GD&ĐT Thái Nguyên
Đề thi thử Tốt nghiệp THPT Hóa năm 2024-2025 Sở GD&ĐT Lạng Sơn
Lưu trữ: Đề minh họa + đề chính thức Hóa học tốt nghiệp THPT (các năm)
Xem thử Đề thi Tốt nghiệp THPT Hóa 2025 Xem thử Đề thi thử Tốt nghiệp THPT Hóa 2025 Xem thử Chuyên đề ôn thi Tốt nghiệp THPT Hóa Xem thử 1000 câu trắc nghiệm Hóa
|
SỞ GD & ĐT HẢI PHÒNG ĐỀ CHÍNH THỨC (Đề thi có 08 trang) |
ĐỀ THI THỬ TỐT NGHIỆP THPT LẦN 1 NĂM HỌC 2025-2026 Môn thi: HOÁ HỌC Ngày thi: … /01/2026 Thời gian làm bài: 50 phút, không kể thời gian phát đề
|
|
|
|
Mã đề thi 0111 |
|
Họ, tên thí sinh:.......................................................................................
Số báo danh:............................................................................................
Cho biết:
- Nguyên tử khối của các nguyên tố: H = 1; He = 4; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; S = 32; Cl = 35,5; K = 39; Ca = 40; Cr = 52; Mn = 55; Fe = 56; Cu = 64; Zn = 65; Br = 80; Ag = 108; Ba = 137.
- Bảng số sóng hấp thụ đặc trưng trên phổ hồng ngoại (IR) của một số nhóm chức:
|
Loại hợp chất |
Liên kết |
Số sóng (cm-1) |
|
Alcohol |
O-H |
3500 - 3200 |
|
Aldehyde |
C=O |
1740 - 1685 |
|
C-H |
2830 - 2695 |
|
|
Carboxylic acid |
C=O |
1760 - 1690 |
|
O-H |
3300 - 2500 |
|
|
Ester |
C=O |
1750 - 1715 |
|
C-O |
1300 - 1000 |
|
|
Ketone |
C=O |
1715 - 1666 |
|
Amine |
N-H |
3300 - 3000 |
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Chất nào sau đây được dùng làm chất giặt rửa tổng hợp?
A. C17H35COONa.
B. CH3–C6H4–ONa.
C. CH3[CH2]11–C6H4–SO3Na.
D. C15H31COONa.
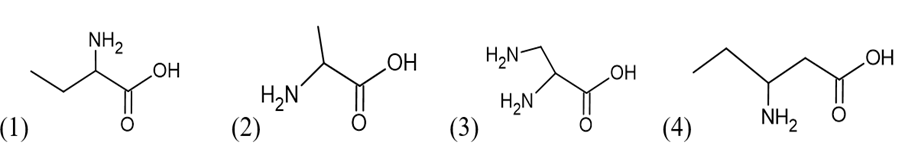
Câu 2. Cho các hợp chất có công thức cấu tạo dưới đây:
Trong số các chất trên, những hợp chất thuộc loại α-amino acid là
A. chất (1) và chất (2).
B. chất (1) và chất (3).
C. chất (1), chất (2) và chất (3).
D. chất (2), chất (3) và chất (4).
Câu 3. Hợp chất sau thuộc loại polysaccharide là
A. peptide.
B. protein.
C. maltose.
D. cellulose.
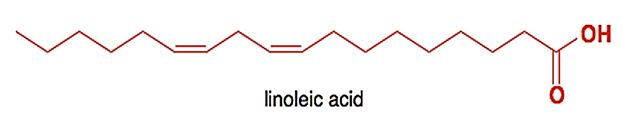
Câu 4. Linoleic acid là một trong những acid béo có lợi cho sức khỏe tim mạch, ngăn ngừa các bệnh về tim, động mạch vành.
Phát biểu nào sau đây không đúng?
A. Trong phân tử linoleic acid có 2 liên kết π.
B. Công thức của chất béo trilinolein là (C17H31COO)3C3H5.
C. Linoleic acid thuộc loại omega-6.
D. Ở điều kiện thích hợp, 1 mol trilinolein tác dụng được tối đa với 6 mol H2.
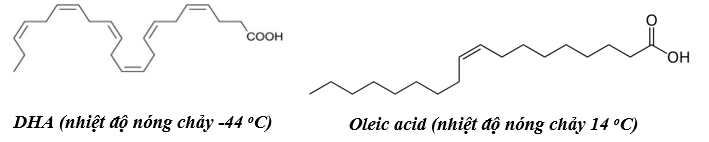
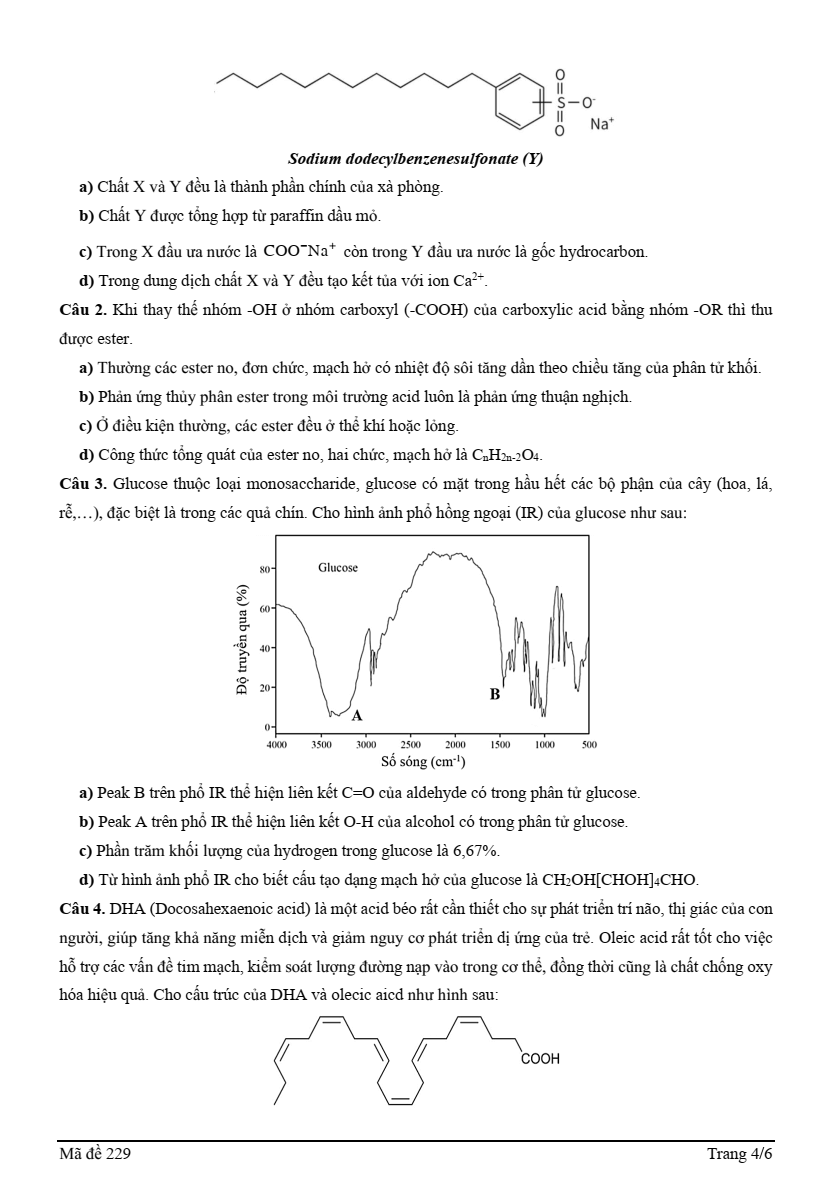
Câu 5. DHA (Docosahexaenoic acid) là một acid béo rất cần thiết cho sự phát triển trí não, thị giác của con người, giúp tăng khả năng miễn dịch và giảm nguy cơ phát triển dị ứng của trẻ. Oleic acid rất tốt cho việc hỗ trợ các vấn đề tim mạch, kiểm soát lượng đường nạp vào trong cơ thể, đồng thời cũng là chất chống oxy hóa hiệu quả. Cho cấu trúc của DHA và olecic aicd như hình sau:
Chọn phát biểu đúng.
A. DHA có nhiệt độ nóng chảy thấp hơn oleic acid do có tương tác van der Waals yếu hơn.
B. DHA thuộc nhóm acid béo omega-3, oleic acid thuộc nhóm acid béo omega-6.
C. Phần trăm khối lượng nguyên tố carbon trong oleic acid là 80,49%.
D. Phân tử DHA có cấu hình trúc dạng trans, oleic acid có trúc dạng cis.
Đề Tốt nghiệp THPT Hóa học 2026 theo form mới
(trắc nghiệm đúng sai, trả lời ngắn)
PHẦN I. CÂU TRẮC NGHIỆM NHIỀU PHƯƠNG ÁN LỰA CHỌN. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Trong nọc ong hoặc trong dịch đốt của kiến có chứa hợp chất với công thức là HCOOH. Chất này gây cảm giác đau, rát khi bị ong, kiến đốt. Khi bị ong đốt, chất nào sau đây có thể được sử dụng để bôi vào vết đốt nhằm làm giảm triệu chứng đau, rát trước khi đến cơ sở y tế?
A. Vôi tôi.
B. Nước muối.
C. Nước chanh.
D. Cồn y tế.
Câu 2. Phát biểu nào sau đây là không đúng về hiện tượng phú dưỡng?
A. Sự tích tụ bùn từ xác tảo ngăn cản oxygen khuếch tán vào nước.
B. Sự phát triển dày đặc của tảo xanh trong nước tới mức có thể quan sát được.
C. Lượng oxygen trong nước sẽ nhanh chóng giảm đi.
D. Sự tích tụ lượng lớn các chất dinh dưỡng chứa nitrogen và phosphorus.
Câu 3. Phát biểu nào sau đây là không đúng?
A. Khi thay thế nguyên tử hydrogen trong phân tử hydrocarbon bằng nguyên tử halogen thu được dẫn xuất halogen.
B. Alcohol là hợp chất hữu cơ, phân tử có nhóm hydroxy (–OH) liên kết trực tiếp với nguyên tử carbon no.
C. Trong phân tử phenol, nhóm hydroxy (–OH) liên kết trực tiếp với nguyên tử carbon của vòng benzene.
D. Khi thay thế nguyên tử hydrogen trong phân tử hydrocarbon bằng nhóm hydroxy (–OH) thu được hợp chất alcohol.
Câu 4. Khi thuỷ phân carbohydrate nào sau đây chỉ thu được glucose?
A. Saccharose.
B. Cellulose.
C. Fructose.
D. Lactose.
Câu 5. Phát biểu nào sau đây là đúng khi nói về phương pháp tách kim loại ra khỏi hợp chất của chúng?
A. Kim loại Cu được tách ra khỏi tinh thể CuSO4 nhờ phản ứng với kim loại Fe.
B. Kim loại Zn được tách ra khỏi ZnO bằng phương pháp nhiệt luyện.
C. Kim loại Mg được tách ra khỏi dung dịch MgCl2 bằng phương pháp điện phân.
D. Kim loại A1 được tách ra khỏi Al2O3 bởi CO bằng phương pháp nhiệt luyện.
Câu 6. Khi sử dụng bếp than, cần lưu ý thông gió tốt để tránh bị ngộ độc khí CO. Phản ứng cháy của than xảy ra theo phương trình hoá học sau:
Có bao nhiêu phát biểu dưới đây là đúng về biện pháp làm giảm nguy cơ ngộ độc khí CO?
(a) Tăng cường thông gió khu vực bếp.
(b) Sử dụng bếp than có ống khói.
(c) Sử dụng bếp than có quạt thổi không khí vào lò.
(d) Giảm lượng than sử dụng.
A. 1.
B. 2.
C. 3.
D. 4.
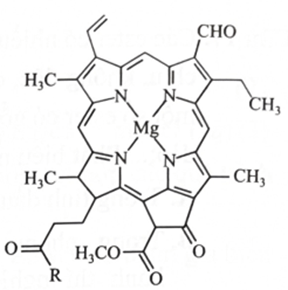
Câu 7. Chlorophyll là phức chất tạo màu xanh cho lá cây, có cấu tạo như hình bên. Số liên kết quanh nguyên tử trung tâm và số phối tử trong chlorophyll lần lượt là
A. 6 và 6.
B. 4 và 4.
C. 4 và 1.
D. 6 và 4.
Câu 8. Ion nào sau đây có cấu hình electron không giống nguyên tử neon (Ne)?
A. Na+.
B. Mg2+.
C. Al3+.
D. Cl-.
Câu 9. Khi cho từ từ dung dịch HCl đặc vào ống nghiệm chứa dung dịch copper(II) sulfate loãng. Hiện tượng xảy ra là gì?
A. Màu xanh của dung dịch trong ống nghiệm nhạt dần và chuyển sang màu vàng.
B. Màu xanh của dung dịch trong ống nghiệm biến mất, sau đó màu vàng xuất hiện.
C. Màu vàng của dung dịch trong ống nghiệm nhạt dần, sau đó chuyển sang màu xanh.
D. Tạo thành dung dịch không màu.
Câu 10. Sắp xếp theo chiều tăng dần độ cứng của một số kim loại kiềm.
A. Cs < Rb < Na < Li.
B. Rb < Cs < K < Li.
C. Li < Na < K < Rb.
D. Cs < Na < K < Li.
Câu 11. Một số ester đơn chức mạch hở, đồng phân cấu tạo của nhau, phân tử có phần trăm khối lượng các nguyên tố C, H, O lần lượt là 54,54%; 9,10% và 36,36%. Phát biểu nào sau đây về các ester trên là không đúng?
A. Có 4 ester đồng phân cấu tạo của nhau.
B. Công thức phân tử của các ester này là C2H4O2.
C. Có ít nhất 1 ester tác dụng được với nước bromine.
D. Trong các đồng phân ester trên, có đồng phân X thoả mãn sơ đồ phản ứng:
Câu 12. Một số amine đồng phân cấu tạo của nhau có công thức phân tử C4H11N. Phát biểu nào sau đây là không đúng về các amine đồng phân này?
A. Có 4 đồng phân cấu tạo tác dụng với acid HNO2 sinh ra khí nitrogen.
B. Có 1 đồng phân amine bậc ba.
C. Có 2 đồng phân amine bậc hai.
D. Dung dịch của các đồng phân đều tạo được màu xanh tím với dung dịch Cu(OH)2 trong môi trường kiềm.
Câu 13. Nguyên tố nào dưới đây không phải là nguyên tố chuyển tiếp dãy thứ nhất?
A. Mn.
B. Zn.
C. Cu.
D. V.
Câu 14. Acetic acid là một acid yếu, ở 25°C, hằng số cân bằng của acid này là 1,75.10-5. Giá trị pH của dung dịch CH3COOH 0,1 M gần nhất với giá trị pH của
A. nước mưa bình thường.
B. đất kiềm.
C. dịch vị dạ dày.
D. nước muối.
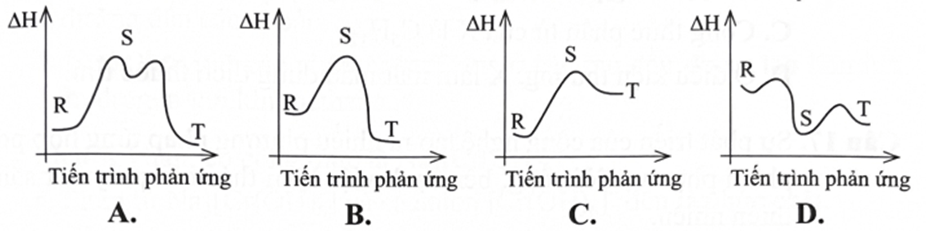
Câu 15. Phản ứng chuyển từ chất R thành chất T có giá trị biến thiên enthalpy âm và đi qua giai đoạn tạo chất trung gian S duy nhất như sau:
R → S DH > 0; S→T DH<0
Tiến trình phản ứng trên được minh hoạ theo sơ đồ nào dưới đây ?
Câu 16. Polymer dùng chế tạo thuỷ tinh hữu cơ được điều chế từ monomer nào sau đây?
A. Methyl acrylate.
B. Methyl methacrylate.
C. Methacrylic acid.
D. Vinyl acetate.
Câu 17. Phát biểu nào sau đây là đúng?
A. Mỗi nguyên tố kim loại chuyển tiếp dãy thứ nhất chỉ tạo một loại phức chất đặc trưng.
B. Trong phức chất bát diện, mỗi nguyên tử trung tâm liên kết với 8 phối tử.
C. Xung quanh nguyên tử trung tâm trong phức chất vuông phẳng có 4 liên kết σ.
D. Phức chất mà xung quanh nguyên tử trung tâm có 4 liên kết σ gọi là phức chất tứ diện.
Câu 18. Cho các loại tơ sau: (1) tơ tằm; (2) bông; (3) len; (4) tơ capron; (5) tơ visco; (6) tơ nylon-6,6; (7) tơ cellulose acetate. Những loại tơ có nguồn gốc cellulose là
A. (2), (5) và (7).
B. (1), (2) và (3).
C. (4), (6) và (7).
D. (1), (6) và (7).
PHẦN II. CÂU TRẮC NGHIỆM ĐÚNG SAI. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
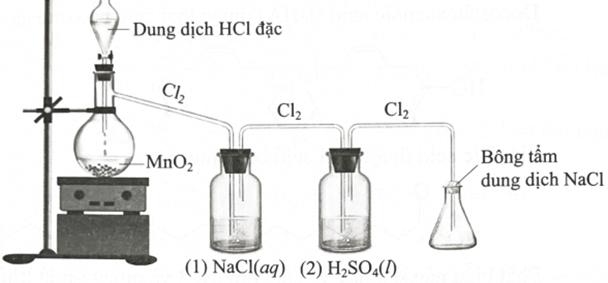
Câu 1. Để điều chế một lượng nhỏ khí chlorine trong phòng thí nghiệm, người ta cho dung dịch HCl đặc phản ứng với MnO2 rắn theo sơ đồ thí nghiệm như hình dưới đây, trong đó bình (1) chứa NaCl(aq) giúp giữ khí HCl, bình (2) chứa H2SO4 (l) đặc giúp hút ẩm, làm khô khí, bảo đảm chất lượng chlorine.
a. Dung dịch HCl đặc đóng vai trò là chất oxi hoá trong phản ứng điều chế chlorine.
b. Bông tẩm dung dịch NaOH giúp ngăn khí chlorine rò rỉ ra ngoài.
c. Khi thay MnO2 bằng KMnO4 cùng khối lượng, lượng Cl2 thu được sẽ nhiều hơn, biết HCl đặc dùng dư. Cho phương trình hoá học của phản ứng giữa KMnO4 và HCl là:
d. Nếu hoán đổi vị trí bình (1) và bình (2), chất lượng khí chlorine thu được sẽ không đổi.
Câu 2. Gói làm nóng thức ăn trong lẩu tự sôi có thành phần theo khối lượng là Mg (90%), Fe (4%), NaCl (6%). Khi thêm vào một ít nước, phản ứng hoá học Mg + 2H2O → Mg(OH)2 + H2 xảy ra mãnh liệt kèm theo lượng nhiệt toả ra lớn, giúp làm nóng thức ăn.
a. Magnesium có thể khử được nước ở nhiệt độ thường.
b. Có thể dùng bột chứa 100% Mg để tăng hiệu quả làm nóng thức ăn.
c. Nếu thêm nước quá nhiều, khả năng làm nóng thức ăn của hỗn hợp giảm.
d. Khi thay NaCl bằng AgCl, khả năng làm nóng của hỗn hợp không đổi.
Câu 3. Trong thành phần của một loại phèn sắt có muối Fe2(SO4)3 và một loại phèn nhôm có muối Al2(SO4)3. Kí hiệu chung của hai muối sulfate trên là M2(SO4)3. Khi hoà tan hoàn toàn phèn sắt hoặc phèn nhôm vào nước có một số quá trình quan trọng sau:
a. Sự thuỷ phân của M2(SO4)3 được giải thích nhờ kết hợp các quá trình (1), (2) và (3).
b. Trong nước, M3+ là một base theo Brønsted – Lowry do tham gia biến đổi ở quá trình (2) và (3).
c. Phức chất không tan, sinh ra ở quá trình (3), ứng với m = 2, là tác nhân để kết dính các hạt lơ lửng trong nước bị đục.
d. Sau khi dùng phèn để làm trong nước thì pH của nước sẽ giảm so với ban đầu.
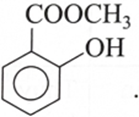
Câu 4. Salicylic acid (2-hydroxybenzoic acid) phản ứng với alcohol X (có sulfuric acid làm xúc tác), thu được chất Y (công thức C8H8O3, phân tử có nhóm chức ester) dùng làm thuốc giảm đau. Mỗi phát biểu sau là đúng hay sai?
a. X là ethyl alcohol.
b. Công thức cấu tạo của Y là
c. X là chất đơn chức, Y là chất đa chức.
d. 1 mol chất Y phản ứng tối đa với 2 mol NaOH (trong dung dịch).
PHẦN III. CÂU TRẮC NGHIỆM TRẢ LỜI NGẮN. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. NO là một chất khí độc, có thể bị loại bỏ nhờ phản ứng sau đây:
2H2(g) + 2NO(g) → 2H2O(g) + N2(g)
Tốc độ của phản ứng này có dạng v = .
Giữ nguyên nhiệt độ, để tăng tốc độ loại bỏ NO, người ta tăng gấp 2 nồng độ H2, hỏi tốc độ phản ứng loại bỏ NO tăng lên bao nhiêu lần?
Câu 2. Một mẫu nước cứng có nồng độ các ion như sau: ; . Để làm mềm 10L nước này cần dùng tối thiểu bao nhiêu gam sodium carbonate? Kết quả được làm tròn đến hàng phần trăm.
Câu 3. Trong quá trình quang hợp, cây xanh sử dụng năng lượng ánh sáng để tổng hợp glucose từ khí CO2 và nước. Biến thiên enthalpy của phản ứng quang hợp này là 673 kJ cho 1 mol glucose. Tính năng lượng ánh sáng (kJ) cần có để tạo ra 36 g đường glucose, biết hiệu suất của quá trình quang hợp của loại cây này là 20%.
Câu 4. Cho các chất: glucose (C6H12O6), fructose (C6H12O6), maltose (C12H22O11), saccharose (C12H22O11). Có bao nhiêu chất phản ứng được với thuốc thử Tollens sinh ra bạc?
Câu 5. Chuẩn độ hàm lượng ion Fe2+ trong môi trường acid (chứa trong bình tam giác) bằng dung dịch KMnO4 đã biết nồng độ (chứa trên burette). Trong quá trình chuẩn độ, nếu dung dịch trên burette được thêm vào bình tam giác quá nhanh thì trong bình sẽ xuất hiện kết tủa nâu MnO2 theo phương trình hoá học dưới đây, dẫn đến sai lệch kết quả chuẩn độ:
Giả sử một học sinh thao tác sai, làm 60% lượng chuẩn độ chuyển thành MnO2 (phần còn lại vẫn phản ứng tạo Mn+), tổng lượng Fe2+ bị oxi hoá là 2,2 mmol. Thể tích dung dịch KMnO4 0,020 M đã dùng tăng bao nhiêu mL so với khi chuẩn độ với thao tác phù hợp?
Câu 6. Trong các chất: phân bón ammonium sulfate, muối ăn, đá vôi, vôi sống, vôi tôi, soda, baking soda, phèn nhôm, phèn sắt có bao nhiêu chất có thể được dùng để làm tăng pH của đất?
Đề thi thử Hóa Tốt nghiệp THPT năm 2025 Trường THCS-THPT Nguyễn Khuyến
Đề thi thử Tốt nghiệp THPT Hóa 2025 Sở GD&ĐT Ninh Bình
................................
................................
................................
Xem thử Đề thi Tốt nghiệp THPT Hóa 2025 Xem thử Đề thi thử Tốt nghiệp THPT Hóa 2025 Xem thử Chuyên đề ôn thi Tốt nghiệp THPT Hóa Xem thử 1000 câu trắc nghiệm Hóa
Xem thêm đề ôn thi Tốt nghiệp THPT các môn học:
Xem thêm đề thi thử Tốt nghiệp THPT các môn học:
Tài liệu ôn thi Tốt nghiệp THPT các môn học:
- 8 Chuyên đề Toán ôn thi Tốt nghiệp THPT 2026
- 11 Chuyên đề toán thực tế lớp 12
- 14 Chuyên đề ôn thi Tốt nghiệp THPT Vật Lí 2026
- 1000 câu trắc nghiệm lý thuyết Vật Lí ôn thi Tốt nghiệp THPT 2026
- 10 Chuyên đề ôn thi Tốt nghiệp THPT Sinh học 2026
- 1200 câu trắc nghiệm lý thuyết Sinh học ôn thi Tốt nghiệp THPT 2026
- Chuyên đề Địa Lí ôn thi Tốt nghiệp THPT 2026
- Trọng tâm Địa Lí 12 ôn thi tốt nghiệp
- Chuyên đề KTPL ôn thi Tốt nghiệp THPT 2026
- Kiến thức trọng tâm KTPL 12
- Chuyên đề Lịch Sử ôn thi Tốt nghiệp THPT 2026
- Chuyên đề Ngữ văn ôn thi Tốt nghiệp THPT 2026
- Ngữ liệu ngoài sgk lớp 12 phần Thơ
- Ngữ liệu ngoài sgk lớp 12 phần Truyện
- 21 Chuyên đề ôn thi Tốt nghiệp THPT Hóa 2025
- 1000 câu trắc nghiệm lý thuyết Hóa thi Tốt nghiệp THPT 2026
- 15 Chuyên đề ôn thi Tiếng Anh Tốt nghiệp THPT 2026
Xem thêm đề ôn thi Đánh giá năng lực, Đánh giá tư duy các trường:
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Lớp 12 Kết nối tri thức
- Soạn văn 12 (hay nhất) - KNTT
- Soạn văn 12 (ngắn nhất) - KNTT
- Giải sgk Toán 12 - KNTT
- Giải sgk Vật Lí 12 - KNTT
- Giải sgk Hóa học 12 - KNTT
- Giải sgk Sinh học 12 - KNTT
- Giải sgk Lịch Sử 12 - KNTT
- Giải sgk Địa Lí 12 - KNTT
- Giải sgk Giáo dục KTPL 12 - KNTT
- Giải sgk Tin học 12 - KNTT
- Giải sgk Công nghệ 12 - KNTT
- Giải sgk Hoạt động trải nghiệm 12 - KNTT
- Giải sgk Giáo dục quốc phòng 12 - KNTT
- Giải sgk Âm nhạc 12 - KNTT
- Giải sgk Mĩ thuật 12 - KNTT
- Lớp 12 Chân trời sáng tạo
- Soạn văn 12 (hay nhất) - CTST
- Soạn văn 12 (ngắn nhất) - CTST
- Giải sgk Toán 12 - CTST
- Giải sgk Vật Lí 12 - CTST
- Giải sgk Hóa học 12 - CTST
- Giải sgk Sinh học 12 - CTST
- Giải sgk Lịch Sử 12 - CTST
- Giải sgk Địa Lí 12 - CTST
- Giải sgk Giáo dục KTPL 12 - CTST
- Giải sgk Tin học 12 - CTST
- Giải sgk Hoạt động trải nghiệm 12 - CTST
- Giải sgk Âm nhạc 12 - CTST
- Lớp 12 Cánh diều
- Soạn văn 12 Cánh diều (hay nhất)
- Soạn văn 12 Cánh diều (ngắn nhất)
- Giải sgk Toán 12 Cánh diều
- Giải sgk Vật Lí 12 - Cánh diều
- Giải sgk Hóa học 12 - Cánh diều
- Giải sgk Sinh học 12 - Cánh diều
- Giải sgk Lịch Sử 12 - Cánh diều
- Giải sgk Địa Lí 12 - Cánh diều
- Giải sgk Giáo dục KTPL 12 - Cánh diều
- Giải sgk Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 - Cánh diều
- Giải sgk Giáo dục quốc phòng 12 - Cánh diều
- Giải sgk Âm nhạc 12 - Cánh diều










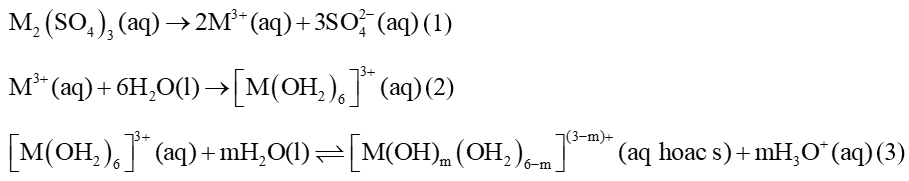















 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

