Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 6 (có lời giải)
Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 6: Đại cương về kim loại có đáp án chi tiết đầy đủ các mức độ sẽ giúp học sinh lớp 12 ôn luyện Hóa học 12.
Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 6 (có lời giải)
Chỉ từ 200k mua trọn bộ Bài tập ôn tập + Đề kiểm tra Hóa học 12 Kết nối tri thức theo chương theo cấu trúc mới bản word có lời giải chi tiết, trình bày đẹp mắt, dễ dàng chỉnh sửa:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận đề thi
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Mỗi câu hỏi học sinh chỉ chọn một phương án.
Câu 1. Những tính chất vật lí chung của kim loại (dẫn điện, dẫn nhiệt, dẻo, ánh kim) gây nên chủ yếu bởi
A. khối lượng riêng.
B. các electron tự do trong tinh thể kim loại.
C. tính chất của kim loại.
D. kiểu cấu tạo mạng tinh thể của kim loại.
Câu 2. Trong tinh thể kim loại, liên kết kim loại được hình thành do
A. lực hút tĩnh điện giữa các electron hoá trị ở các nút mạng với các ion dương kim loại chuyển động tự do.
B. sự góp chung electron của các nguyên tử kim loại cạnh nhau.
C. lực hút tĩnh điện giữa các electron hoá trị tự do với các ion dương kim loại chuyển động tự do trong toàn bộ mạng tinh thể.
D. lực hút tĩnh điện giữa các electron hoá trị tự do với các ion dương kim loại ở các nút mạng.
Câu 3. Đồng là một kim loại dẫn điện tốt (chỉ xếp sau bạc), tuy nhiên các dây điện cao thế không được làm bằng đồng mà thường được làm bằng kim loại nào sau đây?
A. Iron.
B. Sodium.
C. Aluminium.
D. Gold.
Câu 4. Nhóm những kim loại có độ dẫn điện tốt nhất là
A. Fe, Cu, Zn.
B. Cu, Al, Hg.
C. Ag, Cu, Au.
D. Li, Na, K.
Câu 5. Kim loại nào sau đây không phản ứng với dung dịch HCl loãng?
A. Cu.
B. Pb.
C. Zn.
D. Fe.
Câu 6. Cho các phát biểu sau đây về vị trí và cấu tạo của kim loại:
(1) Ở trạng thái rắn, đơn chất kim loại có cấu tạo tinh thể.
(2) Tất các các nguyên tố phân nhóm B (phân nhóm phụ) đều là kim loại.
(3) Hầu hết các kim loại chỉ có từ 1 electron đến 3 electron lớp ngoài cùng.
(4) Các kim loại đều có bán kính nhỏ hơn các phi kim thuộc cùng một chu kì.
(5) Liên kết kim loại là liên kết được hình thành giữa các nguyên tử và ion dương kim loại trong mạng tinh thể do sự tham gia của các electron tự do.
Những phát biểu đúng là
Α. (1), (2), (3), (5).
Β. (1), (2), (3), (4), (5).
C. (1), (2), (3).
D. (1), (3), (5).
Câu 7. Nhờ có hàm lượng lớn trong vỏ Trái Đất nên có một số kim loại được sử dụng làm kim loại cơ bản trong các hợp kim, đó là
A. Fe, Zn, Ca.
B. Al, Mg, Na.
C. Fe, Al, Mg.
D. Fe, Al, Sn.
Câu 8. Kim loại X được sử dụng trong nhiệt kế, áp kế và một số thiết bị khác. Ở điều kiện thường, X là chất lỏng. Kim loại X là
A. Chromium.
B. Lead.
C. Tungsten.
D. Mercury.
Câu 9. Zinc (kẽm) khử được các cation kim loại trong dãy muối nào sau đây?
A. Cu(NO3)2, Pb(NO3)2, Ni(NO3)2.
B. AlCl3, MgCl2, PbSO4.
C. AlCl3, Ni(NO3)2, PbCl2.
D. MgCl2, NaCl, Cu(NO3)2.
Câu 10. Ở điều kiện chuẩn, những kim loại tan trong hydrochloric acid hoặc sulfuric acid loãng thường có thế điện cực chuẩn
A. nhỏ hơn 0 V.
B. lớn hơn 0 V.
C. lớn hơn -0,413 V.
C. nhỏ hơn -0,413 V.
Câu 11. Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường tạo thành dung dịch có môi trường kiềm là
A. Na, Cr, K.
B. Na, Ba, K.
C. Be, Na, Ca.
D. Na, Fe, K.
Câu 12. Phương pháp thích hợp để điều chế Mg từ MgCl2 là
A. điện phân dung dịch .
B. dùng kali khử ion trong dung dịch.
C. điện phân nóng chảy.
D. nhiệt phân .
Câu 13. X là kim loại phản ứng được với dung dịch H2SO4 loãng, Y là kim loại tác dụng được với dung dịch Fe(NO3)3. Hai kim loại X, Y lần lượt có thể là
A. Mg, Ag.
B. Ag, Mg.
C. Fe, Cu.
D. Cu, Fe.
Câu 14. Đồng thau là hợp kim chứa khoảng 70% đồng và 30% kẽm. Ứng dụng nào sau đây không phải là ứng dụng của đồng thau?
A. Làm nhạc cụ.
B. Làm dụng cụ nấu ăn.
C. Làm thiết bị dẫn điện.
D. Làm thân vỏ máy bay.
Câu 15. Thí nghiệm nào sau đây không sinh ra đơn chất?
A. Cho kim loại Mg vào dung dịch HCl.
B. Cho kim loại Zn vào dung dịch CuSO4.
C. Cho MgCO3 vào dung dịch HCl.
D. Cho kim loại Cu vào dung dịch AgNO3.
Câu 16. Lần lượt nối thanh Zn với mỗi kim loại sau đây và cho vào dung dịch HCl. Quá trình ăn mòn thanh Zn xảy ra nhanh nhất khi nối với
A. Mg.
B. Pb.
C. Ag.
D. Cu.
Câu 17. Cho khí CO (dư) đi qua ống sứ nung nóng đựng hỗn hợp X gồm Al2O3, MgO, Fe3O4 và CuO, thu được chất rắn Y. Cho Y vào dung dịch NaOH dư, khuấy kĩ, thấy còn lại phần không tan Z. Giả sử các phản ứng xảy ra hoàn toàn. Phần không tan Z gồm
A. Mg, Fe, Cu.
B. Mg, Al, Fe, Cu.
C. MgO, Fe, Cu.
D. MgO, Fe3O4, Cu.
Câu 18. Cho ba kim loại được tách từ quặng của chúng theo các cách tương ứng sau
|
Kim loại |
Phương pháp tách thông dụng |
|
X |
Điện phân nóng chảy |
|
Y |
Nhiệt phân, nung nóng trực tiếp |
|
Z |
Nung nóng với carbon |
Khả năng hoạt động hóa học của các kim loại giảm dần theo thứ tự nào sau đây?
A. Z, Y, X.
B. X, Y, Z.
C. X, Z, Y.
D. Y, Z, X.
PHẦN II. Câu trắc nghiệm đúng sai. Trong mỗi ý a), b), c), d) ở mỗi câu, học sinh chọn đúng hoặc sai.
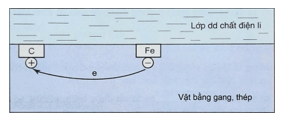
Câu 19. Trong không khí ẩm, trên bề mặt của gang, thép luôn có một lớp nước rất mỏng. Lớp nước này hoà tan khí oxygen và carbon dioxide trong khí quyển, tạo thành dung dịch chất điện li. Gang, thép có thành phần chính là sắt và carbon cùng tiếp xúc với dung dịch chất điện li tạo nên vô số pin rất nhỏ mà sắt là anode và carbon là cathode.
a. Carbon bị khử tại cathode.
b. Tại anode, Fe bị oxi hóa thành
c. Oxygen đóng vai trò là chất oxi hóa.
d. Dạng ăn mòn hóa học là chủ yếu, do sắt dễ dàng phản ứng oxygen trong không khí.
Câu 20. Xét các phát biểu sau về tách và tinh chế kim loại:
a. Trong công nghiệp, kim loại Na được điều chế bằng cách điện phân dung dịch NaCl.
b. Để tách Ag khỏi các tạp chất Fe, Cu ta có thể cho hỗn hợp vào dung dịch AgNO3 dư.
c. Trong công nghiệp, kim loại Al chỉ có thể điều chế được bằng phương pháp điện phân.
d. Các kim loại Fe, Al, Cu đều có thể điều chế bằng phương pháp dùng CO khử oxide kim loại tương ứng.
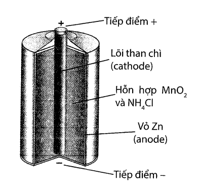
Câu 21. Năm 1866, Georges Leclanché đã phát minh ra một loại pin bao gồm anode bằng kẽm và cathode bằng mangan dioxide bọc trong một vật liệu xốp, nhúng trong lọ đựng dung dịch ammonium chloride. Cathode được trộn vào một ít carbon để cải thiện độ dẫn điện và hấp thụ điện. Pin cung cấp một điện áp khoảng 1,4 – 1,5V.
- Ở anode xảy ra bán phản ứng:
- Ở cathode xảy ra bán phản ứng:
a. Ở anode xảy ra quá trình khử kẽm trên bề mặt của anode.
b. Ở anode xảy ra quá trình nhường electron (quá trình oxi hóa).
c. Anode chứa nhiều electron nên điện tích dương hơn cathode.
d. Ở cathode xảy ra quá trình oxi hóa thành
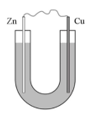
Câu 22. Thực hiện thí nghiệm sau:
Bước 1: Cho dung dịch NaCl 5% vào ống thuỷ tinh hình chữ U như hình bên.
Bước 2: Nhúng một thanh đồng và một thanh kẽm đã làm sạch vào hai đầu của ống chữ U.
Bước 3: Nối hai thanh kim loại bằng dây dẫn.
a. Sau bước 2, kim loại Zn bị ăn mòn.
b. Sau bước 3, kẽm bị ăn mòn, đồng không bị ăn mòn.
c. Sau bước 3, kẽm bị ăn mòn và đóng vai trò là cathode.
d. Khoảng vài phút sau bước 3, nhỏ vài giọt phenolphthalein vào dung dịch gần thanh đồng, thấy dung dịch dần chuyển sang màu hồng.
PHẦN III. Câu trắc nghiệm yêu cầu trả lời ngắn
Câu 23. Trong một nhà máy luyện kim, quặng sắt chứa 50% hematite (Fe2O3) được sử dụng để điều chế gang. Từ 1 tấn quặng trên có thể điều chế được bao nhiêu tấn gang (Fe chiếm 96% khối lượng)? Biết hiệu suất cả quá trình là 70%. (Kết quả làm tròn đến hàng phần trăm).
Câu 24. Một nhà máy sản xuất gang thép sản xuất được m tấn thép từ 400 tấn quặng hematite đỏ (chứa 84% Fe2O3 về khối lượng, còn lại là tạp chất không chứa sắt) theo sơ đồ:
Quặng hematite đỏ Gang trắng Thép
Biết hiệu suất cả quá trình trên đạt 91% và thép chứa 98% sắt về khối lượng. Giá trị của m bằng bao nhiêu? (Kết quả làm tròn đến hàng đơn vị).
Câu 25. Một vết nứt trên đường ray tàu hỏa có thể tích 6,72 cm3. Dùng hỗn hợp tecmite (Al và Fe2O3 theo tỉ lệ mol tương ứng 2: 1) để hàn vết nứt trên theo phản ứng:
2Al + Fe2O3 Al2O3 + 2Fe
Biết rằng: Lượng Fe cần hàn cho vết nứt bằng 79% lượng Fe sinh ra; khối lượng riêng của sắt là 7,9 gam/cm3; chỉ xảy ra phản ứng khử Fe2O3 thành Fe với hiệu suất của phản ứng bằng 96%. Khối lượng của hỗn hợp tecmite tối thiểu cần dùng là bao nhiêu gam? (Làm tròn kết quả đến hàng đơn vị).
Câu 26. Trong một nhà máy luyện kim, quặng chứa 40% cuprite (Cu2O) được sử dụng để điều chế đồng. Từ 1 tấn quặng trên có thể điều chế được bao nhiêu tấn đồng biết rằng hiệu suất của quá trình là 75%? (Kết quả làm tròn đến hàng phần trăm).
Câu 27. Một nhà máy luyện kim, ở giai đoạn đầu của quá trình sản xuất Zn từ quặng blend thu được sản phẩm phụ là SO2 theo sơ đồ phản ứng: ZnS + O2 ZnO + SO2
Đốt cháy 1 tấn quặng blend (chứa 77,6% khối lượng ZnS) bằng không khí, thu được tối đa V m3 khí SO2 (đkc). Giá trị của V là bao nhiêu? Kết quả làm tròn đến hàng đơn vị.
Câu 28. Xét các phản ứng chính xảy ra trong quá trình luyện gang trong lò cao từ nguyên liệu là quặng hematite và than cốc:
Đốt cháy than cốc để cung cấp nhiệt: C + O2 CO2
Tạo chất khử: C + CO2 2CO
Khử iron(III) oxide trong quặng thành sắt: Fe2O3 + 3CO 2Fe + 3CO2.
Giả thiết gang chứa 95% sắt và 5% carbon (từ than cốc), còn than cốc chỉ chứa carbon. Để sản xuất 1000 kg gang cần m kg than cốc với hiệu suất cả quá trình là 80%. Giá trị của m bằng bao nhiêu? (Làm tròn kết quả đến hàng đơn vị).
................................
................................
................................
Xem thêm đề kiểm tra Hóa học lớp 12 Kết nối tri thức có đáp án hay khác:
Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 1 (có lời giải)
Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 2 (có lời giải)
Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 3 (có lời giải)
Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 4 (có lời giải)
Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 5 (có lời giải)
Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 7 (có lời giải)
Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 8 (có lời giải)
Xem thêm các tài liệu học tốt lớp 12 hay khác:
- Giải sgk Hóa học 12 Kết nối tri thức
- Giải Chuyên đề học tập Hóa 12 Kết nối tri thức
- Giải SBT Hóa học 12 Kết nối tri thức
- Giải lớp 12 Kết nối tri thức (các môn học)
- Giải lớp 12 Chân trời sáng tạo (các môn học)
- Giải lớp 12 Cánh diều (các môn học)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Soạn văn 12 (hay nhất) - KNTT
- Soạn văn 12 (ngắn nhất) - KNTT
- Giải sgk Toán 12 - KNTT
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Giải sgk Vật Lí 12 - KNTT
- Giải sgk Hóa học 12 - KNTT
- Giải sgk Sinh học 12 - KNTT
- Giải sgk Lịch Sử 12 - KNTT
- Giải sgk Địa Lí 12 - KNTT
- Giải sgk Giáo dục KTPL 12 - KNTT
- Giải sgk Tin học 12 - KNTT
- Giải sgk Công nghệ 12 - KNTT
- Giải sgk Hoạt động trải nghiệm 12 - KNTT
- Giải sgk Giáo dục quốc phòng 12 - KNTT
- Giải sgk Âm nhạc 12 - KNTT
- Giải sgk Mĩ thuật 12 - KNTT



















 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

