Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 8 (có lời giải)
Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 8: Sơ lược về dãy kim loại chuyển tiếp thứ nhất và phức chất có đáp án chi tiết đầy đủ các mức độ sẽ giúp học sinh lớp 12 ôn luyện Hóa học 12.
Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 8 (có lời giải)
Chỉ từ 200k mua trọn bộ Bài tập ôn tập + Đề kiểm tra Hóa học 12 Kết nối tri thức theo chương theo cấu trúc mới bản word có lời giải chi tiết, trình bày đẹp mắt, dễ dàng chỉnh sửa:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận đề thi
Phần 1. Trắc nghiệm nhiều phương án lựa chọn
Câu 1. Kim loại chuyển tiếp dãy thứ nhất thuộc khối nguyên tố nào sau đây?
A. Nguyên tố s.
B. Nguyên tố p.
C. Nguyên tố d.
D. Nguyên tố f.
Câu 2. Dãy nào sau đây có tất cả các nguyên tố đều là kim loại chuyển tiếp dãy thứ nhất?
A. Chromium, copper, nickel, zinc.
B. Iron, cobalt, manganese, bromine.
C. Manganese, iron, copper, beryllium.
D. Chromium, titanium, vanadium, scandium.
Câu 3. Cấu hình electron của nguyên tử Cu ở trạng thái cơ bản là . Cấu hình electron của ion là
A.
B.
C.
D.
Câu 4. Muối nào sau đây vừa có khả năng thể hiện tính khử (trong môi trường kiềm), vừa thể hiện tính oxi hóa (trong môi trường acid)?
A.
B.
C.
D.
Câu 5. Ở trạng thái cơ bản, cấu hình electron của là Số oxi hoá cao nhất của Mn trong các hợp chất là
A. +5.
B. +7.
C. +2.
D. +6.
Câu 6. Trong phân tử phức chất Fe3+ được gọi là
A. phối tử.
B. base.
C. chất khử.
D. nguyên tử trung tâm.
Câu 7. Nhận xét nào sau đây là không đúng về cấu tạo của phức chất?
A. Nguyên tử trung tâm chỉ có thể là cation kim loại.
B. Thành phần của phức chất có nguyên tử trung tâm và phối tử.
C. Phối tử còn cặp electron chưa liên kết, có khả năng cho nguyên tử trung tâm.
D. Liên kết giữa phối tử và nguyên tử trung tâm là liên kết cho – nhận.
Câu 8. Phức chất nào sau đây có dạng hình học không phải tứ diện?
A.
B.
C.
D.
Câu 9. Số oxi hoá của nguyên tử trung tâm trong phức chất là
A. +3.
B. +6.
C. +2.
D. +4.
Câu 10. Trong dung dịch tồn tại cân bằng:
(da cam) + (vàng) +
Khi nhỏ vài giọt dung dịch chất vô cơ X vào dung dịch thì dung dịch chuyển dần từ màu da cam sang màu vàng. Vậy chất nào dưới đây phù hợp với X?
A. NaOH.
B. NaCl.
C.
D.
Câu 11. Điện tích của nguyên tử trung tâm trong phức chất và lần lượt là
A. +3 và −3.
B. +6 và −6.
C. +3 và +2.
D. +3 và +3.
Câu 12. Phản ứng chuẩn độ trong dung dịch acid bằng dung dịch được biểu diễn bởi phương trình ion rút gọn sau:
Chất oxi hoá trong phản ứng trên là
A.
B.
C.
D.
Câu 13. Phát biểu nào sau đây không đúng?
A. Phức chất aqua của các ion kim loại chuyển tiếp hầu hết có dạng hình học bát diện.
B. Các phối tử H2O trong phức chất aqua không thể bị thế bởi các phối tử khác.
C. Trong dung dịch, các ion kim loại chuyển tiếp đều tạo phức chất aqua.
D. Các phối tử trong phức chất có thể bị thay thế một phần hoặc thay thế hoàn toàn bởi các phối tử khác.
Câu 14. Trong dung dịch nước, ion tồn tại ở dưới dạng phức chất bát diện Số liên kết sigma có trong phức chất là
A. 6.
B. 12.
C. 18.
D. 16.
Câu 15. Cho các nhận định sau:
(1) Cầu nội của phức chất có thể mang điện tích dương, âm hoặc không.
(2) Cation Ni2+ chỉ có thể tạo phức chất bát diện.
(3) Phức chất có các dạng hình học phổ biến là tứ diện, vuông phẳng và bát diện.
(4) Nguyên tử trung tâm là các nguyên tố nhóm B.
(5) Phối tử chỉ có thể là anion hoặc phân tử trung hoà.
(6) Cầu ngoại của phức chất thường mang điện tích âm.
(7) Kiểu lai hoá của nguyên tử trung tâm sẽ quyết định dạng hình học của phức chất.
(8) Trong phức chất bát diện, các phối tử chiếm vị trí 6 đỉnh, còn nguyên tử trung tâm nằm ở tâm của hình bát diện.
Số nhận định sai là
A. 2.
B. 3.
C. 4.
D. 5.
Câu 16. Cho các phản ứng sau:
Số phản ứng xảy ra sự thay thế phối tử trong phức chất là
A. 3.
B. 2.
C. 4.
D. 5.
Câu 17. Nước ngầm nhiễm sắt là nước chứa hàm lượng sắt hoà tan dưới dạng cao vượt quá mức cho phép (), gây ra hiện tượng nước có mùi tanh, vị chua, đục và sẫm màu. Một mẫu nước giếng khoan ô nhiễm sắt ở dạng với nồng độ là Nồng độ mol của trong nước giếng khoan là bao nhiêu? (Cho biết: )
A.
B.
C.
D.
Câu 18. Phát biểu nào sau đây về phức chất bát diện [Cu(OH2)6]2+ là sai?
A. Mỗi phân tử nước sử dụng cả 2 cặp electron hoá trị riêng của nó để tạo liên kết cho – nhận với cation Cu2+.
B. Số oxi hoá của nguyên tử trung tâm là +2.
C. Thêm vài giọt dung dịch ammonia vào dung dịch phức thấy xuất hiện kết tủa màu xanh nhạt.
D. Nguyên tử trung tâm được hình thành từ quá trình cation Cu2+ sử dụng 6 orbital trống để nhận các cặp electron hoá trị riêng của các phân tử H2O.
Phần 2. Trắc nghiệm đúng sai. Trong mỗi ý a, b, c, d ở mỗi câu, học sinh chọn đúng hoặc sai.
Câu 19. Thực hiện hai thí nghiệm liên tiếp:
Thí nghiệm 1: Nhỏ từ từ dung dịch NaCl vào ống nghiệm đựng dung dịch .
Thí nghiệm 2: Sau đó nhỏ thêm dung dịch đến dư vào ống nghiệm.
a. Phức chất được tạo thành ở thí nghiệm (2) chứa 2 phối tử và 2 phối tử
b. Dấu hiệu nhận biết phức chất tạo thành là kết tủa tan.
c. Phức chất AgCl kết tủa trắng được tạo thành ở thí nghiệm (1).
d. Phức chất không màu được tạo thành ở thí nghiệm (2).
Câu 20. Khi hoà tan một lượng phèn nhôm – kali vào nước thì có các quá trình cơ bản sau:
(1)
(2)
a. Quá trình (1) là quá trình tạo phức chất aqua của cation Al3+.
b. Ở quá trình (2), các phân tử nước đóng vai trò là dung môi.
c. Các quá trình (1) và (2) giúp giải thích vì sao cation Al3+ là một base trong dung dịch nước theo Brönsted - Lowry.
d. Để thu được nhiều kết tủa keo thì cần hoà tan lượng nhỏ phèn trong lượng lớn nước.
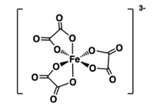
Câu 21. Phức chất X có công thức cấu tạo như hình bên dưới.
a. Số oxi hoá của nguyên tử trung tâm trong phức chất X là +2.
b. Công thức của phức chất X là
c. Phức chất X thuộc loại phức bát diện.
d. Trong phức chất X, nguyên tử trung tâm iron liên kết với 6 phối tử oxalato
Câu 22. Chuẩn độ dung dịch chứa muối nồng độ và dung dịch loãng, đựng trong bình tam giác bằng dung dịch nồng độ để ở burette và để ở vạch 0. Khi vạch thể tích dung dịch trên burette là thì trong bình tam giác xuất hiện màu hồng bền trong khoảng 20 giây.
a. Phản ứng chuẩn độ là:
b. Khi màu hồng trong bình tam giác bền trong khoảng 20 giây thì có thể coi như phản ứng vừa đủ.
c. Mối quan hệ giữa và được biểu diễn qua biểu thức:
d. Có thể thực hiện phép chuẩn độ trên bằng cách đựng dung dịch ở bình tam giác và dung dịch chứa trong môi trường acid ở burette cho kết quả tương tự.
Phần 3. Trắc nghiệm yêu cầu trả lời ngắn
Câu 23. Cấu hình electron của sắt (Fe) là Xác định số electron độc thân trong ion
Câu 24. Nguyên tử trung tâm của phức chất có công thức hóa học là có số oxi hóa là bao nhiêu?
Câu 25. Phức chất X có công thức hóa học là Có bao nhiêu liên sigma có trong phức chất X?
Câu 26. Cho khí CO dư đi qua 2,6 gam hỗn hợp E đun nóng gồm sắt và iron oxide đến khi phản ứng hoàn toàn, sau đó dẫn toàn bộ khí thu được vào bình đựng nước vôi trong dư, thu được tối đa 10 gam kết tủa. Tổng lượng sắt trong E là bao nhiêu gam?
Câu 27. Trong quá trình bảo quản, muối thường bị oxi hoá bởi oxi không khí tạo thành hỗn hợp X chứa các hợp chất của Fe(II) và Để xác định lượng Fe(II) bị oxi hoá người ta hoà tan một lượng X trong dung dịch loãng chứa thu được 100 mL dung dịch Y. Tiến hành hai thí nghiệm với Y:
Thí nghiệm 1. Cho lượng dư dung dịch vào 25 mL dung dịch Y, lọc kết tủa, sấy khô rồi đem cân thu được 4,66 gam chất rắn.
Thí nghiệm 2. Thêm dung dịch (loãng, dư) vào 25 mL dung dịch Y, thu được dung dịch Z. Chuẩn độ dung dịch Z bằng dung dịch chuẩn đến khi đầu xuất hiện màu hồng (tồn tại khoảng 20 giây) thì hết 13,5mL.Phần trăm Fe(II) đã bị oxi hoá trong không khí bằng bao nhiêu? (Làm tròn kết quả đến hàng phần mười)
Câu 28. Khi hoà tan zinc chloride trong nước diễn ra một số quá trình cơ bản sau:
Zn2+(aq) + 6H2O(l) → [Zn(OH2)6]²+(aq) (I)
[Zn(OH2)6]²+(aq) [Zn(OH)(OH2)5] (aq) + H+(aq) Kc = 10-9 (II)
H+(aq) + H2O(l) → H3O+ (aq) (III)
Cho các phát biểu sau:
(1) Dung dịch zinc chloride có tính acid khá mạnh.
(2) Trong dung dịch zinc chloride, nước vừa là dung môi, vừa đóng vai trò base theo Brönsted - Lowry.
(3) Từ quá trình (III) có thể suy ra "H2O là base theo Brönsted - Lowry".
(4) Từ quá trình (I), (II) và (III) suy ra "trong nước, cation Zn2+ là acid theo Brönsted - Lowry".
(5) Quá trình (I) và (III) có thể diễn ra yếu hơn quá trình (II).
(6) Từ quá trình (II) có thể suy ra “[Zn(OH2)6]2+ là acid theo Arrhenius".
Số phát biểu đúng là bao nhiêu?
................................
................................
................................
Xem thêm đề kiểm tra Hóa học lớp 12 Kết nối tri thức có đáp án hay khác:
Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 1 (có lời giải)
Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 2 (có lời giải)
Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 3 (có lời giải)
Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 4 (có lời giải)
Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 5 (có lời giải)
Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 6 (có lời giải)
Đề kiểm tra Hóa học 12 Kết nối tri thức Chương 7 (có lời giải)
Xem thêm các tài liệu học tốt lớp 12 hay khác:
- Giải sgk Hóa học 12 Kết nối tri thức
- Giải Chuyên đề học tập Hóa 12 Kết nối tri thức
- Giải SBT Hóa học 12 Kết nối tri thức
- Giải lớp 12 Kết nối tri thức (các môn học)
- Giải lớp 12 Chân trời sáng tạo (các môn học)
- Giải lớp 12 Cánh diều (các môn học)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Soạn văn 12 (hay nhất) - KNTT
- Soạn văn 12 (ngắn nhất) - KNTT
- Giải sgk Toán 12 - KNTT
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Giải sgk Vật Lí 12 - KNTT
- Giải sgk Hóa học 12 - KNTT
- Giải sgk Sinh học 12 - KNTT
- Giải sgk Lịch Sử 12 - KNTT
- Giải sgk Địa Lí 12 - KNTT
- Giải sgk Giáo dục KTPL 12 - KNTT
- Giải sgk Tin học 12 - KNTT
- Giải sgk Công nghệ 12 - KNTT
- Giải sgk Hoạt động trải nghiệm 12 - KNTT
- Giải sgk Giáo dục quốc phòng 12 - KNTT
- Giải sgk Âm nhạc 12 - KNTT
- Giải sgk Mĩ thuật 12 - KNTT

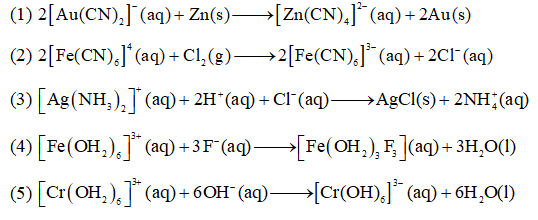

















 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

