C2H4 + H2 | Etilen + H2 | CH2=CH2 + H2 → CH3–CH3 | CH2=CH2 ra CH3–CH3
Phản ứng C2H4 + H2 hoặc Etilen + H2 hoặc CH2=CH2 + H2 hay CH2=CH2 ra CH3–CH3 thuộc loại phản ứng cộng đã được cân bằng chính xác và chi tiết nhất. Bên cạnh đó là một số bài tập có liên quan về C2H4 có lời giải, mời các bạn đón xem:
CH2=CH2 + H2 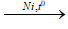 CH3–CH3
CH3–CH3
1. Phương trình phản ứng etilen tác dụng với H2
CH2 = CH2 + H2 CH3 – CH3
2. Hiện tượng của phản ứng etilen tác dụng với H2
- Tạo chất khí, không có khả năng làm mất màu dung dịch nước brom.
3. Cách tiến hành phản ứng etilen tác dụng với H2
- Dẫn khí etilen vào ống nghiệm chứa khí H2, có xúc tác Ni, đun nóng.
4. Mở rộng về tính chất hoá học của alkene
4.1. Phản ứng cộng
a) Phản ứng cộng hiđro (Phản ứng hiđro hoá)
CH2 = CH2 + H2 CH3 – CH3
b) Phản ứng cộng halogen (Phản ứng halogen hoá)
- alkene làm mất màu của dung dịch brom.
→ Phản ứng này dùng để nhận biết alkene.
Thí dụ:
CH2 = CH2 + Br2 → Br–CH2–CH2–Br
c) Phản ứng cộng HX (X là OH, Cl, Br,…)
Cộng nước
Thí dụ:
CH2 = CH2 + H – OH CH3 – CH2 – OH
Cộng axit HX
Thí dụ:
CH2 = CH2 + HCl → CH3 – CH2 – Cl
- Đối với các alkene có cấu tạo không đối xứng khi tác dụng với HX có thể sinh ra hỗn hợp hai sản phẩm.
Thí dụ:
* Quy tắc Mac-côp-nhi-côp: Trong phản ứng cộng HX (axit hoặc nước) vào liên kết C = C của alkene, H (phần mang điện tích dương) cộng vào C mang nhiều H hơn, X (hay phần mang điện tích âm) cộng vào C mang ít H hơn.
4.2. Phản ứng trùng hợp
- Phản ứng trùng hợp là quá trình kết hợp liên tiếp nhiều phân tử nhỏ giống nhau hoặc tương tự nhau tạo thành phân tử lớn gọi là polymer.
- Số lượng mắt xích trong một phân tử polymer gọi là hệ số trùng hợp, kí hiệu n.
Thí dụ: Trùng hợp etilen
4.3. Phản ứng oxi hoá
a) Oxi hoá hoàn toàn
CnH2n + O2 nCO2 + nH2O
⇒ Đốt cháy hoàn toàn alkene thu được
b) Oxi hoá không hoàn toàn
alkene làm mất màu dung dịch KMnO4 ⇒ Dùng để nhận biết alkene.
Thí dụ:
3CH2=CH2 + 4H2O + 2KMnO4 → 3HO–CH2–CH2–OH + 2MnO2↓ + 2KOH
5. Bài tập vận dụng liên quan
Câu 1: alkene là:
A. hydrocarbon không no, trong phân tử có các liên kết bội.
B. hydrocarbon không no, mạch hở, trong phân tử có 1 liên kết C=C.
C. hydrocarbon không no, mạch hở, trong phân tử có nhiều liên kết C=C.
D. hydrocarbon không no, mạch hở, trong phân tử có 2 liên kết C=C.
Hướng dẫn giải
Đáp án B
alkene là hydrocarbon không no, mạch hở, trong phân tử có 1 liên kết C=C.
alkene có công thức phân tử chung là CnH2n (n ≥ 2)
Câu 2: Chất X có công thức CH3–CH(CH3)–CH=CH2. Tên thay thế của X là
A. 2-methylbut-3-en
B. 3-methylbut-1-yne.
C. 3-methylbut-1-en
D. 2-methylbut-3-yne
Hướng dẫn giải
Đáp án C
3-methylbut-1-en
Chú ý: Mạch cacbon được đánh số bắt đầu từ phía gần liên kết đôi hơn.
Câu 3: Ứng với công thức phân tử C4H8 có bao nhiêu đồng phân cấu tạo mạch hở?
A. 2 B. 4 C. 3 D. 5
Hướng dẫn giải
Đáp án C
Các đồng phân cấu tạo mạch hở ứng với công thức C4H8 là:
CH2 = CH – CH2 – CH3; CH3 – CH = CH – CH3; CH2 = C(CH3)2.
Câu 4: hydrocarbon nào sau đây khi phản ứng với dung dịch brom thu được
1,2- đibrombutan?
A. But-1-en B. Butan
C. But-2-en D. 2-methylpropen
Hướng dẫn giải
Đáp án A
CH2 = CH – CH2 – CH3 + Br2 → CH2Br – CHBr – CH2 – CH3
(But – 1 – en) (1,2 – đibrombutan)
Câu 5: Phản ứng của but-1-en với HCl cho sản phẩm chính là:
A. 1-clobutan B. 2-clobuten
C. 2-clobutan D. 1-clobuten
Hướng dẫn giải
Đáp án C
CH2=CH-CH2-CH3 + HCl → CH3=CHCl-CH2-CH3 (sản phẩm chính)
Theo quy tắc cộng Mac-côp-nhi-côp: Trong phản ứng cộng HX vào liên kết đôi, nguyên tử H chủ yếu cộng vào nguyên tử cacbon bậc thấp hơn (có nhiều H hơn), nguyên tử hay nhóm nguyên tử X cộng vào nguyên tử cacbon bậc cao hơn (có ít H hơn).
Câu 6: Propilen có lẫn tạp chất là SO2, CO2 và hơi nước. Có thể loại bỏ tạp chất bằng cách:
A. Dẫn hỗn hợp qua dung dịch brom dư.
B. Dẫn hỗn hợp qua dung dịch NaCl dư.
C. Dẫn hỗn hợp lần lượt qua bình đựng dung dịch NaOH dư và bình đựng dung dịch H2SO4 đặc.
D. Dẫn hỗn hợp lần lượt qua bình đựng dung dịch brom dư và bình đựng dung dịch H2SO4 đặc.
Hướng dẫn giải
Đáp án C
Dẫn hỗn hợp khí qua bình đựng dung dịch NaOH dư có SO2 và CO2 bị hấp thụ.
SO2 + 2NaOH → Na2SO3 + H2O
CO2 + 2NaOH → Na2CO3 + H2O
Còn lại hơi nước sẽ bị hấp thụ bở dung dịch H2SO4 đặc (H2SO4 đặc có khả năng hút nước).
Câu 7: Dẫn từ từ 6,72 lít (đktc) hỗn hợp X gồm etilen và propilen và dung dịch brom, dung dịch brom bị nhạt màu, và không có khí thoát ra. Khối lượng dung dịch sau phản ứng tăng 9,8 gam. Thành phần phần trăm theo thể tích của etilen trong X là
A. 50,00%. B. 66,67%.
C. 57,14%. D. 28,57%.
Hướng dẫn giải
Đáp án B
% = .100 = 66,67%
Câu 8: Một hydrocarbon X cộng hợp với axit HCl theo tỷ lệ mol 1 : 1 tạo sản phẩm có thành phần khối lượng clo là 45,223 %. Công thức phân tử của X là
A. C4H8 B. C3H6 C. C3H8 D. C2H4
Hướng dẫn giải
Đáp án B
X + HCl → Y (CxHyCl)
→ MY = 78,5
→ MX = 78,5 – 36,5 = 42 (C3H6)
Câu 9: Để khử hoàn toàn 200 ml dung dịch KMnO4 0,2M tạo thành chất rắn màu đen cần V lít khí C3H6 (đktc). Giá trị tối thiểu của V là
A. 2,240 B. 2,688 C. 4,480 D. 1,344
Hướng dẫn giải
Đáp án D
3C3H6 + 2KMnO4 + 4H2O → 3C3H6(OH)2 + 2MnO2(đen) + 2KOH
= 0,2.0,2 = 0,04 mol
Theo phương trình: . = = 0,06 mol
→ V = 0,06.22,4 = 1,344 lít
Câu 10: Hỗn hợp X gồm propene và một alkene đồng đẳng. Đốt cháy hoàn toàn 1 mol hỗn hợp X cần 4,75 mol O2. alkene còn lại trong X có thể là:
A. buten. B. propan. C. etan. D. eten.
Hướng dẫn giải
Đáp án A
→= 4,75 → n = 3,17
Hỗn hợp chứa propene có 3C, vậy chất còn lại phải có > 3C, dựa vào đáp án chọn C4H8.
Xem thêm các phương trình hóa học hay khác:
- CH2=CH2 + Br2 → CH2Br–CH2Br
- CH2=CH2 + Cl2 → CH2Cl–CH2Cl
- CH2=CH2 + HCl → CH2Cl–CH3
- CH2=CH2 + HBr → CH2Br–CH3
- CH2=CH2 + H2O → CH2OH–CH3
- CH2=CH2 + H2SO4 → CH3–CH2OSO3H
- nCH2=CH2 → (-CH2-CH2 -)n
- C2H4 + 3O2 → 2CO2 + 2H2O
- 3CH2=CH2 + 4H2O + 2KMnO4 → 3OH-CH2-CH2 – OH + 2MnO2 + 2KOH
- CH2=CH2 + O2 → CH3CHO
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)








 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



