Cu(OH)2 + HCl → CuCl2 + H2O | Cu(OH)2 ra CuCl2
Phản ứng Cu(OH)2 + HCl hay Cu(OH)2 ra CuCl2 thuộc loại phản ứng trao đổi đã được cân bằng chính xác và chi tiết nhất. Bên cạnh đó là một số bài tập có liên quan về Cu(OH)2 có lời giải, mời các bạn đón xem:
Cu(OH)2 + 2HCl → CuCl2 + 2H2O
1. Phương trình phản ứng Cu(OH)2 tác dụng với HCl
Cu(OH)2 + 2HCl → CuCl2 + 2H2O
Phản ứng này thuộc loại phản ứng trao đổi.
2. Hiện tượng của phản ứng Cu(OH)2 tác dụng với HCl
- Chất rắn Cu(OH)2 tan ra tạo dung dịch có màu xanh lam.
3. Cách tiến hành phản ứng Cu(OH)2 tác dụng với HCl
- Nhỏ từ từ dung dịch HCl vào ống nghiệm có chứa Cu(OH)2.
4. Cách viết phương trình ion thu gọn của phản ứng Cu(OH)2 tác dụng với HCl
Bước 1: Viết phương trình phân tử:
Cu(OH)2 + 2HCl → CuCl2 + 2H2O
Bước 2: Viết phương trình ion đầy đủ bằng cách: chuyển các chất vừa dễ tan, vừa điện li mạnh thành ion; các chất điện li yếu, chất kết tủa, chất khí để nguyên dưới dạng phân tử:
Bước 3: Viết phương trình ion thu gọn từ phương trình ion đầy đủ bằng cách lược bỏ đi các ion giống nhau ở cả hai vế:
5. Mở rộng về phản ứng trao đổi trong dung dịch chất điện li
Xét phản ứng:
Dung dịch A + dung dịch B → Sản phẩm.
- Phản ứng xảy ra trong dung dịch các chất điện li là phản ứng giữa các ion.
- Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi các ion kết hợp được với nhau tạo thành ít nhất 1 trong số các chất sau:
+ Chất kết tủa.
+ Chất điện li yếu.
+ Chất khí.
Thí dụ:
+ Phản ứng tạo thành chất kết tủa:
Na2SO4 + BaCl2 → 2NaCl + BaSO4↓
+ Phản ứng tạo thành chất điện li yếu:
HCl + NaOH → NaCl + H2O
+ Phản ứng tạo thành chất khí:
Fe + H2SO4 loãng → FeSO4 + H2↑
6. Mở rộng về copper (II) hydroxide Cu(OH)2
- Cu(OH)2 là chất rắn, màu xanh, không tan trong nước.
- Cu(OH)2 là một bazơ, dễ tan trong các dung dịch axit. Ví dụ:
Cu(OH)2 + 2HCl → CuCl2 + 2H2O
- Cu(OH)2 dễ bị nhiệt phân hủy:
Cu(OH)2 CuO + H2O
7. Bài tập vận dụng liên quan
Câu 1: Điều chế Cl2 từ HCl và MnO2. Cho toàn bộ khí Cl2 điều chế được qua dung dịch NaI, sau phản ứng thấy có 12,7 gam I2 sinh ra. Khối lượng HCl có trong dung dịch đã dùng là
A. 9,1 gam.
B. 8,3 gam.
C. 7,3 gam.
D. 12,5 gam.
Hướng dẫn giải:
Đáp án C
Theo PTHH: Cl2 + 2NaI → 2 NaCl + I2
Theo PTHH: MnO2 + 4HCl MnCl2 + 2H2O +Cl2
= 0,05.4 = 0,2 mol
→ m HCl = 0,2. 36,5 = 7,3 g.
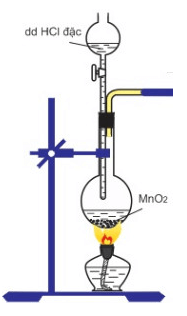
Câu 2:Hiện tượng xảy ra trong thí nghiệm là:
A. Chỉ có khí màu vàng thoát ra
B. Có khí màu vàng sinh ra, đồng thời có kết tủa
C. Chất rắn MnO2 tan dần
D. Có khí màu vàng sinh ra, đồng thời MnO2 tan dần
Hướng dẫn giải:
Đáp án D
Phản ứng: MnO2 + 4HClđ MnCl2 + Cl2↑ + 2H2O
→ Hiện tượng của phản ứng: Có khí màu vàng thoát ra, MnO2 tan dần.
Câu 3: Nhận xét nào sau đây về khí hidro clorua là không đúng?
A. Là chất khí ở điều kiện thường
B. Có mùi xốc
C. Tan tốt trong nước
D. Có tính axit
Hướng dẫn giải:
Đáp án D
Khí hiđro clorua không có tính axit.
Câu 4: Nồng độ cao nhất của dung dịch HCl ở 20oC là
A. 25%
B. 37%
C. 20%
D. 50%
Hướng dẫn giải:
Đáp án B
Nồng độ cao nhất của dung dịch HCl ở 20oC là 37%
Câu 5. Để trung hòa 20 ml dung dịch HCl 0,1M cần 10 ml dung dịch NaOH nồng độ x mol/l. Giá trị của x là
A. 0,3. B. 0,4. C. 0,2. D. 0,1.
Hướng dẫn giải
Đáp án C
nHCl = 0,1.0,02 = 0,002 mol
HCl + NaOH → NaCl + H2O
0,002 → 0,002 mol
Câu 6: Cho 36 gam FeO phản ứng vừa đủ với dung dịch chứa a mol HCl. Giá trị của a là
A. 1,00. B. 0,50. C. 0,75. D. 1,25.
Hướng dẫn giải
Đáp án A
2HCl + FeO → FeCl2 + H2O
Theo PTHH: nHCl = 2nFeO = 1 mol
Câu 7. Cần dùng 300 gam dung dịch HCl 3,65% để hòa tan vừa hết x gam Al2O3. Giá trị của x là
A. 51. B. 5,1. C. 153. D. 15,3.
Hướng dẫn giải
Đáp án B
6HCl + Al2O3 → 2AlCl3 + 3H2O
0,3 → 0,05 mol
= 0,05.102 = 5,1 gam
Câu 8. Cho 5,6 gam một oxit kim loại tác dụng vừa đủ với HCl cho 11,1 gam muối clorua của kim loại đó. Cho biết công thức oxit kim loại?
A. Al2O3. B. CaO. C. CuO. D. FeO.
Hướng dẫn giải
Đáp án B
Gọi công thức oxit là M2Oa
2aHCl + M2Oa → 2MCla + aH2O
Gọi số mol H2O là x (mol) ⇒ nHCl = 2x (mol)
Bảo toàn khối lượng: 36,5.2x + 5,6 = 11,1 + 18.x
⇒ x = 0,1 mol
a |
1 |
2 |
3 |
M |
20 |
40 |
60 |
Kết luận |
Loại |
Ca |
Loại |
Câu 9. Cho 30,00 gam hỗn hợp X gồm Fe và FeO phản ứng với dung dịch HCl dư, đến khi phản ứng xảy ra hoàn toàn thu được 6,72 lít khí H2 (đktc). Khối lượng của FeO trong 30,00 gam hỗn hợp X là
A. 13,2 gam. B. 46,8 gam. C. 16,8 gam. D. 5,6 gam.
Hướng dẫn giải
Đáp án A
2HCl + FeO → FeCl2 + H2O
2HCl + Fe → FeCl2 + H2
Theo PTHH:
nFe = nkhí = 0,3 mol ⇒ mFeO = 30 – 0,3.56 = 13,2 gam.
Câu 10. Để hoà tan hết hỗn hợp Zn và ZnO phải dùng 100,8 ml dung dịch HCl 36,5% (D = 1,19g/ml) thu được 0,4 mol khí. Phần trăm về khối lượng hỗn hợp Zn và ZnO ban đầu lần lượt là
A. 40% và 60%. B. 45% và 55%.
C. 50% và 50%. D. 61,6% và 38,4%.
Hướng dẫn giải
Đáp án D
2HCl + ZnO → ZnCl2 + H2O (1)
2HCl + Zn → ZnCl2 + H2 (2)
Theo PTHH (2):
nHCl (2) = 2.nZn = 0,8 mol ⇒ nHCl (1) = 1,2 – 0,8 = 0,4 mol
mhỗn hợp = 0,4.65 + 0,2.81 = 42,2 gam
Câu 11. Cho 36,5 gam dung dịch HCl 10% vào một cốc đựng NaHCO3 dư thì thu được V lit khí ở đktc. Giá trị của V là
A. 44,8. B. 4,48. C. 22,4. D. 2,24.
Hướng dẫn giải
Đáp án D
NaHCO3 + HCl → NaCl + H2O + CO2
0,1 0,1 mol
⇒ V = 0,1.22,4 = 2,24 lít.
Câu 12. Cho 50 gam CaCO3 tác dụng vừa đủ với dung dịch HCl 20% (D = 1,2g/ml). Khối lượng dung dịch HCl đã dùng là
A. 152,08 gam. B. 55,0 gam.
C. 180,0 gam. D. 182,5 gam.
Hướng dẫn giải
Đáp án D
CaCO3 + 2HCl → CaCl2 + H2O + CO2
0,5 → 1 mol
Xem thêm các phương trình hóa học hay khác:
- Cu(OH)2 → CuO + H2O
- Cu(OH)2 + H2SO4 → CuSO4 + H2O
- Cu(OH)2 + 2HNO3 → Cu(NO3)2 + H2O
- Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2
- Cu(OH)2 + CH3CHO → CH3COOH + Cu2O ↓ + H2O
- Cu(OH)2 + HCHO → HCOOH + Cu2O ↓ + H2O
- 2Cu(OH)2 + HCOOH → CO2 + Cu2O ↓ + 4H2O
- Cu(OH)2 + C3H5(OH)3 → [C3H5(OH)2O]2Cu
- Cu(OH)2 + C2H4(OH)2 → [C2H4(OH)O]2Cu
- Cu(OH)2 + C6H12O6 → [C6H11O6]2Cu + H2O
- Cu(OH)2 + C12H22O11 → [C12H21O11]2Cu + H2O
- Cu(OH)2 + CH3COOH → (CH3COO)2Cu + H2O
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)









 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



