Giáo án Hóa học 8 Bài 43: Pha chế dung dịch mới nhất
Giáo án Hóa học 8 Bài 43: Pha chế dung dịch mới nhất
Xem thử Giáo án KHTN 8 KNTT Xem thử Giáo án KHTN 8 CTST Xem thử Giáo án KHTN 8 CD
Chỉ từ 500k mua trọn bộ Kế hoạch bài dạy (KHBD) hay Giáo án KHTN 8 cả năm (mỗi bộ sách) bản word chuẩn kiến thức, trình bày đẹp mắt, dễ dàng chỉnh sửa:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận giáo án
I. MỤC TIÊU:
1. Kiến thức :
HS biết thực hiện phần tính toán các đại lượng liên quan đến dung dịch như: lượng số mol chất tan, khối lượng chất tan, khối lượng dung dịch, khối lượng dung môi, thể tích dung môi, để từ đó đáp ứng được yêu cầu pha chế một khối lượng hay thể tích dung dịch với nồng độ theo yêu cầu pha chế.
2. Kĩ năng :
Biết cách pha chế dung dịch theo những số liệu đã tính toán
3. Thái độ :
Rèn tính cẩn thận trong các thao tác, ý thức làm việc tập thể.
4. Năng lực cần hướng tới :
- Năng lực tự học
- Năng lực giải quyết vấn đề thông qua môn Hóa học
- Năng lực vận dụng kiến thức hóa học vào cuộc sống
- Năng lực giao tiếp
- Năng lực hợp tác
- Năng lực nghiên cứu và thực hành Hóa học
- Năng lực sử dụng ngôn ngữ Hóa Học
- Năng lực tính toán.
II. CHUẨN BỊ:
1. Giáo viên :
-Hoá chất: CuSO4 (khan), nước cất
-Dụng cụ: cân kĩ thuật, cốc 250ml, bình nước, ống đong, đũa TT, thìa lấy hoá chất.
2. Học sinh :
Học bài cũ và chuẩn bị bài mới.
III. CÁC HOẠT ĐỘNG DẠY – HỌC:
1. Ổn định trật tự, kiểm tra bài cũ (5 phút)
HS 1: làm bài tập 3c /146 sgk.
HS 2: làm bài tập 4c /146 sgk.
HS 3: Thế nào là nồng độ phần trăm của dung dịch, nồng độ mol của dung dịch viết công thức tính 2 đại lượng trên, giải thích ý nghĩa các đại lượng?
2. Hoạt động dạy học
Hoạt động 1: Khởi động – vào bài (2 phút)
Chúng ta đã biết cách tính toán nồng độ dung dịch. Nhưng làm thế nào để pha chế được dung dịch theo nồng độ cho biết? Hôm nay chúng ta tìm hiểu cách pha chế một dung dịch theo nồng độ cho trước? Chúng ta hãy tìm hiểu bài học.
Hoạt động 2: Hình thành kiến thức (30 phút)
| GIÁO VIÊN | HỌC SINH | NỘI DUNG GHI BẢNG |
|---|---|---|
|
Bài tập : Từ muối NaCl nước cất và những dụng cụ cần thiết, hãy tính toán và gới thiệu cách pha chế 1. Pha chế 50 gam dd NaCl có nồng độ 10% - Trong bài tập các em đã biết những đại lượng nào? ?Cần tìm những đại lượng nào để pha chế dung dịch ? - Hãy viết công thức tính mNaCl từ công thức tính C% ? - Tính mdm dựa vào công thức nào? Chia lớp thành 4 nhóm thảo luận và giải, 1 hs lên bảng trình bày GV: hướng dẫn HS cách pha chế + Cân 5 g NaCl +Hướng dẫn cách dùng ống đong 45 ml nước cất và đổ nước cất dần dần vào cốc, khuấy nhẹ. +Dựa vào vạch trên cốc và kết luận số ml dung dịch thu được. ? Hãy nêu các công việc cần thực hiện để pha chế 50 gam NaCl có nồng độ 10% ? GV: yêu cầu HS đọc phần cách pha chế. 2. Pha chế 50 ml dung dịch NaCl có nống độ 1M - Trong bài tập, các em đã biết những đại lượng nào - Cần tìm những đại lượng nào để pha chế dung dịch ? - Hãy viết công thức tính nNaCl từ công thức tính CM của dung dịch? - Tính mNaCl dựa vào công thức nào ? GV: gọi 1 HS lên bảng giải Gv: thu 5 bài nhanh nhất chấm lấy điểm. - hướng dẫn HS cách pha chế -Lấy 2,925 gNaCl vào ống đong - Đổ nước cất dần dần vào ống đong, khuấy đều đến vạch 50ml GV: Gọi 1 HS đọc cách pha chế |
-mdd NaCl = 50 (g) C% = 10% -Từ 2 dữ kiện trên tìm được khối lượng chất tan → tìm khối lượng dung môi. mdm = mdd - mct -Các nhóm thảo luận tính toán để trả lời các vấn đề GV yêu cầu - Đại diện nhóm nhận xét, bổ sung (nếu có) - HS thực hiện theo hướng dẫn của GV +Cân 5g NaCl cho và cốc 100ml +Dùng ống đong 45ml nước cất đổ vào cốc, khuấy nhẹ +Thu được 50g dung dịch. Vdd = 50 (ml) = 0,05 (l) CM = 1M -Tìm số mol -Tìm khối lượng chất tan -Tìm khối lượng dung môi n = CM . V mNaCl = n.M 1 hs lên bảng trình bày bài giải, các hs còn lại giải cá nhân. Hs dưới lớp nhận xét bài giải trên bảng, bổ sung (nếu có) -Hs tiếp thu ý kiến |
I. Cách pha chế một dung dịch theo nồng độ cho trước. Bài tập 1 : Pha chế 50 gam NaCl có nồng độ 10% 1. Tính toán. -Tìm khối lượng chất tan: -Tìm khối lượng dung môi (nước): mdd = mdm + mct → mnước = mdd – mNaCl = 50 – 5 = 45 (g) 2. Pha chế : Cân lấy 5 g NaCl cho vào cốc có dung tích 100 ml. Cân lấy 45 gam (hoặc đong 45 ml) nước cất, rồi đổ dần dần vào cốc khuấy nhẹ. Được 50 gam dung dịch NaCl. Bài tập 2 : 1. Tính toán : - Số mol chất tan: nNaCl = CM. V n = 1. 0,05 n = 0,05 mol - Khối lượng NaCl là : mNaCl = n.M = 0,05 . 58,5 = 2,925 (g) 2. Pha chế : Cân lấy 2,925 g NaCl cho vào cốc thuỷ tinh có dung tích 100ml. Đổ dần dần nước cất vào cốc và khuấy nhẹ cho đủ 50 ml dung dịch. Ta được 50 ml dung dịch NaCl 1M |
Hoạt động 3: Luyện tập – vận dụng (5 phút)
- Giáo viên hệ thống kiến thức và hướng dẫn HS làm các bài tập sau:
- Bài tập : Đun nhẹ 40 gam dung dịch NaCl đến khi nước bay hơi hết, người ta thu được 8 gam muối NaCl khan. Tính nồng độ phần trăm của dung dịch thu được ?
Hướng dẫn:
Trong 40 gam dung dịch NaCl có 8 gam muối khan.
Vậy nồng độ phần trăm của dung dịch là
Hoạt động 4: Tìm tòi, mở rộng (2 phút)
-Học bài giảng và làm BTVN: 1,2,3 sgk trang 149
-Soạn trước phần còn lại
V. RÚT KINH NGHIỆM
............................................................................................................................................................
............................................................................................................................................................
............................................................................................................................................................
Xem thử Giáo án KHTN 8 KNTT Xem thử Giáo án KHTN 8 CTST Xem thử Giáo án KHTN 8 CD
Xem thêm các bài soạn Giáo án Hóa học lớp 8 theo hướng phát triển năng lực mới nhất, hay khác:
- Giáo án Hóa học 8 Bài 42: Nồng độ dung dịch
- Giáo án Hóa học 8 Bài 42: Nồng độ dung dịch (Tiết 2)
- Giáo án Hóa học 8 Bài 43: Pha chế dung dịch (Tiết 2)
- Giáo án Hóa học 8 Bài 44: Bài luyện tập 8
- Giáo án Hóa học 8 Bài 45: Bài thực hành 7
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Giáo án Hóa học lớp 8 mới, chuẩn nhất của chúng tôi được biên soạn bám sát nội dung sgk Hóa học 8 theo chuẩn Giáo án của Bộ GD & ĐT.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giáo án lớp 8 (các môn học)
- Giáo án điện tử lớp 8 (các môn học)
- Giáo án Toán 8
- Giáo án Ngữ văn 8
- Giáo án Tiếng Anh 8
- Giáo án Khoa học tự nhiên 8
- Giáo án KHTN 8
- Giáo án Lịch Sử 8
- Giáo án Địa Lí 8
- Giáo án GDCD 8
- Giáo án HĐTN 8
- Giáo án Tin học 8
- Giáo án Công nghệ 8
- Giáo án Vật Lí 8
- Giáo án Hóa học 8
- Giáo án Sinh học 8
- Đề thi lớp 8 (các môn học)
- Đề thi Ngữ Văn 8 (có đáp án)
- Chuyên đề Tiếng Việt lớp 8
- Đề thi Toán 8
- Đề cương ôn tập Toán 8
- Đề thi Tiếng Anh 8 (có đáp án)
- Đề thi Tiếng Anh 8 mới (có đáp án)
- Đề thi Khoa học tự nhiên 8 (có đáp án)
- Đề thi Lịch Sử và Địa Lí 8 (có đáp án)
- Đề thi GDCD 8 (có đáp án)
- Đề thi Tin học 8 (có đáp án)
- Đề thi Công nghệ 8 (có đáp án)

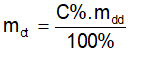
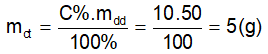
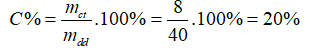





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

