Đề thi vào lớp 10 môn Hóa học năm 2026 có đáp án (Trắc nghiệm - Đề 1)
Đề thi vào lớp 10 môn Hóa học
Thời gian: 60 phút
Đề bài:
Cho nguyên tử khối của các nguyên tố: C = 12; H = 1; N = 14; S = 32; Ca = 40; Mg = 24; Al = 27; Fe = 56; Ag = 108; Zn = 65.
Câu 1. Dãy các kim loại được xếp theo chiều mức độ hoạt động hóa học tăng dần từ trái sang phải là
A. Fe, Cu, Al.
B. Cu, Fe, Al.
C. Al, Fe, Cu.
D. Cu, Al, Fe.
Câu 2. Trên bề mặt của chậu nước vôi để ngoài không khí thường bao phủ lớp váng màu trắng đục. Lớp váng đó là
A. Ca(HCO3)2.
B. Ca(OH)2.
C. CaCO3.
D. CaO.
Câu 3. Cho 13,6 gam hỗn hợp X gồm axit axetic và rượu etylic được trộn theo tỉ lệ mol tương ứng là 3 : 2. Đun nóng X với H2SO4 đặc một thời gian thu được m gam este CH3COOCH2CH3 với hiệu suất phản ứng là 80%. Giá trị của m là
A. 7,04g.
B. 8,80g.
C. 10,56g.
D. 11,00g.
Câu 4. Cho 180g dung dịch glucozơ nồng độ 20% tác dụng với dung dịch AgNO3 trong NH3 dư. Biết phản ứng xảy ra hoàn toàn. Khối lượng Ag thu được là
A. 64,8g.
B. 32,4g.
C. 21,6g.
D. 43,2g.
Câu 5. Kim loại X phản ứng với axit HCl tạo muối XCl2. Kim loại X phản ứng với Cl2 tạo muối XCl3. X là
A. Cu.
B. Zn.
C. Al.
D. Fe.
Câu 6. Chất khí nào sau đây được dung làm nhiên liệu cho đèn xì để hàn cắt kim loại?
A. cacbon monooxit.
B. etilen.
C. metan.
D. axetilen.
Câu 7. Trung hòa 200ml H2SO4 nồng độ aM cần vừa đủ 200ml dung dịch NaOH 1M. Giá trị của a là
A. 0,50.
B. 1,20.
C. 0,75.
D. 1,00.
Câu 8. Cho m gam kim loại Mg tác dụng với dung dịch HCl dư. Sau phản ứng cô cạn dung dịch được 19 gam muối khan. Giá trị của m là
A. 9,6.
B. 7,2.
C. 2,4.
D. 4,8.
Câu 9. Công thức chung của tinh bột là
A. C6H12O6.
B. (-C6O10O5-)n.
C. (- C6H12O6 -)n.
D. C12H22O11.
Câu 10. Hiện tượng xảy ra khi nhỏ dung dịch AgNO3 vào ống nghiệm chứa dung dịch KCl là
A. không có hiện tượng gì.
B. xuất hiện kết tủa vàng.
C. xuất hiện kết tủa trắng.
D. xuất hiện kết tủa đen.
Câu 11. Axit clohiđric phản ứng với tất cả các chất nào trong dãy sau?
A. Ca(OH)2, Cu.
B. Fe, Ag.
C. FeCl2, Mg.
D. Fe2O3, Al.
Câu 12. Thuốc thử để nhận biết dung dịch glucozơ và dung dịch rượu etylic là
A. phenolphtalein.
B. Na.
C. Quỳ tím.
D. AgNO3 trong NH3.
Câu 13. Chọn câu đúng trong các câu sau:
A. Metan, benzen đều làm mất màu dung dịch brom.
B. Etilen, benzen đều làm mất màu dung dịch brom.
C. Metan, etilen, axetilen đều làm mất màu dung dịch brom.
D. Etilen, axetilen đều làm mất màu dung dịch brom.
Câu 14. Khí CO được dùng làm chất đốt trong công nghiệp, có lẫn tạp chất là CO2 và SO2. Hóa chất nào sau đây có thể loại bỏ các tạp chất trên?
A. H2O dư.
B. Dung dịch NaCl dư.
C. Dung dịch Ca(OH)2 dư.
D. Dung dịch HCl dư.
Câu 15. Khí nào sau đây không phản ứng với H2O và dung dịch NaOH?
A. Cl2.
B. SO2.
C. CO.
D. CO2.
Câu 16. Dao, cuốc, xẻng bằng thép sau khi sử dụng sẽ giữ được độ bền lâu nếu?
A. Rửa sạch, lau khô.
B. Ngâm trong nước tự nhiên lâu ngày.
C. Ngâm trong nước muối một thời gian.
D. Để trong tự nhiên.
Câu 17. Muối nào sau đây không tan trong nước?
A. K2SO3
B. Na2SO3
C. CuCl2
D. BaSO4.
Câu 18. Đun nóng chất béo trong dung dịch NaOH thu được các sản phẩm là
A. Muối natri của axit axetic và glixerol.
B. Axit axetic và glixerol.
C. Axit béo và glixerol.
D. Muối natri của axit béo và glixerol.
Câu 19. Có 3 dung dịch: NaOH, HCl, NaCl. Bằng một lần thử duy nhất có thể dùng thuốc thử nảo để nhận biết ba dung dịch trên?
A. Dung dịch BaCl2.
B. BaCO3.
C. Phenolphtalein.
D. Quỳ tím.
Câu 20. Cho kim loại đồng vào dung dịch H2SO4 đặc, nóng sẽ xảy ra hiện tượng nào sau đây?
A. Đồng tan, thu được dung dịch không màu và khí không màu, mùi hắc.
B. Đồng tan, thu được dung dịch màu xanh và khí không màu, mùi hắc.
C. Đồng tan, thu được dung dịch không màu và khí không màu, không mùi.
D. Đồng tan, thu được dung dịch màu vàng và khí không màu, mùi hắc.
Câu 21. Cho 9,2 gam rượu etylic tác dụng với Na dư thu được V lít H2 ở đktc. Giá trị của V là
A. 2,24 lít.
B. 4,48 lít.
C. 3,36 lít.
D. 1,12 lít.
Câu 22. Cho các oxit sau: Na2O, FeO, SO2. Những oxit phản ứng được với nước là
A. FeO, SO2.
B. Na2O, SO2.
C. Na2O, FeO.
D. Cả 3 oxit trên.
Câu 23. Cho 12,8 gam kim loại R có hóa trị II tác dụng hết với khí clo tạo thành 27 gam muối. Kim loại R là
A. Mg.
B. Zn.
C. Cu.
D. Ca.
Câu 24. Chất X được sinh ra từ phản ứng thủy phân protein có khối lượng mol phân tử là 89 g/mol. Đốt cháy hoàn toàn 13,35 gam X thu được 19,8 gam CO2; 9,45 gam H2O và 1,68 lít khí N2 ở đktc. X có công thức phân tử là
A. C2H5NO2.
B. C3H7NO2.
C. C3H5NO2.
D. C4H9NO2.
Câu 25. Phân đạm ure có công thức là
A. CO(NH2)2.
B. NaNO3.
C. (NH4)2SO4.
D. NH4NO3.
Câu 26. Cho các dung dịch: HCl, KCl, Ca(OH)2, BaCl2. Dung dịch Na2CO3 phản ứng với
A. hai chất.
B. bốn chất.
C. ba chất.
D. một chất.
Câu 27. Sản phẩm thu được khi cho dung dịch NaOH vào dung dịch FeCl3 là
A. NaCl và Fe(OH)2.
B. NaCl và Fe(OH)3.
C. Fe2O3 và NaCl.
C. Fe(OH)2; Fe(OH)3 và NaCl.
Câu 28. Dẫn 1,5 mol khí CO2 từ từ đến hết vào dung dịch chứa 1,8 mol NaOH thu được dung dịch có chứa chất tan là
A. NaHCO3.
B. NaOH và Na2CO3.
C. Na2CO3.
D. NaHCO3 và Na2CO3
Câu 29. Dẫn khí CO quan m gam bột Fe2O3 nung nóng, sau một thời gian thu được 24 gam chất rắn X và hỗn hợp khí Y. Dẫn khí Y vào dung dịch nước vôi trong dư thu được 30 gam kết tủa. Giá trị của m là
A. 26,4g.
B. 28,8g.
C. 23,2g.
D. 33,6g.
Câu 30. Phương pháp điều chế nhôm trong công nghiệp là
A. điện phân nóng chảy Al2O3.
B. điện phân nóng chảy Al(OH)3.
C. dùng CO khử Al2O3.
D. dùng kim loại Na tác dụng với dung dịch AlCl3.
Câu 31. Cho m gam hỗn hợp Mg, Al và Zn được chia thành hai phần bằng nhau.
- Phần 1. Tác dụng với H2SO4 loãng, dư thu được 5,6 lít khí H2 ở đktc.
- Phần 2. Tác dụng với oxi dư thu được 11,15 gam hỗn hợp các oxit kim loại.
Giá trị của m là:
A. 7,15g.
B. 18,3g.
C. 14,3g.
D. 9,15g.
Câu 32. Các chất X và Y đều là chất rắn màu đen. Bình hấp thụ khí Z chứa Ca(OH)2. Tiến hành thí nghiệm theo hình vẽ:
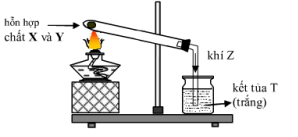
Hỗn hợp các chất X, Y, Z và T là
A. Al2O3, C, CO2 và CaCO3.
B. CuO, C, CO2 và CaCO3.
C. MnO2, KClO3, O2 và CaCO3.
D. CuO, C, CO và CaCO3.
Câu 33. Cho các chất: CH3 –COOH, CH4, C2H6, C2H2, C12H22O11. Dãy chất chỉ gồm các hiđrocacbon là
A. CH3 –COOH, CH4, C2H6, C2H2, C12H22O11.
B. CH3 –COOH, CH4, C2H6, C2H2,
C. CH4, C2H6, C2H2, C12H22O11.
D. CH4, C2H6, C2H2.
Câu 34. Polime nào sau dây không phải là polime thiên nhiên?
A. Poli(vinyl clorua).
B. Xenlulozơ.
C. Protein.
D. Tinh bôt.
Câu 35. Cho sơ đồ phản ứng (chưa cân bằng) sau:
CH3 – COOH + X → CH3COOK + Y
Cặp chất X, Y phù hợp là
A. KOH, H2.
B. K, H2.
C. KCl, HCl.
D. K, H2O.
Câu 36. Cho các oxit sau: CO2, SO2, BaO, Na2O, CO. Dãy gồm các oxit axit là
A. BaO, Na2O, CO.
B. CO2, SO2, CO.
C. CO2, SO2.
D. CO2, SO2, BaO.
Câu 37. Cho 8 gam hỗn hợp gồm Mg và Fe vào dung dịch HCl dư. Phản ứng kết thúc thu được 4,48 lít khí H2 ở đktc. Phần trăm khối lượng của sắt trong hỗn hợp là
A. 70%.
B. 30%.
C. 60%.
D. 40%.
Câu 38. Một dung dịch A có pH = 3. Dung dịch A có môi trường là
A. không xác định được.
B. axit.
C. bazơ.
D. trung tính.
Câu 39. Hiđrocacbon X là chất khí ở điều kiện thường, có khả năng làm mất màu dung dịch nước brom, có tác dụng làm quả xanh mau chín. X là
A. etilen.
B. benzen.
C. metan.
D. axetilen.
Câu 40. Hai chất CH3 – CH2 – OH và CH3 – O – CH3 khác nhau về
A. công thức cấu tạo.
B. số lượng nguyên tử.
C. khối lượng mol phân tử.
D. công thức phân tử.
Đáp án & Thang điểm
Câu 1. B
Dãy hoạt động hóa học của một số kim loại: K, Na, Mg, Al, Zn, Fe, Pb, (H), Cu, Ag, Au.
→ Chiều mức độ hoạt động hóa học tăng dần từ trái sang phải là: Cu; Fe; Al.
Câu 2. C
Nguyên nhân xuất hiện lớp váng là do:
Ca(OH)2 + CO2 → CaCO3 (↓) + H2O.
Câu 3. A
Gọi số mol của CH3COOH là 3a mol → số mol của CH3CH2OH là 2a mol
mX = 13,6 gam → 60.3a + 46.2a = 13,6 → a = 0,05 mol
PTHH:
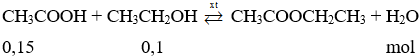
Giả sử hiệu suất là 100% thì rượu etylic hết, nên số mol sản phẩm phản ứng tính theo số mol rượu etylic.
Số mol este là: neste thực tế = neste lý thuyết. H = 0,1.80% = 0,08 mol
→ m = n.M = 0,08.88 = 7,04 gam.
Câu 4. D
Khối lượng glucozơ có trong dung dịch là:
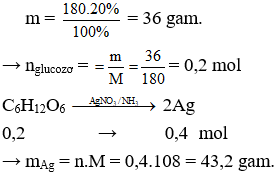
Câu 5. D
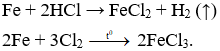
Câu 6. D
Khi axetilen cháy trong oxi, nhiệt độ ngọn lửa có thể lên tới 3000°C. Vì vậy axetilen được sử dụng làm nhiên liệu trong đèn xì oxi – axetilen để hàn cắt kim loại.
Câu 7. A
nNaOH = CM.V = 1.0,2 = 0,2 mol;
nH2SO4 = CM.V = 0,2.a mol
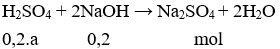
Theo PTHH có: nNaOH = 2.naxit → 0,2 = 2.0,2.a → a = 0,5.
Câu 8. D
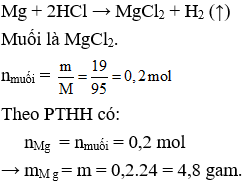
Câu 9. B
Công thức chung của tinh bột là: (-C6O10O5-)n.
Câu 10. C
AgNO3 + KCl → AgCl (↓ trắng) + KNO3.
Câu 11. D
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
2Al + 6HCl → 2AlCl3 + 3H2 (↑)
Câu 12. D
Sử dụng dung dịch AgNO3 trong NH3
+ Có chất màu sáng bạc bám trên thành ống nghiệm → glucozơ.
+ Không hiện tượng → rượu etylic.
Câu 13. D
Etilen, axetilen đều làm mất màu dung dịch brom. PTHH:
C2H4 + Br2 → C2H4Br2
C2H2 + 2Br2 → C2H2Br4.
Câu 14. C
Sử dụng dung dịch Ca(OH)2 dư. SO2 và CO2 phản ứng bị giữ lại, còn CO không phản ứng thoát ra khỏi dung dịch thu được CO tinh khiết.
SO2 + Ca(OH)2 dư → CaSO3 (↓) + H2O
CO2 + Ca(OH)2 dư → CaCO3 (↓) + H2O
Câu 15. C
CO là oxit trung tính nên không tác dụng với H2O và NaOH.
Câu 16. A
Lau chùi sạch sẽ đồ dùng bằng thép sau khi sử dụng sẽ giúp kim loại bị ăn mòn chậm hơn, đồ đạc được bền lâu hơn.
Câu 17. D
BaSO4 không tan trong nước.
Câu 18. D
Đun nóng chất béo trong dung dịch NaOH thu được muối natri của axit béo và glixerol.
Câu 19. D
Sử dụng quỳ tím:
+ Quỳ tím chuyển sang màu đỏ → HCl.
+ Quỳ tím chuyển sang màu xanh → NaOH.
+ Quỳ tím không chuyển màu → NaCl.
Câu 20. B
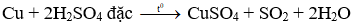
Khí SO2 không màu, mùi hắc. Dung dịch CuSO4 có màu xanh.
Câu 21. A
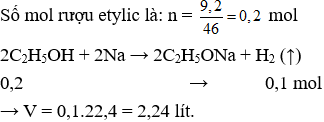
Câu 22. B
Na2O + H2O → 2NaOH
SO2 + H2O ⇄ H2SO3
Câu 23. C
R + Cl2 → RCl2
Bảo toàn khối lượng có: mclo = mmuối – mM = 27 – 12,8 = 14,2 gam
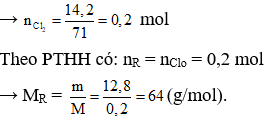
Vậy kim loại R là Cu.
Câu 24. B
Gọi công thức phân tử của X có dạng: CxHyOzNt
Ta có:
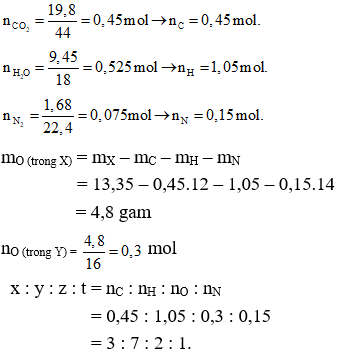
Vậy công thức đơn giản nhất của X là: (C3H7O2N)n
Khối lượng mol phân tử của X là 89 (g/mol) → 89n = 89 → n = 89.
Vậy công thức phân tử của X là C3H7O2N.
Câu 25. A
Đạm ure: CO(NH2)2.
Câu 26. C
Các phản ứng xảy ra:
2HCl + Na2CO3 → 2NaCl + CO2 (↑) + H2O
Ca(OH)2 + Na2CO3 → CaCO3 (↓) + 2NaOH
BaCl2 + Na2CO3 → BaCO3 (↓) + 2NaCl
Câu 27. B
3NaOH + FeCl3 → Fe(OH)3 (↓) + 3NaCl.
Câu 28. D
Ta có: 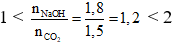
Vậy sau phản ứng thu được hai muối là NaHCO3 và Na2CO3.
Câu 29. B
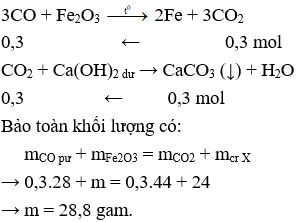
Câu 30. A
Phương pháp điều chế nhôm trong công nghiệp là điện phân nóng chảy Al2O3
Câu 31. A
Gọi số mol của Mg, Al và Fe lần lượt là x, y và z mol
Phần 1:
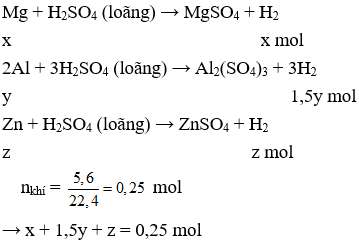
Phần 2:

Câu 32. B
A sai do C không phản ứng được với Al2O3.
C sai do O2 không phản ứng với Ca(OH)2
D sai do CO không phản ứng với Ca(OH)2.
Câu 33. D
CH4, C2H6, C2H2 là các hiđrocacbon.
Câu 34. A
Protein, tinh bột, xenlulozơ là các polime thiên nhiên.
Câu 35. B
2CH3COOH + 2K → 2CH2COOK + H2 (↑)
Câu 36. C
CO2, SO2: oxit axit.
BaO, Na2O: oxit bazơ.
CO: oxit trung tính.
Câu 37. A
Gọi số mol của Mg và Fe lần lượt là x và y (mol)
mhh = 8 gam → 24x + 56y = 8 (1)
PTHH:
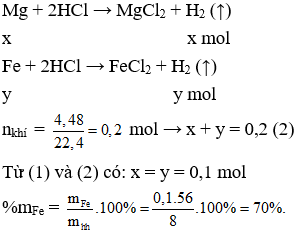
Câu 38. B
pH = 3 < 7 → dung dịch có môi trường axit.
Câu 39. D
Axetilen là chất khí ở điều kiện thường, có khả năng làm mất màu dung dịch nước brom, có tác dụng làm quả xanh mau chín.
Câu 40. A
B sai vì hai chất đều có 2 nguyên tử C, 6 nguyên tử H và 1 nguyên tử O.
C sai vì hai chất đều có khối lượng mol phân tử là 46.
D sai vì hai chất đều có công thức phân tử là C2H6O.
Xem thêm các Đề ôn thi vào lớp 10 môn Hóa học có đáp án hay khác:
- Đề thi vào lớp 10 môn Hóa học năm 2026 có đáp án (Trắc nghiệm - Đề 2)
- Đề thi vào lớp 10 môn Hóa học năm 2026 có đáp án (Trắc nghiệm - Đề 3)
- Đề thi vào lớp 10 môn Hóa học năm 2026 có đáp án (Trắc nghiệm - Đề 4)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Đề thi các môn học lớp 9 năm 2025 học kì 1 và học kì 2 được biên soạn bám sát cấu trúc ra đề thi mới Tự luận và Trắc nghiệm giúp bạn giành được điểm cao trong các bài thi lớp 9.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giáo án lớp 9 (các môn học)
- Giáo án điện tử lớp 9 (các môn học)
- Giáo án Toán 9
- Giáo án Ngữ văn 9
- Giáo án Tiếng Anh 9
- Giáo án Khoa học tự nhiên 9
- Giáo án Vật Lí 9
- Giáo án Hóa học 9
- Giáo án Sinh học 9
- Giáo án Địa Lí 9
- Giáo án Lịch Sử 9
- Giáo án GDCD 9
- Giáo án Tin học 9
- Giáo án Công nghệ 9
- Đề thi lớp 9 (các môn học)
- Đề thi Ngữ Văn 9 (có đáp án)
- Đề thi Toán 9 (có đáp án)
- Đề thi Tiếng Anh 9 mới (có đáp án)
- Đề thi Tiếng Anh 9 (có đáp án)
- Đề thi Khoa học tự nhiên 9 (có đáp án)
- Đề thi Lịch Sử và Địa Lí 9 (có đáp án)
- Đề thi GDCD 9 (có đáp án)
- Đề thi Tin học 9 (có đáp án)
- Đề thi Công nghệ 9 (có đáp án)






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

