Đề thi vào lớp 10 môn Hóa học năm 2026 có đáp án (Tự luận - Đề 2)
Đề thi vào lớp 10 môn Hóa học
Thời gian: 60 phút
Đề bài:
Câu I (2,0 điểm): Viết các phương trình hóa học thực hiện những chuyển đổi hóa học sau:
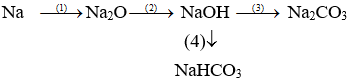
Câu II (2 điểm): Có 4 lọ đựng 4 chất bột màu trắng riêng biệt: NaCl, Na2CO3, CaCO3, BaSO4. Chỉ dùng H2O và dd HCl. Hãy phân biệt từng lọ. Viết phương trình hóa học?
Câu III (2 điểm): Nêu hiện tượng xảy ra, viết phương trình hóa học khi cho:
1) Na vào dd CuSO4.
2) Dây Cu vào dd AgNO3.
3) dd CH3COOH vào Cu(OH)2.
Câu IV (2 điểm): Hòa tan hoàn toàn 11 gam hỗn hợp bột các kim loại: Fe, Al cần V lít dd H2SO4 0,5 M thu được dd A và 8,96 lít H2 (đktc).
1) Viết PTHH xảy ra.
2) Tính phần trăm khối lượng của từng kim loại trong hỗn hợp ban đầu.
3) Tính nồng độ mol/lit của từng chất tan trong dd A (coi thể tích của dd không đổi).
Câu V (2 điểm): Đốt cháy hoàn toàn 12 gam chất hữu cơ X chứa các nguyên tố: C, H, O thu được 13,44 l CO2 (đktc) và 14,4 g H2O.
1) Hãy xác định công thức phân tử của X, biết khối lượng mol của X là 60 (g/mol).
2) Viết công thức cấu tạo của X, biết X có nhóm - OH.
(Cho biết: Al = 27 ; Fe = 56 ; C = 12 ; H = 1 ; O = 16 )
Đáp án & Thang điểm
Câu I
1) 4Na + O2 → 2Na2O
2) Na2O + H2O → 2NaOH
3) CO2 + 2NaOH (dư) → Na2CO3 + H2O
4) CO2 (dư) + NaOH → NaHCO3
Câu II.
- Đánh số thứ tự từng lọ mất nhãn.
- Hòa tan từng chất vào nước
+ Nếu chất rắn bị hòa tan → dd NaCl và dd Na2CO3 (nhóm I)
+ Nếu chất rắn không bị hòa tan → CaCO3 và BaSO4 (nhóm II)
- Phân biệt các dung dịch nhóm I: Dùng dung dịch HCl
+ Nếu có sủi bọt khí → Na2CO3
Na2CO3 + 2HCl → 2NaCl + CO2 (↑) + H2O
+ Nếu không có hiện tượng → NaCl
- Phân biệt nhóm II: Dùng dung dịch HCl
+ Nếu chất rắn tan dần, có khí thoát ra → CaCO3
CaCO3 (↓) + 2HCl → CaCl2 + CO2 (↑) + H2O
+ Nếu không có hiện tượng gì → BaSO4.
- Dán nhãn từng lọ.
Câu III
1) Hiện tượng: Có sủi bọt khí, mẩu Na tan dần, xuất hiện kết tủa xanh.
PTHH:
2Na + 2H2O → 2NaOH + H2 (↑)
CuSO4 + 2NaOH → Cu(OH)2 (↓ xanh) + Na2SO4.
2) Hiện tượng: Có chất rắn màu xám bám vào dây đồng. Dung dịch ban đầu không màu, sau phản ứng thu được dung dịch có màu xanh lam.
PTHH:

3) Hiện tượng: Cu(OH)2 tan dần tạo dung dịch.
PTHH:
Cu(OH)2 (r) + 2CH3COOH (dd) → (CH3COO)2Cu (dd) + 2H2O
Câu IV
1) PTHH:
2Al + 3H2SO4 (loãng) → Al2(SO4)3 + 3H2 (↑) (1)
Fe + H2SO4 (loãng) → FeSO4 + H2 (↑) (2)
2) Gọi số mol của Al và Fe lần lượt là x (mol) và y (mol)

Coi thể tích dung dịch thay đổi không đáng kể sau phản ứng.
Dung dịch A gồm Al2(SO4)3 và FeSO4
Theo PTHH (1) có:
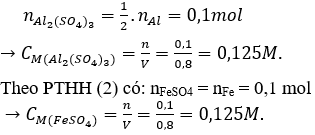
Câu V
1/ Gọi CTPT của X có dạng CxHyOz
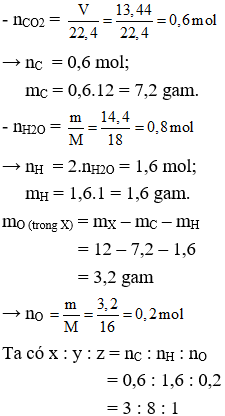
Vậy công thức đơn giản nhất của X là: (C3H8O)n
MX = 60 (g/mol) → 60n = 60 → n = 1.
Công thức phân tử của X là: C3H8O.
2/ X có nhóm – OH nên công thức cấu tạo của X là:
CH3 – CH2 – CH2 – OH hoặc 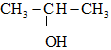
Xem thêm các Đề ôn thi vào lớp 10 môn Hóa học có đáp án hay khác:
- Đề thi vào lớp 10 môn Hóa học năm 2026 có đáp án (Tự luận - Đề 1)
- Đề thi vào lớp 10 môn Hóa học năm 2026 có đáp án (Tự luận - Đề 3)
- Đề thi vào lớp 10 môn Hóa học năm 2026 có đáp án (Tự luận - Đề 4)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Đề thi các môn học lớp 9 năm 2025 học kì 1 và học kì 2 được biên soạn bám sát cấu trúc ra đề thi mới Tự luận và Trắc nghiệm giúp bạn giành được điểm cao trong các bài thi lớp 9.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giáo án lớp 9 (các môn học)
- Giáo án điện tử lớp 9 (các môn học)
- Giáo án Toán 9
- Giáo án Ngữ văn 9
- Giáo án Tiếng Anh 9
- Giáo án Khoa học tự nhiên 9
- Giáo án Vật Lí 9
- Giáo án Hóa học 9
- Giáo án Sinh học 9
- Giáo án Địa Lí 9
- Giáo án Lịch Sử 9
- Giáo án GDCD 9
- Giáo án Tin học 9
- Giáo án Công nghệ 9
- Đề thi lớp 9 (các môn học)
- Đề thi Ngữ Văn 9 (có đáp án)
- Đề thi Toán 9 (có đáp án)
- Đề thi Tiếng Anh 9 mới (có đáp án)
- Đề thi Tiếng Anh 9 (có đáp án)
- Đề thi Khoa học tự nhiên 9 (có đáp án)
- Đề thi Lịch Sử và Địa Lí 9 (có đáp án)
- Đề thi GDCD 9 (có đáp án)
- Đề thi Tin học 9 (có đáp án)
- Đề thi Công nghệ 9 (có đáp án)






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

