Bài tập ôn tập Hóa học 10 Cánh diều Chủ đề 4 (có đúng sai, trả lời ngắn)
Bài tập ôn tập Hóa học 10 Cánh diều Chủ đề 4: Phản ứng oxi hóa – khử có đáp án chi tiết đầy đủ các mức độ sẽ giúp học sinh lớp 10 ôn luyện trắc nghiệm Hóa học 10.
Bài tập ôn tập Hóa học 10 Cánh diều Chủ đề 4 (có đúng sai, trả lời ngắn)
Chỉ từ 200k mua trọn bộ Bài tập ôn tập + Đề kiểm tra Hoá học 10 Cánh diều theo Chủ đề theo cấu trúc mới bản word có lời giải chi tiết, trình bày đẹp mắt, dễ dàng chỉnh sửa:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận đề thi
Phần I. Câu trắc nghiệm nhiều phương án lựa chọn.
Câu 1. Phản ứng oxi hóa – khử là
A. phản ứng hóa học giữa đơn chất và hợp chất, trong đó nguyên tử của đơn chất thay thế nguyên tử của một nguyên tố khác trong hợp chất.
B. phản ứng hóa học trong đó một chất sinh ra hai hay nhiều chất mới.
C. phản ứng hóa học trong đó có sự thay đổi số oxi hóa của ít nhất một nguyên tố hóa học.
D. phản ứng hóa học trong đó hai hay nhiều chất ban đầu sinh ra một chất mới.
Câu 2. Phát biểu nào sau đây là đúng khi nói về chất oxi hóa và chất khử?
A. Chất khử (chất bị oxi hóa) là chất nhường electron, chất oxi hóa (chất bị khử) là chất nhận electron.
B. Chất khử (chất bị oxi hóa) là chất nhận electron, chất oxi hóa (chất bị khử) là chất nhường electron.
C. Chất khử (chất bị oxi hóa) và chất oxi hóa (chất bị khử) đều là chất nhận electron.
D. Chất khử (chất bị oxi hóa) và chất oxi hóa (chất bị khử) đều là chất nhường electron.
Câu 3. Dấu hiệu để nhận biết một phản ứng oxi hóa - khử là
A. có sự thay đổi số oxi hóa của các nguyên tử.
B. có sự thay đổi trạng thái của chất phản ứng.
C. có xuất hiện hiện sản phẩm là chất khí.
D. có xuất hiện sản phẩm là chất kết tủa.
Câu 4. Số oxi hóa của Fe trong hợp chất Fe2O3 là
A. +2.
B. +3.
C. +4.
D. +6.
Câu 5. Số oxi hóa của C trong K2CO3 là
A. +2.
B. +4.
C. +6.
D. +8.
Câu 6. Số oxi hóa của S trong H2SO4 là
A. +4.
B. +6.
C. –2.
D. 0.
Câu 7. Số oxi hóa của N trong ion là
A. -3.
B. +2.
C. +4.
D. +5.
Câu 8. Số oxi hóa của N trong ion là
A. -3.
B. +2.
C. +4.
D. +5.
Câu 9. Phản ứng nào sau đây là phản ứng oxi hóa – khử?
A. CaCO3 CaO + CO2.
B. BaCl2 + Na2SO4 BaSO4↓ + 2NaCl.
C. NaOH + HCl NaCl + H2O.
D. 4Al + 3O2 2Al2O3.
Câu 10. Số oxi hóa của S trong hợp chất KAl(SO4)2 là
A. -2.
B. +2.
C. +4.
D. +6.
Câu 11. Số oxi hóa của Mn trong KMnO4 là
A. +1.
B. +3.
C. +5.
D. +7.
Câu 12. Số oxi hóa của nitrogen tăng dần trong dãy nào sau đây?
A. NH4Cl, N2, NO2, HNO3.
B. NH3, N2O, N2, NO.
C. NH4Cl, N2, NO2, NO.
D. NH3, HNO3, N2, N2O.
Câu 13. Trong phản ứng: CaO + CO2 → CaCO3, carbon dioxide đóng vai trò là
A. chất oxi hóa.
B. chất khử.
C. vừa là chất khử vừa là chất oxi hóa.
D. không bị oxi hóa cũng không bị khử.
Câu 14. Phương trình hóa học nào thể hiện tính oxi hóa của HCl?
A. Fe + 2HCl → FeCl2 + H2.
B. NaOH + HCl → NaCl + H2O.
C. Al2O3 + 6HCl → 2AlCl3 + 3H2O.
D. MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O.
Câu 15. Cho phương trình hóa học của phản ứng:
Cl2 + 2NaOH NaCl + NaClO + H2O
Trong phản ứng trên, Cl2 đóng vai trò
A. là chất oxi hóa.
B. là chất khử.
C. không là chất oxi hóa, không là chất khử
D. vừa là chất oxi hóa, vừa là chất khử.
Phần II. Câu trắc nghiệm đúng sai. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai. (Đ – S)
Câu hỏi. Cho các phản ứng sau:
(1) S + 2Na Na2S.
(2) S + 6HNO3 H2SO4 + 6NO2 + 2H2O.
(3) S + 3F2 SF6.
(4) 4S + 6NaOH(đặc) 2Na2S + Na2S2O3 + 3H2O.
a. Có 2 phản ứng trong các phản ứng trên S chỉ thể hiện tính khử.
b. Trong phản ứng (4), S vừa có tính khử vừa có tính oxi hóa.
c. Trong phản ứng (3), S thể hiện tính oxi hóa.
d. Trong phản ứng (1), S thể hiện tính khử.
Phần III: Câu hỏi trắc nghiệm yêu cầu trả lời ngắn.
Câu hỏi. Hòa tan hoàn toàn 6,5 gam Zn bằng dung dịch H2SO4 loãng, thu được V lít H2 (đkc). Giá trị của V là?
................................
................................
................................
Xem thêm bài tập ôn tập Hóa học lớp 10 Cánh diều có đáp án hay khác:
Bài tập ôn tập Hóa học 10 Cánh diều Chủ đề 1 (có đúng sai, trả lời ngắn)
Bài tập ôn tập Hóa học 10 Cánh diều Chủ đề 2 (có đúng sai, trả lời ngắn)
Bài tập ôn tập Hóa học 10 Cánh diều Chủ đề 3 (có đúng sai, trả lời ngắn)
Bài tập ôn tập Hóa học 10 Cánh diều Chủ đề 5 (có đúng sai, trả lời ngắn)
Bài tập ôn tập Hóa học 10 Cánh diều Chủ đề 6 (có đúng sai, trả lời ngắn)
Bài tập ôn tập Hóa học 10 Cánh diều Chủ đề 7 (có đúng sai, trả lời ngắn)
Xem thêm các tài liệu học tốt lớp 10 hay khác:
- Giải sgk Hóa học 10 Cánh diều
- Giải Chuyên đề Hóa học 10 Cánh diều
- Giải SBT Hóa học 10 Cánh diều
- Giải lớp 10 Cánh diều (các môn học)
- Giải lớp 10 Kết nối tri thức (các môn học)
- Giải lớp 10 Chân trời sáng tạo (các môn học)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Soạn văn 10 (hay nhất) - Cánh diều
- Soạn văn 10 (ngắn nhất) - Cánh diều
- Soạn văn 10 (siêu ngắn) - Cánh diều
- Giải sgk Toán 10 - Cánh diều
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Giải sgk Vật lí 10 - Cánh diều
- Giải sgk Hóa học 10 - Cánh diều
- Giải sgk Sinh học 10 - Cánh diều
- Giải sgk Địa lí 10 - Cánh diều
- Giải sgk Lịch sử 10 - Cánh diều
- Giải sgk Kinh tế và Pháp luật 10 - Cánh diều
- Giải sgk Tin học 10 - Cánh diều
- Giải sgk Công nghệ 10 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 10 - Cánh diều
- Giải sgk Giáo dục quốc phòng 10 - Cánh diều

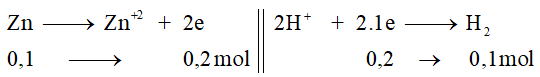





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

