Công thức thủy phân peptit (hay, chi tiết)
Bài viết Công thức thủy phân peptit hay nhất, chi tiết với bài tập minh họa có lời giải sẽ giúp học sinh nắm vững Công thức thủy phân peptit từ đó biết cách làm bài tập về thủy phân peptit.
Công thức thủy phân peptit (hay, chi tiết)
Các bài tập liên quan đến thủy phân peptit thường xuyên xuất hiện trong các đề kiểm tra và cũng là nỗi lo lắng của rất nhiều học sinh. Bài viết dưới đây sẽ giúp các em nắm rõ và giải quyết dễ dàng dạng bài tập này.
1. Công thức thủy phân n-peptit (với n là số mắt xích của peptit)
a) Thủy phân hoàn toàn trong môi trường trung tính (xúc tác enzim)
b) Thủy phân hoàn toàn trong môi trường axit
n-peptit + (n – 1)H2O + aHCl → n muối của ∝-amino acid
Trong đó: a là số nguyên tử N trong peptit
Ví dụ:
Gly-Gly-Lys + 2H2O + 4HCl → 2ClH3N-CH2-COOH + ClH3N-(CH2)4-CH(NH3Cl)-COOH
- Tỉ lệ mol:
- Định luật bảo toàn khối lượng:
m n-peptit + + mHCl = mmuối
- Bảo toàn gốc ∝-amino acid:
n một muối ∝-amino acid = (số lượng nhóm ∝-amino acid đó có mặt trong n-peptit).npepetit
c) Thủy phân hoàn toàn trong môi trường kiềm
n-peptit + (n - 1 + b)NaOH → n muối của ∝-amino acid + bH2O
Trong đó: b là tổng số nhóm -COOH còn tự do trong peptit (các nhóm COOH không tạo liên kết peptit)
Ví dụ:
Gly-Glu-Gly + 4NaOH → 2H2N-CH2-COONa + NaOOC-(CH2)2-CH(NH2)-COONa + 2H2O
- Tỉ lệ mol:
- Định luật bảo toàn khối lượng:
mpeptit + mNaOH = mmuối + mH2O
- Bảo toàn gốc ∝-amino acid:
n một muối ∝-amino acid = (số lượng nhóm ∝-amino acid đó có mặt trong n-peptit).npepetit
d) Thủy phân không hoàn toàn
Khi thủy phân không hoàn toàn peptit thu được hỗn hợp các amino acid và các oligopeptit.
Ví dụ: Thủy phân không hoàn toàn Ala-Gly-Gly-Ala-Glu ta có thể thu được hỗn hợp các chất gồm Ala, Glu, Gly, Gly-Ala- Glu, Ala-Gly-Gly, …
- Bảo toàn gốc ∝-amino acid:
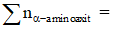
Ví dụ: Thủy phân hoàn toàn 12,3 gam một peptit X chỉ được tạo bởi một amino acid thu được 15 gam gly. X thuộc loại
A. dipeptide B. tripeptide C. tetrapeptide D. pentapeptit
Hướng dẫn giải
Sơ đồ phản ứng: n-peptit X + (n-1)H2O → ngly
Áp dụng định luật bảo toàn khối lượng:
m peptit + mH2O = m gly
→ 12,3 + 18. nH2O = 15
→ nH2O = 0,15 mol
Lập tỉ lệ mol:
→ n = 4
→ X là tetrapeptide (gly-gly-gly-gly)
→ Đáp án C

2. Bạn nên biết
Công thức tính phân tử khối của n-peptit
3. Bài tập minh họa thủy phân peptit
Câu 1: Thủy phân hoàn toàn m gam dipeptide gly-ala (mạch hở) bằng dung dịch KOH vừa đủ thu được dung dịch X. Cô cạn toàn bộ dung dịch X thu được 2,4 gam muối khan. Giá trị của m là
A. 1,46 B. 1,36 C. 1,64 D. 1,22
Hướng dẫn giải
Sơ đồ phản ứng:
gly-ala + 2KOH → Muối + 1H2O
Đặt số mol đipepti bằng x (mol)
Mgly-ala = 75 + 89 – 18(2 – 1) = 146 (g/mol)
Áp dụng định luật bảo toàn khối lượng:
m peptit + m KOH = m muối + mH2O
→ 146x + 56.2x = 2,4 + 18.x
→ x = 0,01 mol
→ m gly-ala = 0,01.146 = 1,46 gam
→ Đáp án A
Câu 2: Thủy phân hoàn toàn 14,6g Gly-Ala trong dung dịch HCl dư, thu được m gam muối. Giá trị của m là:
A. 11,15g B. 12,55g C. 18,6gam D. 23,7 gam.
Hướng dẫn giải:
Mgly-ala = 75 + 89 – 18(2 – 1) = 146 (g/mol)
Sơ đồ phản ứng:
Gly-ala + 1H2O + 2HCl → muối
Áp dụng định luật bảo toàn khối lượng:
m gly-ala + mH2O + m HCl = m muối
→ 14,6 + 18.0,1 + 36,5.0,2 = m muối
→ m muối = 23,7 gam
→ Đáp án D
Xem thêm các Công thức Hóa học lớp 12 quan trọng hay khác:
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)

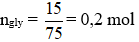
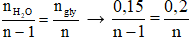
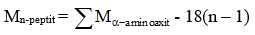
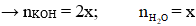
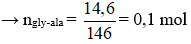
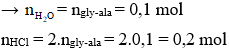





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

