C6H6 (Benzene) (Tính chất hóa học, vật lí, nhận biết, điều chế, ứng dụng)
Bài viết về tính chất hóa học của C6H6 (Benzene) gồm đầy đủ định nghĩa, công thức phân tử, công thức cấu tạo, tên gọi, tính chất hóa học, tính chất vật lí, cách điều chế và ứng dụng.
C6H6 (Benzene) (Tính chất hóa học, vật lí, nhận biết, điều chế, ứng dụng)
I. Định nghĩa benzene
- Định nghĩa:
benzene là chất lỏng, không màu, không tan trong nước, nhẹ hơn nước, hòa tan nhiều chất như: dầu ăn, nến, cao su, iot.... Benzene có mùi thơm nhẹ nhưng có hại cho sức khỏe.
- Công thức phân tử: C6H6.
- Công thức cấu tạo:
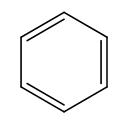
II. Tính chất vật lí của benzene và nhận biết
- benzene là chất lỏng, không màu, không tan trong nước, nhẹ hơn nước, hòa tan nhiều chất như: dầu ăn, nến, cao su, iot.... Benzene độc.
III. Tính chất hóa học của benzene
1. Phản ứng thế
a) Phản ứng halogen hóa
• Khi có bột sắt, benzene tác dụng với brom khan tạo thành brombenzen và khí hiđro bromua.
• Nếu không dùng sắt mà chiếu sáng (as) thì Brom thế cho hiđro ở nhánh.
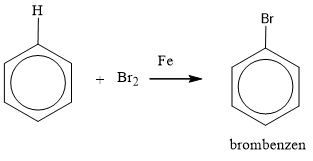
b) Phản ứng nitro hóa
benzene tác dụng với hỗn hợp HNO3 đặc và H2SO4 đậm đặc tạo thành nitrobenzen:
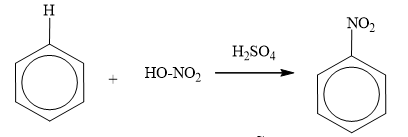
Nitro benzene tác dụng với hỗn hợp axit HNO3 bốc khói và H2SO4 đậm đặc đồng thời đun nóng thì tạo thành m-đinitrobenzen.
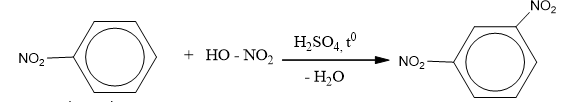
c) Quy tắc thế ở vòng benzene
Khi vòng benzene đã có sắn nhóm ankyl (hay các nhóm –OH, -NH2, -OCH3,...
Phản ứng thế vào vòng sẽ dễ dàng hơn và ưu tiên xảy ra ở vị trí nhóm ortho và para. Ngược lại, nếu ở vòng benzene đã có sẵn nhóm –NO2 (hoặc các nhóm –COOH, -SO3H, ...) phản ứng thế vào vòng sẽ khó hơn và ưu tiên xảy ra ở vị trí meta.
d) Cơ chế phản ứng thế ở vòng benzene
Phân tử halogen hoặc phân tử nitric acid không trực tiếp tấn công. Các tiểu phân mag điện tích dương tạo thành do tác dụng của chúng với xúc tác mới là tác nhân tấn công trực tiếp vào vòng benzene. Thí dụ:
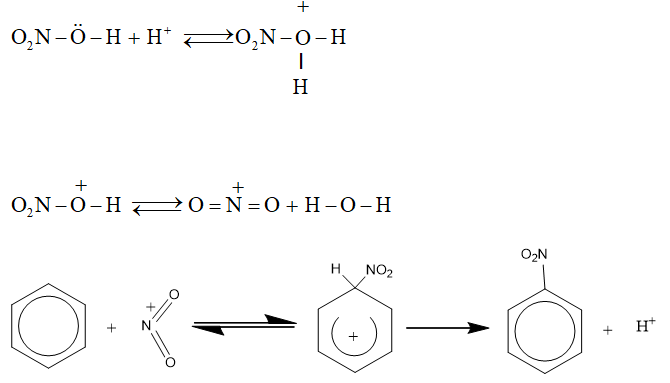
2. Phản ứng cộng
- benzene không tác dụng được với brom trong dung dịch, chứng tỏ benzene khó tham gia phản ứng cộng hơn Ethylene và acetylene. Tuy nhiên, trong điều kiện thích hợp, benzene có phản ứng cộng với một số chất:
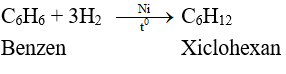
Do phân tử có cấu tạo đặc biệt nên benzene vừa có phản ứng thế vừa có phản ứng cộng. Tuy nhiên phản ứng cộng của benzene xảy ra khó hơn so với Ethylene và acetylene.
3. Phản ứng oxi hóa
• Benzen không tác dụng với KMnO4 (không làm mất màu dung dịch KMnO4).
• Cũng như các hydrocarbon khác, benzene cháy dễ tạo ra khí carbon dioxide và hơi nước.
C6H6 + O2 → 6CO2 + 3H2O
Tuy nhiên, khi benzene cháy trong không khí, ngoài carbon dioxide và hơi nước còn sinh ra muội than.
benzene tương đối dễ tham gia phản ứng thế, khó tham gia phản ứng cộng và bền vững các chất oxi hóa. Đây cũng là tính chất hóa học đặc trưng của hydrocarbon thơm nên được gọi là tính thơm.
IV. Điều chế benzene
- benzene thường được tách bằng cách chưng cất dầu mỏ và nhựa than đá. Chúng còn được điều chế từ alkane hoặc cycloalkane
CH3[CH2]4CH3 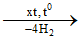
V. Ứng dụng của benzene
- benzene là nguyên liệu quan trọng nhất của công nghiệp hóa hữu cơ.
- benzene được dùng nhiều chất để tổng hợp các monome trong sản xuất polymer làm chất dẻo, cao su, tơ sợi (chẳng hạn poli styrene, cao su buna – styrene, tơ capron). Từ benzene người ta điều chế ra nitrobenzen, aniline, phenol để dùng tổng hợp phẩm nhuộm, dược phẩm, thuốc trừ dịch hại,...
- benzene được sử dụng làm dung môi trong công nghiệp và trong phòng thí nghiệm.
Xem thêm tính chất hóa học của các chất khác:
- Tính chất của Naphthalene
- Tính chất của styrene
- Tính chất của Phenol
- Tính chất của ethylic alcohol (C2H5OH)
- Tính chất của acetic acid
- Tính chất của Cellulose
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Wiki tính chất hóa học trình bày toàn bộ tính chất hóa học, vật lí, nhận biết, điều chế và ứng dụng của tất cả các đơn chất, hợp chất hóa học đã học trong chương trình Hóa học cấp 2, 3.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

