Amino acid (Tính chất hóa học, vật lí, nhận biết, điều chế, ứng dụng)
Bài viết về tính chất hóa học của amino acid gồm đầy đủ định nghĩa, công thức phân tử, công thức cấu tạo, tên gọi, tính chất hóa học, tính chất vật lí, cách điều chế và ứng dụng.
Amino acid (Tính chất hóa học, vật lí, nhận biết, điều chế, ứng dụng)
I. Định nghĩa amino acid
- Định nghĩa: amino acid là loại hợp chất hữu cơ tạp chức mà phân tử chứa đồng thời nhóm amino (NH2) và nhóm cacboxyl (COOH)–
- Công thức tổng quát: (H2N)x – R – (COOH)y
- Tên gọi:
+ Tên thay thế: axit + vị trí + amino + tên carboxylic acid tương ứng.
Ví dụ: H2N–CH2–COOH: aminoethanoic acid
+ Tên bán hệ thống: axit + vị trí (α, β, γ, δ, ε, ω) + amino + tên thông thường của carboxylic acid tương ứng.
Ví dụ: CH3–CH(NH2)–COOH: axit α-aminopropionic
+ Tên thường: các amino acid thiên nhiên (α-amino acid) đều có tên thường.
Ví dụ: H2N–CH2–COOH có tên thường là glycine (Gly) hay glicocol
II. Tính chất vật lí của amino acid và nhận biết
- Các amino acid là các chất rắn không màu, vị hơi ngọt, dễ tan trong nước vì chúng tồn tại ở dạng ion lưỡng cực (muối nội phân tử), nhiệt độ nóng chảy cao (vì là hợp chất ion)
III. Tính chất hóa học của amino acid
1. Tác dụng lên thuốc thử màu: (H2N)x – R – (COOH)y. Khi :
- x = y thì amino acid trung tính, quỳ tím không đổi màu
- x > y thì amino acid có tính bazơ, quỳ tím hóa xanh
- x < y thì amino acid có tính axit, quỳ tím hóa đỏ
2. Tính chất axit – bazơ của dung dịch amino acid :
- Tác dụng với dung dịch bazơ (do có nhóm COOH)
H2N–CH2–COOH + NaOH → H2N–CH2–COONa + H2O
- Tác dụng với dung dịch axit (do có nhóm NH2)
H2N–CH2–COOH + HCl → ClH3N–CH2–COOH
3. Phản ứng ester hóa nhóm COOH :
H2N-CH2-COOH + C2H5OH 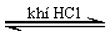
4. Phản ứng của nhóm NH2 với HNO2 :
H2N-CH2-COOH + HNO2 → HO-CH2-COOH + N2 + H2O
5. Phản ứng trùng ngưng :
- Do có nhóm NH2 và COOH nên amino acid tham gia phản ứng trùng ngưng tạo thành polymer thuộc loại poliamit
- Trong phản ứng này, OH của nhóm COOH ở phân tử axit này kết hợp với H của nhóm NH2 ở phân tử axit kia tạo thành nước và sinh ra polymer.
IV. Ứng dụng của amino acid
- amino acid thiên nhiên (hầu hết là α-amino acid) là cơ sở để kiến tạo nên các loại protein của cơ thể sống
- Muối mononatri của α-aminoglutaric acid được dùng làm mì chính (hay bột ngọt)
- Axit ε-aminocaproic và axit ω-aminoenantoic là nguyên liệu sản xuất tơ tổng hợp (nylon – 6 và nylon – 7)
- α-aminoglutaric acid là thuốc hỗ trợ thần kinh, methionin là thuốc bổ gan.
Xem thêm tính chất hóa học của các chất khác:
- Tính chất của Protein
- polyethylene (C2H4)n
- Poly (vinyl chloride) (C2H3Cl)n
- Poly (methyl methacrylate) (C5H8O2)n
- Poly butadiene (Cao su Buna) (C4H6)n
- Tính chất của Li (Lithium)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Wiki tính chất hóa học trình bày toàn bộ tính chất hóa học, vật lí, nhận biết, điều chế và ứng dụng của tất cả các đơn chất, hợp chất hóa học đã học trong chương trình Hóa học cấp 2, 3.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

