Pt (Platinum) (Tính chất hóa học, vật lí, nhận biết, điều chế, ứng dụng)
Bài viết về tính chất hóa học của Pt (Platinum) gồm đầy đủ thông tin cơ bản về Pt trong bảng tuần hoàn, tính chất hóa học, tính chất vật lí, cách điều chế và ứng dụng.
Pt (Platinum) (Tính chất hóa học, vật lí, nhận biết, điều chế, ứng dụng)
I. Định nghĩa Pt (Platinum)
- Platin là một kim loại được tìm thấy vào năm 1906. Tên Platin bắt nguồn từ thuật ngữ tiếng Tây Ban Nhaplatina del Pinto, nghĩa đen là "sắc hơi óng ánh bạc của sông Pinto".
- Kí hiệu: Pt
- Cấu hình electron: [Xe] 4f14 5d9 6s1
- Số hiệu nguyên tử: 78
- Khối lượng nguyên tử: 195 g/mol
- Vị trí trong bảng tuần hoàn
+ Ô: số 78
+ Nhóm: VIIIB
+ Chu kì: 6
- Đồng vị: 190Pt, 192Pt, 193Pt, 194Pt, 195Pt, 196Pt, 198Pt.
- Độ âm điện: 2,28
II. Tính chất vật lí của Pt (Platinum) & nhận biết
Tính chất vật lí:
- Kim loại quý, màu trắng - xám, tương đối mềm, rất dễ cán kéo, rèn được, khó nóng chảy.
- Pt có khối lượng riêng là 21,45 g/cm3; nhiệt độ nóng chảy là 17720C và nhiệt độ sôi là 38000C.
III. Tính chất hóa học của Pt (Platinum)
- Pt là kim loại kém hoạt động.
a. Tác dụng với phi kim
Khi nung nóng, Pt tác dụng được với phi kim có tính oxi hóa mạnh (như oxi, halogen,...)
b. Tác dụng với axit
Pt không tan trong axit, chỉ tan trong nước cường toan và HCl đặc có bão hòa clo.
3Pt + 18HCl (đặc) + 4HNO3 (đặc) → 3H2[PtCl6] + 4NO2 + 8H2O.
Pt + 2HCl(đặc, nóng) + 2Cl2 → H2[PtCl6]
IV. Trạng thái tự nhiên của Pt (Platinum)
- Platinum có sáu đồng vị tự nhiên: 190Pt, 192Pt, 194Pt,195Pt, 196Pt và 198Pt. Phổ biến nhất trong số này là 195Pt, chiếm tỉ lệ 33,83%. Đây là đồng vị ổn định duy nhất.
- Platin tự nhiên thường được tìm thấy ở dạng tinh khiết và hợp kim với Iridi như platiniridium. Phần lớn Platin tự nhiên được tìm thấy ở các lớp trầm tích đại trung sinh.
V. Điều chế Pt (Platinum)
- Khai thác từ tự nhiên.
VI. Ứng dụng của Pt (Platinum)
- Platin được sử dụng trong làm chất xúc tác, trang thiết bị phòng thí nghiệm, thiết bị điện báo, các điện cực, nhiệt kế điện trở bạch kim, thiết bị nha khoa, và đồ trang sức.
- Platin là một vật liệu khan hiếm, quý và rất có giá trị bởi vì sản lượng khai thác hằng năm chỉ tầm vài trăm tấn.
- Vì là một kim loại nặng, nó có ảnh hưởng không tốt đối với sức khỏe khi tiếp xúc với các muối của nó, nhưng do khả năng chống ăn mòn cho nên nó ít độc hại hơn so với các kim loại khác. Một số hợp chất của Platin, đặc biệt là cisplatin, được sử dụng để dùng trong hóa trị liệu chống lại một số loại ung thư.
VII. Các hợp chất quan trọng của Pt (Platinum)
- Axit hexachloroplatinic: (H3O)2PtCl6•nH2O
- Oxit Platin(IV): PtO2
Xem thêm tính chất hóa học của các chất khác:
- Tính chất của Cu (Copper) và hợp chất của Cu
- Tính chất của Ag (Silver) và hợp chất của Ag
- Tính chất của Au (Gold) và hợp chất của Au
- Tính chất của Zn (Zinc) và hợp chất của Zn
- Tính chất của Pb (Lead) và hợp chất của Pb
- Tính chất của Sn (Tin)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Wiki tính chất hóa học trình bày toàn bộ tính chất hóa học, vật lí, nhận biết, điều chế và ứng dụng của tất cả các đơn chất, hợp chất hóa học đã học trong chương trình Hóa học cấp 2, 3.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)

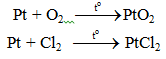





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

