Amine (Tính chất hóa học, vật lí, nhận biết, điều chế, ứng dụng)
Bài viết về tính chất hóa học của Amine gồm đầy đủ định nghĩa, công thức phân tử, công thức cấu tạo, tên gọi, tính chất hóa học, tính chất vật lí, cách điều chế và ứng dụng.
Amine (Tính chất hóa học, vật lí, nhận biết, điều chế, ứng dụng)
I. Định nghĩa Amine
- Định nghĩa: Amine là sản phẩm thu được khi thay thế một hay nhiều nguyên tử hiđro trong phân tử NH3 bằng một hay nhiều gốc hydrocarbon.
- Công thức tổng quát: CxHyNz hoặc CnH2n+2-2k+tNt
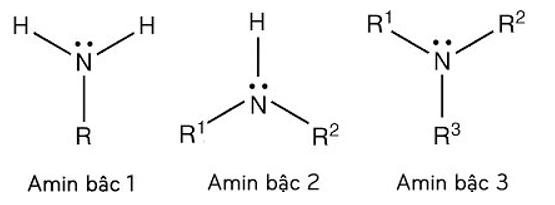
Tên gọi:
+ Tên thay thế: Tên hydrocarbon + vị trí + amine
Ví dụ: CH3NH2 (methamine)
+ Tên gốc chức: Tên gốc hydrocarbon + amine
Ví dụ: CH3NH2 (methylamine)
II. Tính chất vật lí của Amine và nhận biết
- Metyl–, dimethyl–, trimethyl– và ethylamine là những chất khí có mùi khai khó chịu, độc, dễ tan trong nước, các amine đồng đẳng cao hơn là chất lỏng hoặc rắn.
- aniline là chất lỏng, nhiệt độ sôi là 184°C, không màu, rất độc, ít tan trong nước, tan trong ancol và benzene.
III. Tính chất hóa học của Amine
1. Tính Bazơ :
Do nguyên tử N trong phân tử amine còn cặp e chưa sử dụng có khả năng nhận proton.
* So sánh tính bazơ của các amine:
+ Nếu nguyên tử N trong phân tử amine được gắn với gốc đẩy e (gốc no: ankyl) thì tính bazơ của amine mạnh hơn so với tính bazơ của NH3. Những amine này làm cho quỳ tím chuyển thành màu xanh.
+ Nếu nguyên tử N trong phân tử amine gắn với các gốc hút e (gốc không no, gốc thơm) thì tính bazơ của amine yếu hơn so với tính bazơ của NH3. Những amine này không làm xanh quỳ tím.
+ amine có càng nhiều gốc đẩy e thì tính bazơ càng mạnh, amine có càng nhiều gốc hút e thì tính bazơ càng yếu.
⇒ Lực bazơ: CnH2n + 1NH2 > HNH2 > C6H5NH2
2. Phản ứng với nitrous acid HNO2 :
- amine bậc một tác dụng với nitrous acid ở nhiệt độ thường cho ancol hoặc phenol và giải phóng nitơ.
C2H5NH2 + HONO → C2H5OH + N2↑ + H2O
- aniline và các amine thơm bậc một tác dụng với nitrous acid ở nhiệt độ thấp (0 - 5°C) cho muối điazoni:
C6H5NH2 + HONO + HCl → C6H5N2+Cl- + 2H2O
3. Phản ứng ankyl hóa :
- amine bậc một hoặc bậc hai tác dụng với ankyl halogenua (CH3I, …) , nguyên tử H của nhóm amine có thể bị thay thế bởi gốc ankyl:
Ví dụ: C2H5NH2 + CH3I → C2H5NHCH3 + HI
- Phản ứng này dùng để điều chế amine bậc cao từ amine bậc thấp hơn.
4. Phản ứng thế ở nhân thơm của aniline :
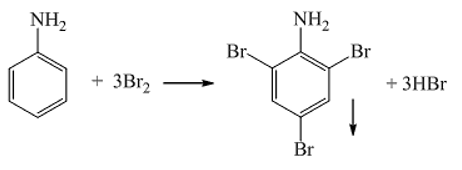
IV. Điều chế Amine
- Thay thế nguyên tử H của phân tử amonia:
NH3 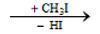
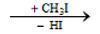
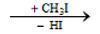
- Khử hợp chất nitro:
C6H5NO2 +6H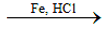 C6H5NH2 + 2H2O
C6H5NH2 + 2H2O
V. Ứng dụng của Amine
- Các ankylamin được dùng trong tổng hợp hữu cơ, đặc biệt là các điamin được dùng để tổng hợp polymer.
- aniline là nguyên liệu quan trọng trong công nghiệp phẩm nhuộm (phẩm azo, đen aniline,...), polymer (nhựa aniline - fomanđehit,...), dược phẩm (streptoxit, suafaguaniđin,...)
Xem thêm tính chất hóa học của các chất khác:
- Tính chất của Protein
- polyethylene (C2H4)n
- Poly (vinyl chloride) (C2H3Cl)n
- Poly (methyl methacrylate) (C5H8O2)n
- Poly butadiene (Cao su Buna) (C4H6)n
- Tính chất của Li (Lithium)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Wiki tính chất hóa học trình bày toàn bộ tính chất hóa học, vật lí, nhận biết, điều chế và ứng dụng của tất cả các đơn chất, hợp chất hóa học đã học trong chương trình Hóa học cấp 2, 3.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

