Phân tử khối của Lauric acid (chính xác nhất)
Phân tử khối của Lauric acid (công thức phân tử là: C12H24O2) có phân tử khối là 200. Bài viết dưới đây giúp bạn hiểu rõ hơn về cách tính phân tử khối của Lauric acid. Mời các bạn đón đọc.
Phân tử khối của Lauric acid (chính xác nhất)
1. Lauric acid là gì?
- Lauric acid là một axit béo no có nguồn gốc từ thực vật, đặc biệt phổ biến trong dầu dừa và dầu cọ. Lauric acid có công thức phân tử là C12H24O2.
- Lauric acid thường được sử dụng trong sản xuất xà phòng, mỹ phẩm và một số sản phẩm chăm sóc cá nhân.
- Lauric acid có phân tử khối M = 200.
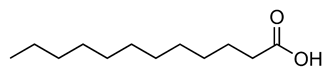
- Công thức cấu tạo của lauric acid là:
2. Cách tính phân tử khối của lauric acid
- Phân tử khối của lauric acid: Kí hiệu là
- Cách tính phân tử khối của lauric acid:
= 12.MC + 24.MH + 2.MO = 12.12 + 24.1 + 2.16 = 200.
3. Phân tử khối là gì?
- Phân tử khối là khối lượng tương đối của một phân tử.
- Phân tử khối của một chất bằng tổng nguyên tử khối của các nguyên tử trong phân tử chất đó.
Ví dụ:
Phân tử khối của khí nitrogen (N2) bằng: 14.2 = 28.
Phân tử khối của đường (C12H22O11) bằng: 12.12 + 1.22 + 16.11 = 342.
4. Bài tập minh họa
Câu 1: Công thức phân tử của lauric acid là
A. C10H20O2.
B. C12H22O2.
C. C12H24O2.
D. C14H28O2.
Lời giải:
Đáp án đúng là: C
Câu 2: Lauric acid thuộc loại hợp chất nào sau đây?
A. ester.
B. acid béo no.
C. acid béo không no.
D. lipid.
Lời giải:
Đáp án đúng là: B
Câu 3: Lauric acid có phân tử khối là
A. 186.
B. 198.
C. 200.
D. 214.
Lời giải:
Đáp án đúng là: C
Xem thêm phân tử khối của các chất hóa học hay khác:
- Phân tử khối của Adipic acid
- Phân tử khối của Fusidic acid
- Phân tử khối của C2H2Br4
- Phân tử khối của 1-chloropropane
- Phân tử khối của Vinyl chloride
- Phân tử khối của Benzyl bromide
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Wiki tính chất hóa học trình bày toàn bộ tính chất hóa học, vật lí, nhận biết, điều chế và ứng dụng của tất cả các đơn chất, hợp chất hóa học đã học trong chương trình Hóa học cấp 2, 3.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

