Ba (Barium) (Tính chất hóa học, vật lí, nhận biết, điều chế, ứng dụng)
Bài viết về tính chất hóa học của Ba (Barium) gồm đầy đủ thông tin cơ bản về Ba trong bảng tuần hoàn, tính chất hóa học, tính chất vật lí, cách điều chế và ứng dụng.
Ba (Barium) (Tính chất hóa học, vật lí, nhận biết, điều chế, ứng dụng)
I. Định nghĩa Ba (Barium)
- Bari là kim loại kiềm thổ được Carl Scheele nhận biết lần đầu tiên vào năm 1774.
- Kí hiệu: Ba
- Cấu hình electron: [Xe] 6s1
- Số hiệu nguyên tử: 56
- Khối lượng nguyên tử: 137 g/mol
- Vị trí trong bảng tuần hoàn
+ Ô: số 56
+ Nhóm: IIA
+ Chu kì: 6
- Đồng vị: 130Ba, 132Ba, 134Ba, 135Ba, 136Ba, 137Ba, 138Ba
- Độ âm điện: 0,89
II. Tính chất vật lí của Ba (Barium) & nhận biết
1. Tính chất vật lí:
- Bari là kim loại kiềm thổ màu trắng bạc, dẻo, rèn được.
- Có khối lượng riêng là 3,6 g/cm3; có nhiệt độ nóng chảy là 7270C và sôi ở 18600C.
2. Nhận biết
- Đốt cháy các hợp chất của Ba, cho ngọn lửa màu đỏ son.
III. Tính chất hóa học của Ba (Barium)
- Bari là kim loại kiềm thổ có tính khử mạnh.
Ba → Ba2+ + 2e
a. Tác dụng với phi kim (oxi, halogen….)
2Ba + O2 → 2BaO
Ba + Cl2 →BaCl2
b. Tác dụng với axit
- Với dung dịch axit HCl:
Ba + 2HCl → BaCl2 + H2
- Với dung dịch HNO3:
Ba + 4HNO3 đặc → Ba(NO3)2 + 2NO2 + 2H2O.
Lưu ý: Kim loại Ba dễ dàng phản ứng với hầu hết axit, với ngoại lệ là axit sunfuric, phản ứng dừng lại khi tạo thành lớp muối không tan trên bề mặt là bari sulfat.
c. Tác dụng với nước
- Ở nhiệt độ thường, Ba khử nước mãnh liệt.
Ba + 2H2O → Ba(OH)2 + H2
IV. Trạng thái tự nhiên của Ba (Barium)
- Bari trong tự nhiên là hỗn hợp của 7 đồng vị bền, đồng vị phổ biến nhất là 138Ba (71,7 %).
- Bari chiếm 0,0425% trong vỏ Trái Đất và 13 µg/L trong nước biển. Nó có mặt trong các khoáng barit (ở dạng sulphat) và witherit (ở dạng carbonate).
V. Điều chế Ba (Barium)
- Bari được sản xuất thương mại bằng phương pháp điện phân nóng chảy Barium chloride (BaCl2).
- Ba còn được điều chế bằng cách trộn barium oxide với bột nhôm nghiền mịn ở nhiệt độ giữa 1100 và 1200 °C
3BaO + 2 Al → 3Ba + Al2O3
VI. Ứng dụng của Ba (Barium)
- Bari được sử dụng chủ yếu trong sản xuất buji, ống chân không, pháo hoa và bóng đèn huỳnh quang.
+ Hợp chất bari sulfat có màu trắng và được sử dụng trong sản xuất sơn, trong chẩn đoán bằng tia X, và trong sản xuất thủy tinh.
+ Barium carbonate được dùng làm bả chuột và có thể được sử dụng trong sản xuất thủy tinh và gạch.
+ Barium nitrate và Barium chloride được sử dụng để tạo màu xanh lá cây trong sản xuất pháo hoa.
+ Bari sulfua không tinh khiết phát lân quang sau khi đặt dưới ánh sáng.
+ Các muối của bari, đặc biệt là bari sulfat, có khi cũng được sử dụng để uống hoặc bơm vào ruột bệnh nhân, để làm tăng độ tương phản của những tấm phim X quang trong việc chẩn đoán hệ tiêu hóa.
VII. Các hợp chất quan trọng của Ba (Barium)
- Bari peoxit: Ba2O2
- Barium chloride: BaCl2
- Bari sunfat: BaSO4
- Barium carbonate: BaCO3
- Barium nitrate: Ba(NO3)2
Xem thêm tính chất hóa học của các chất khác:
- Tính chất của Ba(OH)2 (Barium hydroxide)
- Tính chất của Ba(NO3)2 (Barium nitrate)
- Tính chất của BaCl2 (Barium chloride)
- Tính chất của BaCO3 (Barium carbonate)
- Tính chất của BaO (Barium oxide)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Wiki tính chất hóa học trình bày toàn bộ tính chất hóa học, vật lí, nhận biết, điều chế và ứng dụng của tất cả các đơn chất, hợp chất hóa học đã học trong chương trình Hóa học cấp 2, 3.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)

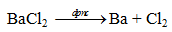





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

