Đề thi tuyển sinh Hóa học vào lớp 10 trường Chuyên Phan Bội Châu (Nghệ An) năm 2025
Bài viết cập nhật Đề thi Hóa học vào lớp 10 trường Chuyên Phan Bội Châu, Nghệ An năm 2025 giúp học sinh nắm được cấu trúc đề thi và có thêm tài liệu ôn thi vào lớp 10 môn Hóa học.
Đề thi tuyển sinh Hóa học vào lớp 10 trường Chuyên Phan Bội Châu (Nghệ An) năm 2025
Chỉ từ 450k mua trọn bộ Đề thi vào 10 chuyên Hóa theo cấu trúc mới bản word có lời giải chi tiết, trình bày đẹp mắt, dễ dàng chỉnh sửa:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận đề thi
|
SỞ GIÁO DỤC VÀ ĐÀO TẠO NGHỆ AN ĐỀ CHINH THỨC (Đề thi gồm 04 trang)
|
KỲ THI TUYỂN SINH LỚP 10 TRƯỜNG THPT PHAN BỘI CHÂU NĂM HỌC 2025-2025 MÔN THI: KHOA HỌC TỰ NHIÊN (Dùng cho thí sinh thi vào lớp chuyên Hóa học) Thời gian làm bài: 150 phút (không kể thời gian giao đề) |
Câu I. (4 điểm)
1. Hợp chất T được tạo ra từ 3 nguyên tử của 2 nguyên tố X và Y. Tổng số hạt mang điện trong hạt nhân của các nguyên tử trong phân tử T là 22. Ở trạng thái cơ bản, nguyên tử nguyên tố X có electron phân bố trên 2 lớp, lớp thứ 2 có 4 electron.
a) Xác định công thức hóa học của T.
b) Khi cho sợi Mg nung nóng vào bình chứa khí T, thấy sợi Mg cháy thu được oxide M và đơn chất X. Mô tả sự tạo thành liên kết trong phân tử T và M.
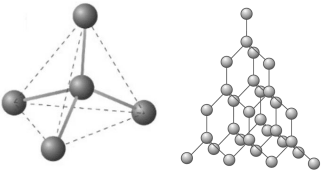
2. Sodium fluoride (NaF) và carbon (C) được sử dụng trong nhiều ứng dụng công nghệ vật liệu khác nhau. Dựa vào đặc điểm liên kết hóa học, giải thích các tính chất sau của NaF và kim cương (một dạng thù hình của carbon).
Cấu trúc tính thể kim cương
a) NaF bền với nhiệt, có độ tan cao trong nước và dẫn điện khi tan trong nước.
b) Kim cương có độ cứng rất cao, không tan trong nước và không dẫn điện.
3. Để kiểm chứng giả thuyết “tăng nồng độ chất tham gia phản ứng làm tăng tốc độ phản ứng”, hai học sinh A, B tiến hành các thí nghiệm và quan sát được hiện tượng như bảng sau:
|
Học sinh A |
Học sinh B |
||
|
Thí nghiệm (TN) |
Hiện tượng |
Thí nghiệm (TN) |
Hiện tượng |
|
TN1: Cho x gam một lá Zn vào dung dịch HCl 1M |
Thoát ra khí không màu |
TN1: Cho y gam một lá Cu vào dung dịch HNO3 loãng |
Thoát ra khí không màu (NO) |
|
TN2: Cho x gam một lá Zn vào dung dịch HC12M |
Thoát ra khí không màu
|
TN2: Cho y gam một lá Cu vào dung dịch HNO3 đặc |
Thoát ra khí màu nâu đỏ (NO2) |
a) Viết phương trình hóa học của các phản ứng xảy ra trong mỗi thí nghiệm trên.
b) Trong thí nghiệm trên, hai học sinh A, B đều thấy khí thoát ra ở thí nghiệm 2 nhanh hơn ở thí nghiệm 1. Bằng thí nghiệm của mình, mỗi học sinh A, B đã chứng minh được giả thuyết trên hay chưa? Vì sao?
Câu II. (4 điểm)
1. Trong phòng thí nghiệm có 5 lọ hóa chất được đánh số thứ tự từ (1) đến (5), mỗi lọ chứa một trong các dung dịch sau: (NH4)2SO4,, Na2SO4, Ba(OH)2, K2CO3, HCl. Một học sinh tiến hành thí nghiệm với dung dịch ở 5 lọ, thu được kết quả như sau:
- Cho dung dịch ở lọ (2) tác dụng với dung dịch ở lọ (3) thấy có kết tủa trắng và khí thoát ra.
- Cho dung dịch ở lọ (2) tác dụng với dung dịch ở lọ (1) hoặc dung dịch ở lọ (4) đều thấy xuất hiện kết tủa.
- Cho dung dịch ở lọ (4) tác dụng với dung dịch ở lọ (5) thấy có khí thoát ra.
Hãy xác định dung dịch có trong mỗi lọ và viết phương trình hóa học của các phản ứng xảy ra.
2. Phân hỗn hợp NPK được sản xuất chủ yếu bằng cách phối trộn các loại phân đơn chứa các nguyên tố dinh dưỡng là N, P và K. Tùy thuộc vào loại cây trồng và loại đất có thể sử dụng phân NPK có tỷ lệ chất dinh dưỡng khác nhau đặc trưng bằng tỷ lệ N: P2O5 : K2O. Một nhà máy sản xuất 100 kg phân NPK (20 – 15 – 15) bằng cách phối trộn 98 kg hỗn hợp các loại phân DAP (chứa (NH4)HPO4 (16 – 48 – 0)), SA (chứa (NH4)2SO4, có độ dinh dưỡng 21%), urea (có độ dinh dưỡng 46%), kali (chứa KCl, có độ dinh dưỡng 60%) và 2 kg là hỗn hợp các chất chống kết dính, chất chống vón cục và các phụ gia. Tính khối lượng urea để sản xuất 100 kg phân NPK (20 – 15 – 15) trên.
3. Khí X có trong thành phần của không khí và đóng vai trò quan trọng trong quá trình sinh hóa của các dạng sống. Đốt cháy một dải Mg trong khí X thu được hỗn hợp bột màu xám gồm hợp chất T (màu trắng) và đơn chất M (màu đen). Đốt cháy M trong khí oxygen dư thu được khí X. Khi đốt cháy dải Mg trong khí Y (là một khí khác có trong không khí) sinh ra chất rắn H (màu trắng). Khi cho H tác dụng với nước sinh ra một chất khí Z có mùi khai nồng đặc trưng. Trong công nghiệp, X tác dụng với Z trong điều thích hợp sinh ra G là một loại phân bón hóa học. Xác định các chất X, Y, Z, T, M, H, G và viết phương trình hóa học của các phản ứng xảy ra.
Câu III. (4 điểm)
1. Cho giá trị nhiệt độ sôi của 6 alkane như sau:
|
Alkane |
Methane CH4 |
Ethane C2H6 |
Propane C3H8 |
Butane C4H10 |
Pentane C5H12 |
Hexane C6H14 |
|
Nhiệt độ sôi (°C) |
-161,5 |
-88,6 |
-42,1 |
-0,5 |
36,1 |
68,7 |
a) Ở 25 °C và dưới áp suất khí quyển, những alkane nào tồn tại thể khí?
b) Bên trong một chiếc bật lửa gas là chất lỏng trong suốt có thành phần chính là butane. Vì sao butane bên trong bật lửa lại không sôi?
c) Hãy giải thích tại sao không được để các bình chứa gas (có thành phần chính là propane và butane) gần lửa, trong khi đó người ta có thể nấu chảy nhựa đường (trong thành phần cũng có các alkane) để làm đường giao thông.
d) Một trong những ứng dụng quan trọng của hexane được sử dụng để tách dầu thô, chất béo từ các loại hạt như đậu nành, hướng dương… trong quy trình chiết xuất. Hãy cho biết ứng dụng trên dựa vào tính chất nào của hexane? Giải thích.
2. Trong phòng thí nghiệm, điều chế ethyl acetate được tiến hành theo các bước sau:
Bước 1: Cho khoảng 2 mL C2H5OH và 2 mL CH3COOH vào ống nghiệm, lắc đều hỗn hợp.
Bước 2: Thêm khoảng 1 mL dung dịch H2SO4 đặc, lắc nhẹ để các chất trộn đều với nhau.
Bước 3: Đặt ống nghiệm vào cốc nước nóng (khoảng 60 °C – 70 °C) trong khoảng 5 phút, thỉnh thoảng lắc đều hỗn hợp. Sau đó lấy ống nghiệm ra khỏi cốc nước nóng, để nguội hỗn hợp, rồi rót hỗn hợp chất lỏng sang ống nghiệm khác chứa 5 mL dung dịch muối ăn bão hòa thì thấy chất lỏng trong ống nghiệm tách thành hai lớp và có mùi thơm nhẹ.
Cho một số tính chất vật lí của các chất như sau:
|
Chất |
Khối lượng riêng & 25 °C (g.mL) |
Độ tan ở 25 °C (g/100g nước) |
Nhiệt độ sôi (°C) |
|
H₂O |
1,000 |
|
100,000 |
|
C2H5OH |
0,789 |
Tan vô hạn |
78,300 |
|
CH3COOH |
1,050 |
Tan vô hạn |
118,000 |
|
CH3COOC2H5 |
0,900 |
9,700 |
77,100 |
|
Dung dịch NaCl bão hòa |
1,200 |
36,000 |
|
a) Dựa vào dấu hiệu nào để khẳng định có phản ứng hóa học xảy ra. Viết phương trình hóa học của phản ứng.
b) Nêu vai trò của dung dịch H2SO4 đặc và dung dịch NaCl bão hòa.
c) Hãy cho biết thành phần các chất có trong mỗi lớp sau bước 3?
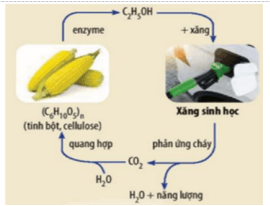
3. Xăng sinh học (gasohol hay biogasoline) được tạo ra bằng cách phối trộn ethanol (C2H5OH) với xăng thông thường theo một tỷ lệ nhất định. Ví dụ xăng E5 RON 92 (gồm 5% ethanol và 95% xăng RON 92 về thể tích). Từ tinh bột (có trong các loại ngũ cốc như ngô, lúa mì, đậu tương...) có thể chuyển hóa thành ethanol và việc sử dụng ethanol trong xăng sinh học diễn ra theo chu trình khép kín (như hình bên) giúp giảm thải khí CO2, góp phần bảo vệ môi trường. sinh học.
a) Viết phương trình hóa học của các phản ứng xảy ra chu trình khép kín của ethanol trong xăng
b) Một loại xăng E5 có tỉ lệ số mol như sau: 5% C2H5OH, 7,5% C7H16, 87,5% C8H18. Khi được đốt hoàn toàn, 1 mol C2H5OH sinh ra năng lượng 1367 kJ, 1 mol C7H16 sinh ra năng lượng 4825 kJ và 1 mol C8H18 sinh ra năng lượng 5460 kJ, năng lượng giải phóng ra có 20% thải vào môi trườg. Trung bình một xe máy chạy 1 giờ cần một năng lượng 36500 kJ. Tính khối lượng xăng E5 cần sử dụng cho xe máy nói trên chạy được 2 giờ.
Câu IV. (4 điểm)
1. Ở nước ta hiện nay, nhiệt điện vẫn chiếm vai trò nòng cốt, cung cấp hơn 60% tổng năng lượng điện cho đời sống và sản xuất. Có hai công nghệ sản xuất nhiệt điện là nhiệt điện khí và nhiệt điện than. Một nhà máy nhiệt điện X sử dụng than đá làm nhiên liệu có sản lượng điện 2.106 kW/ngày (1 kW = 3600 kJ).
Trong than đá chứa 2% sulfur (ở dạng vô cơ và hữu cơ như FeS2, CaSO4, CxHySH...) về khối lượng, có 80% sulfur bị đốt cháy tạo thành SO2. Khí thải SO2 của nhà máy nhiệt điện được xử lý bằng cách cho lội qua dung dịch với sữa (dung dịch huyền phủ calcium hydroxide). Vôi sữa hấp thụ 90% lượng khí SO2 theo phương trình hóa học sau:
2SO2 + O2 + 2Ca(OH)2 →2CaSO4 + 2H₂O
Sau đó CaSO4 được lọc tách, làm sạch, nung khô và thu hồi dưới dạng thạch cao thương phẩm (2CaSO4.H2O) với hiệu suất 80%. Biết năng lượng khi đốt cháy 1 kg than đá là 30000 kJ và chỉ có 50% lượng nhiệt tỏa ra của quá trình đốt cháy hoàn toàn than đá được chuyển hóa thành điện năng.
a) Tính khối lượng 2CaSO4.H2O thu được và tính khối lượng SO2 phát thải ra không khí trong 30 ngày.
b) Theo Quy chuẩn kỹ thuật của Việt Nam về lượng khí thải trong công nghiệp nhiệt điện khi phát thải vào môi trường không khí, nồng độ tối đa cho phép các thông số của ô nhiễm khí thải trong công nghiệp ở 25°C và áp suất 760 mmHg, được tính bằng công thức sau:
Cmax = C. Kp. Kv
Trong đó:
Cmax: nồng độ tối đa cho phép của các thông số ô nhiễm khí thải công nghiệp (mg/m3)
C: nồng độ làm cơ sở tính toán nồng độ của các thông số ô nhiễm tối đa cho phép (mg/m3)
Kp: hệ số công suất thiết kế của nhà máy nhiệt điện
Kv: hệ số phân vùng, khu vực
|
Thông số |
Nồng độ C (mg/m3) |
|
Than |
|
|
Sulfur dioxide (SO2) |
500 |
Nhà máy nhiệt điện X có hệ số công suất thiết kế Kp =0,85. Hệ số Kv trong hai khu vực như sau:
|
Khu vực |
Hệ số Kv |
|
|
Loại 1 |
Đô thị đặc biệt, đô thị loại I, di sản thiên nhiên, di tích lịch sử, văn hóa được xếp hạng. Khoảng cách của nhà máy đến ranh giới của khu vực này là 5 km. |
Kv =0,6 |
|
Loại 2 |
Các khu vực khác. Khoảng cách của nhà máy đến ranh giới của khu vực này là 5 km. |
Kv =0,8 |
- Tính nồng độ tối đa cho phép (mg/m3) của các thông số ô nhiễm khí thải công nghiệp của nhà máy nhiệt điện X trong hai khu vực trên.
- Khi phân tích 40 lít không khí của Thành phố Y (đô thị loại I) nằm gần nhà máy nhiệt điện X người ta thấy có chứa lượng SO2 bằng 1,875.10-4 mol. Hỏi không khí ở Thành phố Y có bị ô nhiễm không? Giải thích.
c) Em hãy đề xuất các biện pháp hạn chế ô nhiễm không khi do nhà máy nhiệt điện gây ra.
2. Trong nước thải của một nhà máy sản xuất phân đạm có chứa NH4Cl với hàm lượng 550 mg/L. Để xử lý NH4Cl về nồng độ cho phép không quá 15 mg/L (theo quy chuẩn Việt Nam), người ta tiến hành xử lý nước thải theo phương pháp Anammox (Anaerobic Ammonium Oxidation), đây là một phương pháp nhờ sự tác động của vi sinh vật, thời gian xử lý 2 tuần. Phương pháp này gồm 2 giai đoạn:
Giai đoạn 1: Thêm NaHCO3 (dùng dư 10% so với lượng cần thiết) vào nước thải rồi liên tục sục không khí vào, khi đó NH4Cl sẽ phản ứng với NaHCO3 và O2 tạo ra NaNO2 đồng thời giải phóng CO2.
Giai đoạn 2: Diễn ra trong điều kiện yếm khí, NH4Cl sẽ được oxi hóa trực tiếp thành khi nitrogen bằng NaNO2 vừa tạo ra.
a) Viết phương trình hóa học của các phản ứng xảy ra.
b) Một bể nước thải dung tích 3000 m3 được xử lí theo phương pháp này, không khí được sục liên tục một cách phân tán đều, chỉ 15% O2 được sục vào tham gia quá trình xử lí (O2 chiếm 20,95% thể tích không khí). Sau 2 tuần nước thải đạt tiêu chuẩn cho phép.
- Tính khối lượng tối thiểu NaHCO3 đã dùng.
- Tính lưu lượng không khí (ở điều kiện chuẩn) được sục vào bể (m3/h).
Câu V. (4 điểm)
1. Quả chanh được sử dụng phổ biến để làm gia vị trong các bữa ăn. Trong nước cốt chanh có chứa hợp chất hữu cơ, mạch hở X. Kết quả phân tích thành phần nguyên tố trong X có 4,167% hydrogen; 37,500% carbon theo khối lượng, còn lại là oxygen. Khối lượng phân tử của X bằng 192 amu. Phân tử chất X có chứa 2 nhóm methylene (CH2) và có cấu trúc đối xứng. Khi cho a mol X tác dụng với với NaHCO3 dư, tạo ra tối đa 3a mol khí. Mặt khác, nếu lấy a mol X tác dụng với kim loại Na dư, tạo ra tối đa 2a mol khí. Xác định công thức phân tử, công thức cấu tạo của X và viết phương trình hóa học của các phản ứng xảy ra ở trên.
2. Trong thực tế, thành phần chất béo gồm các triglyceride (RCOO)3C3H5 và có lẫn một ít acid béo tự do RCOOH (trong đó R là gốc hydrocarbon của acid béo). Để đánh giá chất lượng của chất béo người ta sử dụng các chỉ số chất lượng, trong đó có chỉ số acid và chỉ số xà phòng hóa. Các chỉ số này được định nghĩa như sau:
- Chỉ số acid của chất béo là số miligam KOH cần dùng để trung hòa acid béo tự do có trong 1 gam chất béo.
- Chỉ số xà phòng hóa là số miligam KOH cần để xà phòng hóa 1 gam chất béo.
Theo TCVN 6126:2015 (tương đương với ISO 3657:2020), chỉ số acid và chỉ số xà phòng hóa trung bình của chất béo trong mỡ bò lần lượt là 6 là 196. Một cơ sở cần sản xuất 10000 bánh xà phòng, mỗi bánh xà phòng có khối lượng 90 gam (chứa 72% khối lượng muối sodium của các acid béo) bằng cách xà phòng hóa m kg mỡ bò (chứa 96% khối lượng là chất béo) nói trên với dung dịch NaOH. Biết trong quá trình sản xuất, lượng xà phòng bị hao hụt 4%.
a) Viết phương trình hóa học ở dạng tổng quát của các phản ứng xảy ra.
b) Tính giá trị của m.
……………… HẾT ………………
Xem thêm Đề thi tuyển sinh vào lớp 10 môn Hóa học năm 2025 trên cả nước khác:
Đề thi tuyển sinh Hóa học vào lớp 10 năm 2025 trường Chuyên Lam Sơn (Thanh Hóa)
Đề thi tuyển sinh Hóa học vào lớp 10 năm 2025 trường Chuyên Lai Châu
Đề thi tuyển sinh Hóa học vào lớp 10 năm 2025 trường Chuyên Khoa học - Huế
Đề thi tuyển sinh Hóa học vào lớp 10 năm 2025 trường Chuyên Bắc Ninh
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Đề thi các môn học lớp 9 năm 2025 học kì 1 và học kì 2 được biên soạn bám sát cấu trúc ra đề thi mới Tự luận và Trắc nghiệm giúp bạn giành được điểm cao trong các bài thi lớp 9.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giáo án lớp 9 (các môn học)
- Giáo án điện tử lớp 9 (các môn học)
- Giáo án Toán 9
- Giáo án Ngữ văn 9
- Giáo án Tiếng Anh 9
- Giáo án Khoa học tự nhiên 9
- Giáo án Vật Lí 9
- Giáo án Hóa học 9
- Giáo án Sinh học 9
- Giáo án Địa Lí 9
- Giáo án Lịch Sử 9
- Giáo án GDCD 9
- Giáo án Tin học 9
- Giáo án Công nghệ 9
- Đề thi lớp 9 (các môn học)
- Đề thi Ngữ Văn 9 (có đáp án)
- Đề thi Toán 9 (có đáp án)
- Đề thi Tiếng Anh 9 mới (có đáp án)
- Đề thi Tiếng Anh 9 (có đáp án)
- Đề thi Khoa học tự nhiên 9 (có đáp án)
- Đề thi Lịch Sử và Địa Lí 9 (có đáp án)
- Đề thi GDCD 9 (có đáp án)
- Đề thi Tin học 9 (có đáp án)
- Đề thi Công nghệ 9 (có đáp án)






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

