Giáo án Hóa học 8 Bài 16: Phương trình hóa học mới nhất
Giáo án Hóa học 8 Bài 16: Phương trình hóa học mới nhất
Xem thử Giáo án KHTN 8 KNTT Xem thử Giáo án KHTN 8 CTST Xem thử Giáo án KHTN 8 CD
Chỉ từ 500k mua trọn bộ Kế hoạch bài dạy (KHBD) hay Giáo án KHTN 8 cả năm (mỗi bộ sách) bản word chuẩn kiến thức, trình bày đẹp mắt, dễ dàng chỉnh sửa:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận giáo án
I. MỤC TIÊU:
1. Kiến thức :
Học sinh biết được:
-Phương trình hóa học biểu diễn phản ứng hóa học.
-Các bước lập PTHH.
-Ý nghĩa của PTHH: Cho biết các chất phản ứng và các chất sản phẩm, tỷ lệ số phân tử, số nguyên tử giữa các chất trong phản ứng.
2. Kĩ năng :
-Biết lập PTHH khi biết các chất tham gia và các chất sản phẩm.
-Xác định được ý nghĩa của một số PTHH cụ thể.
3. Thái độ : Kiên trì trong học tập và yêu thích bộ môn.
4. Năng lực cần hướng tới :
-Năng lực sử dụng ngôn ngữ hóa học.
-Năng lực sáng tạo
-Năng lực hợp tác
II. TRỌNG TÂM:
-Cách lập PTHH.
-Ý nghĩa của PTHH và vận dụng ĐLBTKL vào các PTHH đã lập.
III. CHUẨN BỊ:
1. Giáo viên :
- Hình 2.5(sgk/48). Bảng phụ ghi đề bài tập vận dụng.
- Phiếu học tập.
2. Học sinh :
Ôn lại nội dung định luật BTKL, lập CTHH, viết PT chữ.
IV. TIẾN TRÌNH BÀI GIẢNG:
| GIÁO VIÊN | HỌC SINH | NỘI DUNG |
|---|---|---|
|
Hoạt động 1: Khởi động (2 phút) Theo định luật bảo toàn khối lượng, số nguyên tử của mỗi nguyên tố trong các chất trước và sau phản ứng được giữ nguyên. Dựa vào đó cùng với CTHH ta sẽ lập được PTHH để biểu diễn ngắn gọn phản ứng hoá học. Đây là nội dung của buổi học hôm nay. |
||
Hoạt động 2: Hình thành kiến thức (28 phút) |
||
Hoạt động 2.1. Tìm hiểu về phương trình hoá học (8 phút) |
||
|
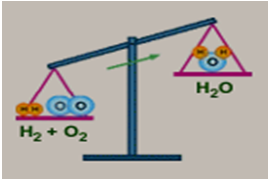
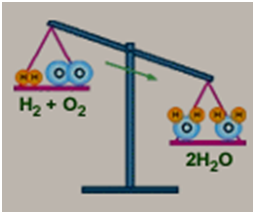
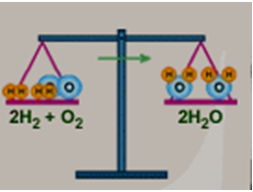
- GV treo Hình: 2.5 → Hãy viết PT chữ khi cho khí hiđro tác dụng với oxi tạo thành nước? - Hãy thay các chất trong PT bằng CTHH? - GV nhận xét, uốn nắn sai sót của HS khi viết CTHH. - GV treo hình vẽ như SGK/55. Hãy quan sát chiếc cân 1 và cho biết vì sao cân không thăng bằng? GV hướng dẫn: Để cân bằng số nguyên tử O ở 2 vế ta thêm hệ số 2 trước công thức H2O. - GV chỉ lên chiếc cân 2 → Chiếc cân 2 vẫn chưa thăng bằng, vì sao? - Làm thế nào để số nguyên tử H ở 2 vế bằng nhau? - Cân 3 đã thăng bằng, vì sao? - GV nhận xét → PTHH. Lưu ý: Khi số nguyên tử của các nguyên tố ở 2 vế bằng nhau, ta thay ( ) bằng dấu (→). - Hãy đọc PTHH vừa lập? - Từ bài tập 3/54(bài cũ), đã có PT chữ: Magie + Oxi Hãy lập PTHH? - GV hướng dẫn: Từ PT chữ → viết dưới dạng CTHH? Cân bằng số nguyên tử của nguyên tố không bằng nhau ở 2 vế → lập PTHH? - GV nhận xét, chấm bài 1 số HS (phát hiện ra lỗi sai của HS để kịp thời sửa chữa). Chuyển ý : Làm thế nào để lập được PTHH? ta sang phần 2 |
- 1 HS lên bảng viết, HS khác viết vào vở. - HS lần lượt thay thế. - Vì số nguyên tử Oxi ở vế trái nhiều hơn vế phải. - HS cân bằng số nguyên tử O theo hướng dẫn. - Vì số nguyên tử H ở vế phải nhiều hơn vế trái. - Thêm hệ số 2 trước công thức H2. - Vì số nguyên tử H, O ở 2 vế bằng nhau. - 2 phân tử Hiđro tác dụng với 1 phân tử Oxi tạo thành 2 phân tử nước. - HS lập PTHH vào vở theo từng bước: + Viết PT dạng CTHH. + Cân bằng số nguyên tử O bằng cách thêm hệ số 2 trước MgO → O ở 2 vế bằng nhau. + Thêm hệ số 2 trước Mg → số nguyên tử Mg ở 2 vế bằng nhau. + Viết thành PTHH. |
I. Lập phương trình hoá học. 1. Phương trình hoá học VD1: Hiđro + oxi → nước. H2 + O2 → H2O H2 + O2 - - -> 2 H2O 2 H2 + O2 - - - > 2 H2O PTHH: 2 H2 + O2 VD2: PT chữ: Magie + Oxi Magie oxit Mg + O2 Mg + O2 2 Mg + O2 - PTHH: 2 Mg + O2 |
Hoạt động 2.2. Các bước lập phương trình hóa học (20 phút) |
||
|
?Qua 2 ví dụ trên, hãy thảo luận nhóm nhỏ rút ra các bước lập phương trình hoá học ? - GV gọi đại diện nhóm trình bày ý kiến . ?Viết sơ đồ phản ứng là viết gì ? - GV lưu ý: Khi viết CTHH của các chất không được viết sai CTHH, không viết thiếu chất, muốn viết đúng CTHH hợp chất phải nhớ hoá trị của nguyên tố hay nhóm nguyên tử . ?Cân bằng số nguyên tử của mỗi nguyên tố là ta làm gì ? - GV lưu ý : Ở bước này, khi chọn hệ số, hệ số phải được viết ngang bằng kí hiệu hóa học, không được thay đổi chỉ số nguyên tử . ?Viết PTHH là làm gì ? - GV đưa ví dụ lên bảng : VD1 : Lập PTHH của phản ứng sau: Nhôm + khí oxi → Nhôm oxit * Thảo luận nhóm lập PTHH của phản ứng hóa học trên? GV:Trong phản ứng hóa học, để cân bằng số nguyên tử thường bắt đầu từ nguyên tố có số nguyên tử nhiều hơn và không bằng nhau. Trường hợp một số nguyên tố có số nguyên tử một bên là chẵn, một bên là lẻ, ta nên làm chẵn số nguyên tử lẻ bằng đặt hệ số 2 trước CTHH có chứa nguyên tố có số nguyên tử lẻ. - GV hướng dẫn: Trong phản ứng trên, cả số nguyên tử Al và O ở 2 vế là không bằng nhau . Ta nên bắt đầu từ nguyên tố O có số nguyên nhiều hơn, làm chẵn số nguyên tử O ở vế phải. ?Lúc này bên trái cần có mấy nguyên tử O và Al? ?Do đó ta cần làm gì ? - GV lưu ý : Vì số oxi ở dạng phân tử O2, không được viết 6O, không được thay đổi chỉ số trong CTHH viết đúng . Ví dụ 2 : Lập phương trình hóa học của phản ứng: Na2CO3 + Ca(OH)2 --> CaCO3 + NaOH ?Nhận xét số nguyên tử của nguyên tố và số nhóm nguyên tử ở 2 vế như thế nào? ?Do đó, để cân bằng ta phải làm gì ? - GV nhấn mạnh : Tuy nhiên, trường hợp số nhóm nguyên tử bị phá vỡ sau phản ứng thì khi cân bằng ta cần đếm số nguyên tử của mỗi nguyên tố . - GV đưa ra ví dụ : VD : Al(OH)3 --> Al2O3 + H2O → Hướng dẫn HS hoàn thành PTHH . |
Có 3 bước lập PTHH : 1/ Viết sơ đồ phản ứng 2/ Cân bằng số nguyên tử của mỗi nguyên tố . 3/ Viết thành PTHH -Là viết CTHH của các chất tham gia phản ứng và sản phẩm - HS ghi nhận - Chọn hệ số thích hợp đặt trước CTHH sao cho số nguyên tử của mỗi nguyên tố ở 2 vế là bằng nhau . - HS ghi nhận Nối mũi tên rời thành mũi tên liền . - HS ghi đề bài vào vở . - HS thảo luận nhóm, làm vào bảng phụ . - HS tiếp nhận thông tin kiến thức . - HS lĩnh hội 4Al và 6O Đặt hệ số 4 Al và 3O2 - HS chú ý - HS viết ví dụ vào vở + Vế trái : 2Na, 2 (OH) + Vế phải : 1Na, 1 (OH) còn số Ca, và CO3 ở 2 vế là bằng nhau . -->Do đó, ta đặt 2 trước CTHH NaOH . - HS lĩnh hội kiến thức . - HS ghi ví dụ vào vở . |
2.Các bước lập phương trình hoá học. -Bước 1: Viết sơ đồ phản ứng. -Bước 2: Cân bằng số nguyên tử của mỗi nguyên tố. -Bước 3: Viết PTHH VD1 : Al + O2 ---> Al2O3 4Al + 3O2 ---> 2Al2O3 4Al + 3O2 VD 2 : Na2CO3 + Ca(OH)2 --> CaCO3 + NaOH Na2CO3 + Ca(OH)2 --> CaCO3 + 2NaOH Na2CO3 + Ca(OH)2 |
|
Hoạt động 3: Củng cố, luyện tập (5 phút) -Nhắc lại các bước lập phương trình hoá học? -Khi cân bằng PTHH ta chỉ được thêm hệ số hay thay đổi chỉ số? -Nhận biết PTHH đã được cân bằng hay chưa dựa và dấu mũi tên ntn? |
||
|
Hoạt động 4: Vận dụng (5 phút) -Cân bằng các phương trình hoá học sau: 1. Al + Cl2 --------> AlCl3 2. Al + O2 ---------> Al2O3 3. Al(OH)3 --------> Al2O3 + H2O |
||
|
Hoạt động 5: Tìm tòi, mở rộng (5 phút) -BTVN: 2,3,4,5,7 sgk trang 55,56. -Chuẩn bị trước phần còn lại. -Học thuộc các bước lập PTHH. |
||
V. RÚT KINH NGHIỆM:
Xem thử Giáo án KHTN 8 KNTT Xem thử Giáo án KHTN 8 CTST Xem thử Giáo án KHTN 8 CD
Xem thêm các bài soạn Giáo án Hóa học lớp 8 theo hướng phát triển năng lực mới nhất, hay khác:
- Giáo án Hóa học 8 Bài 16: Phương trình hóa học (Tiết 2)
- Giáo án Hóa học 8 Bài 17: Bài luyện tập 3
- Giáo án Hóa học 8 Bài 18: Mol
- Giáo án Hóa học 8 Bài 19: Chuyển đổi giữa khối lượng, thể tích và lượng chất
- Giáo án Hóa học 8 Bài 19: Chuyển đổi giữa khối lượng, thể tích và lượng chất (Tiết 2)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Giáo án Hóa học lớp 8 mới, chuẩn nhất của chúng tôi được biên soạn bám sát nội dung sgk Hóa học 8 theo chuẩn Giáo án của Bộ GD & ĐT.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giáo án lớp 8 (các môn học)
- Giáo án điện tử lớp 8 (các môn học)
- Giáo án Toán 8
- Giáo án Ngữ văn 8
- Giáo án Tiếng Anh 8
- Giáo án Khoa học tự nhiên 8
- Giáo án KHTN 8
- Giáo án Lịch Sử 8
- Giáo án Địa Lí 8
- Giáo án GDCD 8
- Giáo án HĐTN 8
- Giáo án Tin học 8
- Giáo án Công nghệ 8
- Giáo án Vật Lí 8
- Giáo án Hóa học 8
- Giáo án Sinh học 8
- Đề thi lớp 8 (các môn học)
- Đề thi Ngữ Văn 8 (có đáp án)
- Chuyên đề Tiếng Việt lớp 8
- Đề thi Toán 8
- Đề cương ôn tập Toán 8
- Đề thi Tiếng Anh 8 (có đáp án)
- Đề thi Tiếng Anh 8 mới (có đáp án)
- Đề thi Khoa học tự nhiên 8 (có đáp án)
- Đề thi Lịch Sử và Địa Lí 8 (có đáp án)
- Đề thi GDCD 8 (có đáp án)
- Đề thi Tin học 8 (có đáp án)
- Đề thi Công nghệ 8 (có đáp án)

 Magie oxit(MgO)
Magie oxit(MgO) MgO
MgO




 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

