KOH + CO2 → K2CO3 + H2O | KOH + CO2 tỉ lệ 2:1
Phản ứng KOH + CO2 (tỉ lệ 2 : 1) ra K2CO3 thuộc loại phản ứng trao đổi đã được cân bằng chính xác và chi tiết nhất. Bên cạnh đó là một số bài tập có liên quan về KOH có lời giải, mời các bạn đón xem:
2KOH + CO2 → K2CO3 + H2O
1. Phương trình phản ứng CO2 tác dụng với KOH
CO2 + 2KOH → K2CO3 + H2O
2. Cách tiến hành phản ứng CO2 tác dụng với KOH
- Dẫn khí CO2 từ từ đến dư vào ống nghiệm chứa KOH và vài giọt chất chỉ thị.
3. Cách viết phương trình ion thu gọn của phản ứng CO2 tác dụng với KOH
Bước 1: Viết phương trình phân tử:
CO2 + 2KOH → K2CO3 + H2O
Bước 2: Viết phương trình ion đầy đủ bằng cách: chuyển các chất vừa dễ tan, vừa điện li mạnh thành ion; các chất điện li yếu, chất kết tủa, chất khí để nguyên dưới dạng phân tử:
CO2 + 2K+ + 2OH- → 2K+ + CO32- + H2O
Bước 3: Viết phương trình ion thu gọn từ phương trình ion đầy đủ bằng cách lược bỏ đi các ion giống nhau ở cả hai vế:
CO2 + 2OH- → CO32- + H2O
4. Xác định sản phẩm của phản ứng CO2 tác dụng với KOH
- CO2 phản ứng với KOH chỉ thu được muối KHCO3 khi T = .
- CO2 phản ứng với KOH chỉ thu được muối K2CO3 khi T = .
- CO2 phản ứng với KOH thu được cả muối KHCO3 và K2CO3 khi 1< T = < 2.
5. Mở rộng kiến thức về CO2
5.1. Cấu tạo phân tử
- Cấu tạo của CO2 là O = C = O.
- Phân tử CO2 có cấu tạo thẳng, không phân cực.
5.2. Tính chất vật lý
- Là chất khí không màu, nặng gấp 1,5 lần không khí.
- Tan ít trong nước.
- CO2 khi bị làm lạnh đột ngột chuyển sang trạng thái rắn, gọi là nước đá khô.
- Nước đá khô không nóng chảy mà thăng hoa nên được dùng để làm môi trường lạnh và khô, rất tiện lợi để bảo quản thực phẩm.
Lưu ý: Khi sử dụng đá khô phải đeo gang tay chống lạnh để tránh bị bỏng lạnh khi tiếp xúc với đá khô.
5.3. Tính chất hóa học
- Khí CO2 không cháy, không duy trì sự cháy của nhiều chất.
- CO2 là acidic oxide, khi tan trong nước tạo thành carbonic acid:
CO2 (k) + H2O (l) ⇄ H2CO3 (dd)
- Ngoài ra, CO2 còn tác dụng với basic oxide và dung dịch kiềm.
Thí dụ:
CaO + CO2 CaCO3
NaOH + CO2 → NaHCO3
2NaOH + CO2 → Na2CO3 + H2O
5.4. Điều chế
a. Trong phòng thí nghiệm
- CO2 được điều chế bằng cách cho dung dịch HCl tác dụng với đá vôi.
- Phương trình hóa học:
CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O
b. Trong công nghiệp
- Khí CO2 được thu hồi từ quá trình đốt cháy hoàn toàn than để cung cấp năng lượng cho các quá trình sản xuất khác.
C + O2 CO2
- Ngoài ra, khí CO2 còn được thu hồi từ quá trình chuyển hóa khí thiên nhiên, các sản phẩm dầu mỏ; quá trình nung vôi; quá trình lên men rượu từ đường glucose.
CaCO3 CaO + CO2
C6H12O6 2CO2 + 2C2H5OH
6. Bài tập vận dụng liên quan
Câu 1: Nung 13,4g hỗn hợp muối carbonate của hai kim loại hóa trị II. Sau khi phản ứng xảy ra hoàn toàn thu được 6,8g chất rắn và khí X. Lượng khí X sinh ra cho hấp thụ vào 75 ml dung dịch NaOH 1M. Khối lượng muối khan thu được sau phản ứng là:
A. 4,2g.
B. 5,8g.
C. 6,3g.
D. 6,5g.
Hướng dẫn giải:
Đáp án C
Gọi công thức chung của hai muối carbonate là RCO3.
RCO3 RO + CO2↑
→ Tạo muối axit, NaOH hết.
CO2 + NaOH → NaHCO3
→ nmuối = nNaOH = 0,075 mol
→ mmuối = 0,075.84 = 6,3 gam
Câu 2:Sục 1,12 lít CO2 (đktc) vào 200ml dung dịch Ba(OH)2 0,2M. Khối lượng kết tủa thu được là:
A. 5,91g.
B. 19,7g.
C. 78,8g.
D. 98,5g.
Hướng dẫn giải:
Đáp án A
→ Tạo hỗn hợp 2 muối.
Câu 3: Chất khí nào sau đây, được tạo ra từ bình chữa cháy và dùng để sản xuất thuốc giảm đau dạ dày?
A. CO2.
B. N2.
C. CO.
D. CH4.
Hướng dẫn giải:
Đáp án A
Chất khí được tạo ra từ bình chữa cháy là CO2.
Thuốc giảm đau dạ dày là NaHCO3.
NaOH + CO2 → NaHCO3.
Câu 4:Cho dãy các chất sau: CO2, CO, SiO2, NaHCO3, NH4Cl. Số chất trong dãy tác dụng với dung dịch NaOH loãng ở nhiệt độ thường là:
A. 2.
B. 3.
C. 4.
D. 5.
Hướng dẫn giải:
Đáp án B
Các chất thỏa mãn là CO2, NaHCO3 và NH4Cl.
CO2 + 2NaOH → Na2CO3 + H2O
NaHCO3 + NaOH → Na2CO3 + H2O
NH4Cl + NaOH → NH3↑ + NaCl + H2O
Chú ý: SiO2 chỉ phản ứng với dung NaOH đặc nóng hoặc NaOH nóng chảy.
Câu 5: Cho 5,6 lít CO2 (đktc) đi qua 164ml dung dịch NaOH 20% (d = 1,22g/ml) thu được dung dịch X. Cô cạn dung dịch X thì thu được khối lượng chất rắn là:
A. 15,5g.
B. 26,5g.
C. 31g.
D. 46,5g.
Hướng dẫn giải:
Đáp án D
→ NaOH dư
→ Chất rắn gồm NaOH dư và muối Na2CO3.
Bảo toàn nguyên tố C:
Bảo toàn nguyên tố Na:
nNaOH dư = 1 – 0,25.2 = 0,5 mol
→ mchất rắn = 0,25.106 + 0,5.40 = 46,5 gam
Câu 6: Hấp thụ hoàn toàn 0,16 mol CO2 vào 2 lít dung dịch Ca(OH)2 0,05M được kết tủa X và dung dịch Y. Khi đó khối lượng dung dịch Y so với khối lượng dung dịch Ca(OH)2 ban đầu sẽ là:
A. tăng 3,04g.
B. tăng 7,04g.
C. giảm 3,04g.
D. giảm 7,04g.
Hướng dẫn giải:
Đáp án A
→ Dung dịch Y chỉ có muối Ca(HCO3)2 và kết tủa X là CaCO3
→ Dung dịch sau phản ứng tăng 3,04 gam.
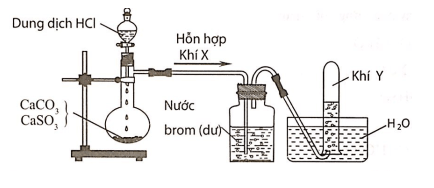
Câu 7:Hình vẽ sau đây mô tả thí nghiệm điều chế và thu khí Y từ hỗn hợp rắn gồm CaCO3 và CaSO3:
Khí Y là
A. CO2.
B. SO2.
C. H2.
D. Cl2.
Hướng dẫn giải:
Đáp án A
Hỗn hợp khí X gồm CO2 và SO2. Khí SO2 khi đi qua bình đựng nước brom đã bị giữ lại, còn khí Y thoát ra là CO2.
Câu 8:Dẫn từ từ CO2 đến dư vào dung dịch Ca(OH)2, hiện tượng quan sát được là
A. có kết tủa, lượng kết tủa tăng dần, kết tủa không tan.
B. không có hiện tượng gì trong suốt quá trình thực hiện.
C. lúc đầu không thấy hiện tượng, sau đó có kết tủa xuất hiện.
D. có kết tủa, lượng kết tủa tăng dần, sau đó kết tủa tan.
Hướng dẫn giải:
Đáp án D
Dẫn từ từ CO2 đến dư vào dung dịch Ca(OH)2 xảy ra phản ứng:
CO2 + Ca(OH)2 → CaCO3 + H2O
CO2 + CaCO3 + H2O → Ca(HCO3)2
Hiện tượng quan sát được: Dung dịch xuất hiện kết tủa trắng tăng dần đến cực đại, sau đó kết tủa tan dần đến hết.
Câu 9: “Nước đá khô” không nóng chảy mà dễ thăng hoa nên được dùng để tạo môi trường lạnh và khô, rất tiện cho việc bảo quản thực phẩm. “Nước đá khô” là
A. SO2 rắn.
B. CO2 rắn.
C. CO rắn.
D. H2O rắn.
Hướng dẫn giải:
Đáp án B
Nước đá khô là CO2 rắn.
Câu 10: Hấp thụ hoàn toàn 1,568 lít CO2 (đktc) vào 500 ml dung dịch NaOH 0,16M thu được dung dịch X. Thêm 250 ml dung dịch Y gồm BaCl2 0,16M và Ba(OH)2 aM vào dung dịch X thu được 3,94g kết tủa và dung dịch Z. Giá trị của a là:
A. 0,015.
B. 0,02.
C. 0,03.
D. 0,04.
Hướng dẫn giải:
Đáp án B
Nhận thấy:
→ Dung dịch Z chứa
Bảo toàn nguyên tố C:
Câu 11: Hấp thụ toàn bộ 0,3 mol CO2 vào dung dịch chứa 0,25 mol Ca(OH)2. Khối lượng dung dịch sau phản ứng tăng hay giảm bao nhiêu gam?
A. tăng 13,2g.
B. tăng 20g.
C. giảm 6,8g.
D. giảm 16,8g.
Hướng dẫn giải:
Đáp án C
Ta có:
→ Sau phản ứng thu được hai muối CaCO3 và Ca(HCO3)2
→ Khối lượng dung dịch sau phản ứng giảm 6,8 gam.
Câu 12:Cho 3,36 lít khí CO2 (đktc) vào dung dịch chứa 500 ml KOH 0,1M và Ba(OH)2 0,12M kết thúc phản ứng thu được m gam kết tủa. Giá trị của m là
A. 2,55.
B. 3,94.
C. 1,97.
D. 4,925.
Hướng dẫn giải:
Đáp án B
Câu 13:Cho 10 gam CaCO3 vào dung dịch HCl dư, sau khi phản ứng xảy ra hoàn toàn thu được V lít CO2 (đktc). Giá trị của V là
A. 2,80.
B. 2,24.
C. 1,12.
D. 3,36.
Hướng dẫn giải:
Đáp án B
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Bảo toàn nguyên tố C ta có:
lít
Câu 14:Cho khí CO2 vào lượng dư dung dịch nào sau đây sẽ tạo kết tủa?
A.MgCl2.
B. Ca(OH)2.
C. Ca(HCO3)2.
D.NaOH.
Hướng dẫn giải:
Đáp ánB
A và C không phản ứng → loại.
D. CO2 + 2NaOHdư → Na2CO3 + H2O → loại.
B. CO2 + Ca(OH)2 dư → CaCO3↓ + H2O
Câu 15: Cho 8,96 lít CO2 (đktc) sục vào dung dịch chứa 100 ml dung dịch chứa hỗn hợp Ca(OH)2 2M và NaOH 1,5M thu được a gam kết tủa và dung dịch X. Đun nóng kĩ dung dịch X thu được thêm b gam kết tủa. Giá trị (a + b) là
A. 5 gam
B. 15 gam
C. 20 gam
D. 40 gam
Hướng dẫn giải:
Đáp ánC
Theo bài → dung dịch X gồm các ion
→ dung dịch X
Bảo toàn điện tích →
Câu 16:Cho 5,6 lít CO2 (đktc) tan hết trong 200ml dung dịch NaOH nồng độ a M; dung dịch thu được có khả năng tác dụng tối đa 100 ml dung dịch KOH 1M. Giá trị của a là:
A. 0,75.
B. 1,5.
C. 2.
D. 2,5.
Hướng dẫn giải:
Đáp ánC
Câu 17: “Hiệu ứng nhà kính” là hiện tượng Trái Đất ấm dần lên do các bức xạ có bước sóng dài trong vùng hồng ngoại bị khí quyển giữ lại mà không bức xạ ra ngoài vũ trụ. Khí nào dưới đây là nguyên nhân chính gây ra hiệu ứng nhà kính?
A. CO2
B. CFC
C. SO2
D. NO2
Hướng dẫn giải:
Đáp án A
CH4, CO2 là nguyên nhân gây ra hiệu ứng nhà kính.
Câu 18: CO2 không cháy và không duy trì sự cháy nhiều chất nên được dùng để dập tắt các đám cháy. Tuy nhiên, CO2 không dùng để dập tắt đám cháy nào dưới đây?
A. đám cháy do xăng, dầu.
B. đám cháy nhà cửa, quần áo.
C. đám cháy do magie hoặc nhôm.
D. đám cháy do khí ga.
Hướng dẫn giải:
Đáp án C
Các kim loại mạnh như Mg, Al,..có thể cháy trong khí CO2
2Mg + CO2 2MgO + C
4Al + 3CO2 2Al2O3 + 3C
Do đó không dùng CO2 để dập tắt đám cháy do Mg, Al.
Xem thêm các phương trình hóa học hay khác:
- KOH + CO2 → KHCO3
- 2KOH + SO2 → K2SO3 + H2O
- KOH + SO2 → KHSO3
- KOH + HCl → KCl + H2O
- KOH + HNO3 → KNO3 + H2O
- 2KOH + H2SO4 → K2SO4+ 2H2O
- 2KOH + CuSO4 → K2SO4+ Cu(OH)2
- 2KOH + FeSO4 → K2SO4+ Fe(OH)2
- 3KOH + FeCl3 → 3KCl+ Fe(OH)3
- 2KOH + Mg(NO3)2 → 2KNO3+ Mg(OH)2
- KOH + Al(OH)3 → KAlO2+ 2H2O
- KOH + Cr(OH)3 → KCrO2+ 2H2O
- 2KOH + Zn(OH)2 → K2ZnO2+ 2H2O
- KOH + KHCO3 → K2CO3 + H2O
- KOH + KHSO3 → K2SO3 + H2O
- 2KOH + Ba(HSO3)2 → K2SO3 + BaSO3 + 2H2O
- 2KOH + Ba(HCO3)2 → K2CO3 + BaCO3 + 2H2O
- 2KOH + Ca(HCO3)2 → K2CO3 + CaCO3 + 2H2O
- 2KOH + Ca(HSO3)2 → K2SO3 + CaSO3 + 2H2O
- 2KOH + Cl2 → KCl + KClO + H2O
- 6KOH + 3Cl2 -90oC→ 5KCl + KClO3 + 3H2O
- 2KOH + Al2O3 → 2KAlO2 + H2O
- 2KOH + ZnO → K2ZnO2 + H2O
- 2KOH + H2S → K2S + 2H2O
- KOH + H2S → KHS + H2O
- KOH + CH3COOH → CH3COOK + H2O
- KOH + NH4Cl -to→ KCl+ NH3 + H2O
- KOH + NH4NO3 -to→ KNO3+ NH3 + H2O
- 2KOH + (NH4)2SO4 -to→ K2SO4+ 2NH3 + 2H2O
- CH3COOCH3 + KOH -H2O,to→ CH3COOK + CH3OH
- CH3COOC2H5 + KOH -H2O,to→ CH3COOK + C2H5OH
- C2H5Cl + KOH -to→ KCl + C2H5OH
- C2H5Br + KOH -to→ KBr + C2H5OH
- C2H5Br + KOH -toC2H5OH→ KBr + C2H4 + H2O
- C2H5Cl + KOH -toC2H5OH→ KCl + C2H4 + H2O
- C6H5OH + KOH → C6H5OK + H2O
- 2Al + 2KOH + 2H2O → 2KAlO2 + 3H2
- Zn + 2KOH -to→ K2ZnO2 + H2
- KOH + KHS → K2S + H2O
- 2KOH + 2NaHS → K2S + Na2S + 2H2O
- 2KOH + 2NaHSO3 → K2SO3 + Na2SO3 + 2H2O
- 2KOH + 2NaHCO3 → K2CO3 + Na2CO3 + 2H2O
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)








 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



