KOH + CuSO4 → K2SO4+ Cu(OH)2 | KOH ra K2SO4 | KOH ra Cu(OH)2 | CuSO4 ra K2SO4 | CuSO4 ra Cu(OH)2
Phản ứng KOH + CuSO4 hay KOH ra K2 SO4 hoặc KOH ra Cu(OH)2 hoặc CuSO4 ra K2 SO4 hoặc CuSO4 ra Cu(OH)2 thuộc loại phản ứng trao đổi đã được cân bằng chính xác và chi tiết nhất. Bên cạnh đó là một số bài tập có liên quan về KOH có lời giải, mời các bạn đón xem:
2KOH + CuSO4 → K2SO4+ Cu(OH)2
Điều kiện phản ứng
- Phản ứng xảy ra ngay điều kiện thường.
Cách thực hiện phản ứng
- Nhỏ từ từ dung dịch KOH vào ống nghiệm chứa CuSO4.
Hiện tượng nhận biết phản ứng
- Sau phản ứng thu được kết tủa xanh.
Bạn có biết
- Tương tự CuSO4, các muối của kim loại đồng như CuCl2, Cu(NO3)2… cũng phản ứng với KOH tạo kết tủa xanh.
- Phản ứng của KOH với CuSO4 là phản ứng trao đổi.
Ví dụ minh họa
Ví dụ 1:
Nhỏ từ từ dung dịch KOH vào ống nghiệm chứa CuSO4. Hiện tượng thu được sau phản ứng là
A. xuất hiện kết tủa trắng.
B. xuất hiện kết tủa nâu đỏ.
C. xuất hiện kết tủa sau đó kết tủa tan.
D. xuất hiện kết tủa xanh.
Hướng dẫn giải
2KOH + CuSO4 → K2SO4+ Cu(OH)2
Cu(OH)2: kết tủa xanh.
Đáp án D.
Ví dụ 2:
Phản ứng nào sau đây là phản ứng trao đổi?
A. KOH + CO2 → KHCO3
B. 2KOH + CO2 → K2CO3+ H2O
C. 2K + 2HCl → 2KCl + H2
D. 2KOH + CuSO4 → K2SO4 + Cu(OH)2
Hướng dẫn giải
2KOH + CuSO4 → K2SO4 + Cu(OH)2 là phản ứng trao đổi.
Đáp án D.
Ví dụ 3:
Cho 100ml CuSO4 0,01M phản ứng vừa đủ với dung dịch KOH thu được kết tủa X. Khối lượng kết tủa X là
A. 0,098g. B. 0,98g. C. 0,754g. D. 1,10g.
Hướng dẫn giải
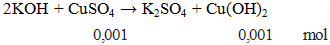
mmuối = 0,001.98 = 0,098gam.
Đáp án A.
Xem thêm các phương trình hóa học hay khác:
- 2KOH + CO2 → K2CO3 + H2O
- KOH + CO2 → KHCO3
- 2KOH + SO2 → K2SO3 + H2O
- KOH + SO2 → KHSO3
- KOH + HCl → KCl + H2O
- KOH + HNO3 → KNO3 + H2O
- 2KOH + H2SO4 → K2SO4+ 2H2O
- 2KOH + FeSO4 → K2SO4+ Fe(OH)2
- 3KOH + FeCl3 → 3KCl+ Fe(OH)3
- 2KOH + Mg(NO3)2 → 2KNO3+ Mg(OH)2
- KOH + Al(OH)3 → KAlO2+ 2H2O
- KOH + Cr(OH)3 → KCrO2+ 2H2O
- 2KOH + Zn(OH)2 → K2ZnO2+ 2H2O
- KOH + KHCO3 → K2CO3 + H2O
- KOH + KHSO3 → K2SO3 + H2O
- 2KOH + Ba(HSO3)2 → K2SO3 + BaSO3 + 2H2O
- 2KOH + Ba(HCO3)2 → K2CO3 + BaCO3 + 2H2O
- 2KOH + Ca(HCO3)2 → K2CO3 + CaCO3 + 2H2O
- 2KOH + Ca(HSO3)2 → K2SO3 + CaSO3 + 2H2O
- 2KOH + Cl2 → KCl + KClO + H2O
- 6KOH + 3Cl2 -90oC→ 5KCl + KClO3 + 3H2O
- 2KOH + Al2O3 → 2KAlO2 + H2O
- 2KOH + ZnO → K2ZnO2 + H2O
- 2KOH + H2S → K2S + 2H2O
- KOH + H2S → KHS + H2O
- KOH + CH3COOH → CH3COOK + H2O
- KOH + NH4Cl -to→ KCl+ NH3 + H2O
- KOH + NH4NO3 -to→ KNO3+ NH3 + H2O
- 2KOH + (NH4)2SO4 -to→ K2SO4+ 2NH3 + 2H2O
- CH3COOCH3 + KOH -H2O,to→ CH3COOK + CH3OH
- CH3COOC2H5 + KOH -H2O,to→ CH3COOK + C2H5OH
- C2H5Cl + KOH -to→ KCl + C2H5OH
- C2H5Br + KOH -to→ KBr + C2H5OH
- C2H5Br + KOH -toC2H5OH→ KBr + C2H4 + H2O
- C2H5Cl + KOH -toC2H5OH→ KCl + C2H4 + H2O
- C6H5OH + KOH → C6H5OK + H2O
- 2Al + 2KOH + 2H2O → 2KAlO2 + 3H2
- Zn + 2KOH -to→ K2ZnO2 + H2
- KOH + KHS → K2S + H2O
- 2KOH + 2NaHS → K2S + Na2S + 2H2O
- 2KOH + 2NaHSO3 → K2SO3 + Na2SO3 + 2H2O
- 2KOH + 2NaHCO3 → K2CO3 + Na2CO3 + 2H2O
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)








 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



