Giáo án Hóa học 10 Chương 2: Bảng tuần hoàn các nguyên tố hóa học và Định luật tuần hoàn mới nhất
Với mục đích giúp các Thầy / Cô giảng dạy môn Hóa học dễ dàng biên soạn Giáo án Hóa học lớp 10, VietJack biên soạn Bộ Giáo án Hóa học 10 Chương 2: Bảng tuần hoàn các nguyên tố hóa học và Định luật tuần hoàn phương pháp mới theo hướng phát triển năng lực theo 5 bước bám sát mẫu Giáo án môn Hóa học chuẩn của Bộ Giáo dục. Hi vọng tài liệu Giáo án Hóa học 10 này sẽ được Thầy/Cô đón nhận và đóng góp những ý kiến quí báu.
Mục lục Giáo án Hóa học 10 Chương 2: Bảng tuần hoàn các nguyên tố hóa học và Định luật tuần hoàn
- Giáo án Hóa học 10 Bài 7: Bảng tuần hoàn các nguyên tố hóa học
- Giáo án Hóa học 10 Bài 8: Sự biến đổi tuần hoàn cấu hình electron nguyên tử của các nguyên tố hóa học
- Giáo án Hóa học 10 Bài 9: Sự biến đổi tuần hoàn tính chất của các nguyên tố hóa học. Định luật tuần hoàn
- Giáo án Hóa học 10 Bài 10: Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
- Giáo án Hóa học 10 Bài 11: Luyện tập: Bảng tuần hoàn, sự biến đổi tuần hoàn cấu hình electron nguyên tử và tính chất của các nguyên tố hóa học
- Giáo án Hóa học 10 Bài 11: Luyện tập: Bảng tuần hoàn, sự biến đổi tuần hoàn cấu hình electron nguyên tử và tính chất của các nguyên tố hóa học (tiết 2)
Giáo án Hóa học 10 Bài 7: Bảng tuần hoàn các nguyên tố hóa học
I - MỤC TIÊU BÀI HỌC:
1. Kiến thức, kỹ năng, thái độ
Kiến thức
Biết được: Nguyên tắc xây dựng BTH
Hiểu được:
- Cấu tạo BTH
- Mối quan hệ chặt chẽ giữa cấu hình electron nguyên tử với vị trí của nguyên tố trong BTH
Kĩ năng
- Xác định được vị trí của nguyên tố trong BTH (Ô nguyên tố, chu kì, nhóm)
- Từ vị trí của nguyên tố trong BTH xác định được cấu tạo của nguyên tử.
Trọng tâm
- Ô nguyên tố.
- Chu kì nguyên tố.
- Nhóm nguyên tố.
- Mối liên hệ giữa cấu hình electron và vị trí nguyên tố trong bảng tuần hoàn.
Thái độ
- Say mê, hứng thú, tự chủ trong học tập; trung thực; yêu khoa học.
2. Định hướng các năng lực có thể hình thành và phát triển
- Năng lực giải quyết vấn đề, năng lực tư duy, năng lực hợp tác (trong hoạt động nhóm).
- Năng lực thực hành hóa học: từ cấu tạo nguyên tử xác định được vị trí trong bảng tuần hoàn và ngược lại. từ đó giải thích được một số tính chất hóa học giống nhau của một số nguyên tố.
- Năng lực vận dụng kiến thức hóa học vào thực tiễn cuộc sống.
- Năng lực sử dụng ngôn ngữ: Diễn đạt, trình bày ý kiến, nhận định của bản thân.
- Năng lực tính toán qua việc giải các bài tập hóa học có bối cảnh thực tiễn.
II. PHƯƠNG PHÁP VÀ KĨ THUẬT DẠY HỌC
1/ Phương pháp dạy học:
- Phương pháp dạy học nhóm, dạy học nêu vấn đề, hướng dẫn HS tự xây dựng bài và rút ra kết luận.
2/ Các kĩ thuật dạy học
- Hỏi đáp tích cực.
- Dạy học hợp tác theo nhóm nhỏ.
III. CHUẨN BỊ CỦA GIÁO VIÊN VÀ HỌC SINH
1. Giáo viên (GV)
- Làm các slide trình chiếu, giáo án.
- Bảng tuần hoàn các nguyên tố hóa học
- Nam châm (để gắn nội dung báo cáo của HS lên bảng từ).
2. Học sinh (HS)
- Học bài cũ.
- Bảng phụ để làm bài tập nhóm
- Bảng tuần hoàn các nguyên tố hóa
IV. CHUỖI CÁC HOẠT ĐỘNG HỌC
A. Hoạt động trải nghiệm, kết nối (10 phút)
Mục tiêu |
Phương thức tổ chức |
Kết quả |
Đánh giá |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
- Huy động các kiến thức đã được học của HS về chương cấu tạo nguyên tử, cấu hình electron để giải quyết vấn đề mới. |
HĐ nhóm: - GV chia lớp thành 4 nhóm - HS hoàn thành nội dung trong phiêu học tập số 1 để ôn lại kiến thức cũ, vận dụng vào bài học mới. Phiếu học tập số 1 Yêu cầu 1: Hoàn thành nội dung bảng sau
Yêu cầu 2: Dựa vào các dữ liệu vừa tìm cho biết a. Trong bảng tuần hoàn, những nguyên tố nào ở trên nằm cùng hàng. Vì sao ? (dựa vào các dữ liệu vừa xác định) b. Trong bảng tuần hoàn những nguyên tố nào ở trên nằm cùng cột. Vì sao ? (dựa vào các dữ liệu vừa xác định) - Các nhóm trưởng phân công nhiệm vụ cho từng thành viên để hoàn thành nhiệm vụ vào bảng phụ. HĐ chung cả lớp: - GV mời một nhóm báo cáo kết quả, các nhóm khác góp ý, bổ sung. GV tạo mâu thuẩn giữa các nhóm vì sao (Na, Mg, Al) và (K, Fe ) cùng hàng (Na, K) cùng cột, Fe và Mg đều có 2 electron lớp ngoài cùng tại sao không cùng cột . - HS có thể xác định sai số electron hóa trị. - GV chuyển sang hoạt động tiếp theo: HĐ hình thành kiến thức. |
Nguyên tố cùng hàng: (Na, Mg, Al) và (K, Fe) Vì có cùng số lớp electron Nguyên tố cùng cột: Na và K vì có cùng số electron hóa trị. |
+ Qua quan sát: Trong quá trình hoạt động nhóm GV quan sát để phát hiện xem các thành viên có tích cực làm việc, nhất là các HS yếu đã nắm được bài cũ chưa để kịp thời khắc phục. |
...........................................................................................
Tài liệu còn nhiều, mời bạn tải xuống để xem đầy đủ.
Giáo án Hóa học 10 Bài 8: Sự biến đổi tuần hoàn cấu hình electron nguyên tử của các nguyên tố hóa học
I - MỤC TIÊU BÀI HỌC:
1. Kiến thức, kỹ năng, thái độ
Kiến thức: Biết được:
- Đặc điểm cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố nhóm A;
- Sự tương tự nhau về cấu hình electron lớp ngoài cùng của nguyên tử (nguyên tố s, p) là nguyên nhân của sự tương tự nhau về tính chất hoá học các nguyên tố trong cùng một nhóm A;
- Sự biến đổi tuần hoàn cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố khi số điện tích hạt nhân tăng dần chính là nguyên nhân của sự biến đổi tuần hoàn tính chất của các nguyên tố.
- Các nguyên tố và tính chất hóa học cơ bản của một số nhóm A tiêu biểu.
Kỹ năng:
- Dựa vào cấu hình electron của nguyên tử, suy ra cấu tạo nguyên tử, đặc điểm cấu hình electron lớp ngoài cùng.
- Dựa vào cấu hình electron, xác định nguyên tố s, p.
- Dựa vào số eletron lớp ngoài cùng xác định tính chất hóa học cơ bản của các nguyên tố.
*Trọng tâm
Đặc điểm cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố nhóm A
- Trong một chu kì.
- Trong một nhóm A.
Thái độ: Tích cực, chủ động nắm bắt kiến thức, hứng thú với bộ môn, phát huy khả năng tư duy của hs
2. Định hướng các năng lực có thể hình thành và phát triển
- Năng lực tự học và giải quyết vấn đề.
- Năng lực tư duy, năng lực hợp tác (trong hoạt động nhóm).
- Năng lực vận dụng kiến thức hóa học vào thực tiễn cuộc sống.
- Năng lực thực hành hóa học: quan sát hiện tượng, nêu và giải thích các hiện tượng xảy ra khi tiến hành thí nghiệm kim loại kiềm với H2O
- Năng lực giao tiếp và sử dụng ngôn ngữ: Diễn đạt, trình bày ý kiến, nhận định của bản thân.
- Năng lực tính toán qua việc giải các bài tập hóa học.
II. PHƯƠNG PHÁP VÀ KĨ THUẬT DẠY HỌC
1/ Phương pháp dạy học: Phương pháp dạy học nhóm, dạy học nêu vấn đề.
2/ Các kĩ thuật dạy học
- Hỏi đáp tích cực.
- Khăn trải bàn.
- Nhóm nhỏ.
III. CHUẨN BỊ CỦA GIÁO VIÊN VÀ HỌC SINH
1. Giáo viên (GV)
- Làm các slide trình chiếu, giáo án.
- Bảng phụ
- Thẻ trả lời cho hs
- Nam châm (để gắn nội dung báo cáo của HS lên bảng từ).
- Bảng cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố nhóm A được photocopy thành khổ lớn (Bảng 5/trang 38/SGK).
- Video Phản ứng của các kim loại nhóm IA tác dụng với nước.
- Video Sự linh động của các halogen.
2. Học sinh (HS)
- Học bài cũ, xem lại các kiến thức của bài bảng tuần hoàn các nguyên tố hóa học.
- Tập lịch cũ cỡ lớn hoặc bảng phụ hoạt động nhóm.
- Bút mực viết bảng.
IV. CHUỖI CÁC HOẠT ĐỘNG HỌC
A. Hoạt động trải nghiệm, kết nối (8 phút)
Mục tiêu |
Phương thức tổ chức |
Kết quả |
Đánh giá |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Vận dụng kiến thức cấu hình electron nguyên tử; Bảng tuần hoàn các nguyên tố hóa học hướng cho học sinh phát hiện và tìm ra quy luật kích thích tư duy từ đó hình thành kiến thức mới. + Xác định được vị trí của các nguyên tố trong chu kỳ 3 + Biết được sự biến thiên số eletron lớp ngoài cùng của các nguyên tố trong chu kỳ 3. |
1. Chuyển giao nhiệm vụ GV chia lớp thành 4 nhóm để hoàn thành PHT số 1 PHIẾU HỌC TẬP SỐ 1 Hoàn thành nội dung bảng sau
2. Thực hiện nhiệm vụ học tập - Gv hướng dẫn HS dùng kĩ thuật tia chớp. - GV cho học sinh hoạt động nhóm để chuẩn bị và chơi trò chơi tốc độ, hoàn thành phiếu học tập số 1. (Nhóm hoàn thành đúng và nhanh nhất đạt 1 điểm cộng) Nhóm 1: Na, Ar và K Nhóm 2: Mg và Cl Nhóm 3: Al và S Nhóm 4: K và Li - Giáo viên treo bảng có nội dung khuyết cho thành viên các nhóm gắn nội dung trả lời vào chỗ khuyết. HS ghi đáp án vào phiếu trả lời gv chuẩn bị sẵn . 3. Báo cáo, thảo luận HĐ chung cả lớp: Sau đó giáo viên hướng dẫn cả lớp bổ sung đánh giá nhóm thắng cuộc đồng thời hoàn thiện phiếu học tập. - Giáo viên gợi ý học sinh tìm ra trên bảng kiến thức có sự biến đổi nào đặc biệt? (có thể dùng phấn màu để gợi ) GV đặt vấn đề: Số eletron lớp ngoài cùng của chu kỳ 3 tăng dần từ 1 đến 8. Vậy ở các chu kỳ khác số eletron lớp ngoài cùng biến đổi thế nào? Sự biến đổi đó được gọi là gì? - GV chuyển sang hoạt động tiếp theo: HĐ hình thành kiến thức. |
HS hoàn thành phiếu học tập số 1
Mâu thuẩn nhận thức: HS không biết được sự biến đổi số eletron lớp ngoài cùng của các chu kỳ 2, 3, 4 có giống nhau không và không biết được sự biến đổi đó được gọi là gì. |
- Đánh giá giá kết quả hoạt động: Thông qua quan sát: Trong quá trình HS HĐ nhóm, GV cần quan sát kĩ tất cả các nhóm, kịp thời phát hiện những khó khăn, vướng mắc của HS và có giải pháp hỗ trợ hợp lí. Thông qua báo cáo các nhóm và sự góp ý, bổ sung của các nhóm khác, GV biết được HS đã có được những kiến thức nào, những kiến thức nào cần phải điều chỉnh, bổ sung ở các HĐ tiếp theo. |
...........................................................................................
Xem thêm các bài soạn Giáo án Hóa học lớp 10 theo hướng phát triển năng lực mới nhất, hay khác:
- Giáo án Hóa học 10 Chương 3: Liên kết hóa học
- Giáo án Hóa học 10 Chương 4: Phản ứng oxi hóa - khử
- Giáo án Hóa học 10 Chương 5: Nhóm Halogen
- Giáo án Hóa học 10 Chương 6: Oxi - Lưu huỳnh
- Giáo án Hóa học 10 Chương 7: Tốc độ phản ứng và cân bằng hóa học
Để học tốt lớp 10 các môn học sách mới:
- Giải bài tập Lớp 10 Kết nối tri thức
- Giải bài tập Lớp 10 Chân trời sáng tạo
- Giải bài tập Lớp 10 Cánh diều
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Giáo án Vật Lí lớp 10 chuẩn nhất của chúng tôi được biên soạn bám sát nội dung sgk Vật Lí 10 theo chuẩn Giáo án của Bộ GD & ĐT.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giáo án lớp 10 (các môn học)
- Giáo án điện tử lớp 10 (các môn học)
- Giáo án Ngữ văn 10
- Giáo án Toán 10
- Giáo án Tiếng Anh 10
- Giáo án Vật Lí 10
- Giáo án Hóa học 10
- Giáo án Sinh học 10
- Giáo án Lịch Sử 10
- Giáo án Địa Lí 10
- Giáo án Kinh tế Pháp luật 10
- Giáo án Tin học 10
- Giáo án Công nghệ 10
- Giáo án Giáo dục quốc phòng 10
- Giáo án Hoạt động trải nghiệm 10
- Đề thi lớp 10 (các môn học)
- Đề thi Ngữ Văn 10 (có đáp án)
- Chuyên đề Tiếng Việt lớp 10
- Đề cương ôn tập Văn 10
- Đề thi Toán 10 (có đáp án)
- Đề thi cương ôn tập Toán 10
- Đề thi Toán 10 cấu trúc mới (có đáp án)
- Đề thi Tiếng Anh 10 (có đáp án)
- Đề thi Vật Lí 10 (có đáp án)
- Đề thi Hóa học 10 (có đáp án)
- Đề thi Sinh học 10 (có đáp án)
- Đề thi Lịch Sử 10 (có đáp án)
- Đề thi Địa Lí 10 (có đáp án)
- Đề thi Kinh tế & Pháp luật 10 (có đáp án)
- Đề thi Tin học 10 (có đáp án)
- Đề thi Công nghệ 10 (có đáp án)
- Đề thi Giáo dục quốc phòng 10 (có đáp án)

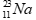
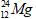
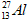
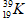





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

